某溶液可能含有Cl—、SO42—、CO32—、NH4+、Fe3+、Fe2+、Al3+和Na+。某同学为了确定其成分,取部分试液,设计并完成了如下实验:
下列说法正确的是
| A.原溶液中c(Fe3+)="0.2" mol·L—1 |
| B.原溶液中至少有4种离子存在,其中Cl—一定存在,且c(Cl—)≥0.2 mol·L—1 |
| C.原溶液中SO42—、NH4+、Na+一定存在,CO32—、Al3+一定不存在 |
| D.要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入适量氯水,无现象,再加KSCN溶液,溶液呈血红色,则含有Fe2+ |
无色的混合气体甲中可能含NO、CO2、NO2、NH3、N2中的几种。将100 mL气体甲经过下图实验处理,结果得到酸性溶液,而几乎无气体剩余,则气体甲的组成可能为( )
| A.NH3、NO2、N2 | B.NH3、NO、CO2 |
| C.NH3、NO2、CO2 | D.NO、CO2、N2 |
下图为海水综合利用的工业流程图,判断下列说法正确的是
| A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 |
| B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.在过程④、⑥反应中每氧化0.2 mol Br-需消耗0.1mol Cl2 |
| D.除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
下列各组稀溶液:①氨水和硝酸银 ②NaAlO2和盐酸 ③硫酸氢钠和氢氧化钡 ④硝酸和碳酸钠。只用试管、滴管及闻气味就能鉴别的是
| A.③④ | B.①②④ | C.①②③④ | D.②④ |
某无色溶液中含有:①K+、②Ba2+、③Cl-、④Br-、⑤SO32-、⑥CO32-、⑦SO42-中的一种或几种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:下列结论正确的是
| 步骤 |
操作 |
现象 |
| ① |
用pH试纸检验 |
溶液的pH大于7 |
| ② |
向溶液中滴加氯水,再加入CCl4振荡,静置 |
CCl4层呈橙色 |
| ③ |
向②所得溶液中加入Ba(NO3)2溶液和稀HNO3 |
有白色沉淀产生 |
| ④ |
过滤,向滤液中加入AgNO3溶液和稀HNO3 |
有白色沉淀产生 |
A.可能含有的离子是①②⑦ B.肯定含有的离子是①④
C.不能确定的离子是①③⑦ D.肯定没有的离子是②⑤⑥
有一无色溶液,可能含有K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是( )
| A.肯定有Al3+、Mg2+、NH4+、Cl- | B.可能有K+、Cl-、MnO4- |
| C.肯定有Al3+、Mg2+、SO42- | D.肯定有K+、HCO3-、MnO4- |
某溶液中只可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是
| A.溶液中的阳离子只有H+、Mg2+、Al3+可能含有Fe3+ |
| B.溶液中一定不含CO32-和NO3-,一定含有SO42- |
| C.溶液中c(NH4+)=0.3 mol/L |
| D.c(H+)∶c (Al3+)∶c(Mg2+)=1∶1∶1 |
下列说法正确的是
| A.某溶液中滴加硝酸酸化的Ba(NO3)2溶液有白色沉淀,该溶液一定有SO42- |
| B.某溶液中滴加盐酸,产生无色无味的气体,将该气体通入澄清的石灰水中产生白色沉淀,则该溶液一定有CO32- |
| C.某溶液中滴加NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,则该溶液中一定有NH4+ |
| D.某溶液中滴加AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,则该溶液中一定有Cl- |
实验是研究化学的基础,下图中所示的实验方法、装置或操作均正确的是 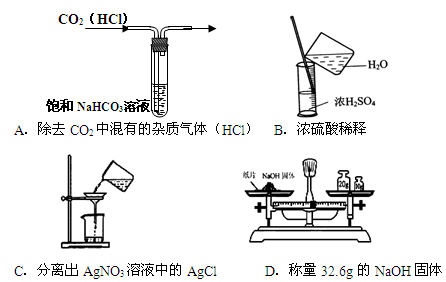
某溶液中可能含有下列6种离子中的某几种:Cl—、SO42—、CO32—、NH4+、Na+、K+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
| A.一定存在SO42—、CO32—、NH4+,可能存在Cl—、Na+、K+ |
| B.一定存在Cl—、SO42—、CO32—、NH4+,一定不存在Na+、K+ |
| C.c(CO32—)=0.01mol·L-1,NH4+>SO42— |
| D.如果上述6种离子都存在,则c(Cl—)>c(SO42—) |
向某二价金属M的M(OH)2溶液中加入过量的NaHCO3溶液,生成了MCO3沉淀,过滤,将沉淀置于足量的稀盐酸中,充分反应后,在标准状况下收集到V L气体,如果计算金属M的相对原子质量,你认为还必需提供下列哪项数据( )
| A.M(OH)2溶液的物质的量浓度 |
| B.与M CO3反应的盐酸的物质的量浓度 |
| C.MCO3的质量 |
| D.题给条件充足,不需要再补充数据 |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+、Al3+和Na+。某同学为了确认其成分,取部分试液,设计并完成了如下实验:
下列说法正确的是
| A.原溶液中c(Fe3+)=0.2 mol·L-1 |
| B.要确定原溶液中是否含有Fe2+,其操作为取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有Fe2+ |
| C.SO42-、NH4+、Na+一定存在,CO32-,Al3+一定不存在 |
| D.溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2 mol·L-1 |
下列实验操作正确且能达到相应实验目的的是
| |
实验目的 |
实验操作 |
| A |
称取2.0gNaOH固体 |
先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体 |
| B |
制备Fe(OH)3胶体 |
向沸水中逐滴加入少量氯化铁饱和溶液,继续加热煮沸至液体变为红褐色 |
| C |
检验溶液中是否含有SO42- |
取少量试液于试管中,先加入BaCl2溶液,再滴加稀盐酸,若产生的白色沉淀不溶解,则说明溶液中含有SO42- |
| D |
萃取碘水中的碘 |
将碘水倒入分液漏斗,然后再注入酒精,振荡,静置分层后,下层液体从下口放出,上层液体从上口倒出 |
某强酸性溶液中可能存在 中的若干种,现取适量溶液进行如下实验
中的若干种,现取适量溶液进行如下实验
下列有关判断正确的是
A.原溶液中一定有.
B.原溶液中一定没有
c.步骤③中反应的离子方程式为
D.气体A、B之间肯定不能发生反应
钢铁等铁制品是应用最广泛的金属材料,铁元素的单质及其化合物在元素化合物世界始终扮演着重要角色。
I.打磨过的细铁丝可在纯氧中剧烈燃烧,最终生成黑色固体,其化学式为 ;铁粉与水蒸气在高温下也可生成该黑色固体,反应的化学方程式为 。
II.某校探究性学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如下:
请回答下列问题:
(1)步骤②中,除发生反应Fe +2HCl=FeCl2+H2↑外,其他可能反应的离子方程式为 。
(2)若溶液B中只含有Fe2+而不含Fe3+,可证明该事实的实验方法是( )
①先加氯水,后加KSCN溶液后显红色;
②先加KSCN溶液,不显红色,再加氯水后显红色;
③滴加NaOH溶液,只产生白色沉淀,迅速变为灰绿色,最后呈红褐色;
④只滴加KSCN溶液不显红色。
| A.①② | B.②⑨ | C.⑨④ | D.①④ |
(3)步骤⑤产生金属铜的化学方程式为 。
Ⅲ.金属的腐蚀所导致的钢铁损耗占钢铁年产量的l/4还多。在钢铁的吸氧腐蚀过程中,正极反应式为 ,若此过程中共生成了8 gFe2O3,则转移的电子的物质的量为 。