甲、乙两同学拟用实验确定某酸HA是弱电解质。他们设计的方案(理论方案)分别是:
甲:①称取一定质量的HA配制0.1 mol/L的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=3的两种酸溶液各100 mL;
②分别取这两种溶液各1 mL,加水稀释为100 mL;
③用两支试管分别取相同体积的两种稀释液,同时加入纯度相同、颗粒大小均等的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是 。
(2)甲方案中,能说明HA是弱电质的理由是测得溶液的pH___1(选填“>”、“<”、“=”)。
(3)关于pH试纸的使用方法,下列叙述正确的是 。
a.pH试纸在使用之前应用蒸馏水润湿
b.将pH试纸直接插入待测溶液,取出后再与标准比色卡对比
c.pH试纸测出的数值应该保留一位小数
d.能使pH试纸显红色的溶液显酸性
(4)乙方案中,说明HA是弱电解质的现象是 。
已知2NO2(g) N2O4(g) ΔH(298K)=-52.7kJ·mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
N2O4(g) ΔH(298K)=-52.7kJ·mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
Ⅰ.该小组的同学取了两个烧瓶A和B,分别加入相同浓度的NO2与N2O4的混合气体,中间用夹子夹紧,并将A和B浸入到已盛有水的两个烧杯中(如图所示),然后分别向两个烧杯中加入浓硫酸和NH4NO3固体。
请回答:
(1)A中的现象 ,B中的现象 ;
(2)由此可知,降低温度,该化学平衡向 (填“正”或“逆”)反应方向移动;
(3)该化学反应的浓度平衡常数表达式为 ,升高温度,该反应中NO2的转化率将 (填“增大”、“减小”或“不变”)。
Ⅱ.在三支容积均为30cm3针筒中分别抽入10cm3NO2气体,将针筒前端封闭。
(1)将第二支针筒活塞迅速推至5cm3处,此时气体的颜色变深,一段时间后气体颜色又变浅了,但仍比第一支针筒气体的颜色深。
①推进针筒后颜色变深的原因是 ;
②一段时间后气体颜色又变浅的原因是 ;
③由此实验得出的结论是 。
(2)将第三支针筒活塞拉至20cm3处,该同学观察到的现象是 ;在此过程中,该反应的化学平衡常数将 (填“增大”、“减小”或“不变”,下同),NO2的转化率将 。
下图所示为某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。图中A试管盛有无水乙醇(沸点为78℃),B处为螺旋状的细铜丝,C处为无水硫酸铜粉末,干燥管D中盛有碱石灰,E为新制的氢氧化铜,F为氧气的发生装置。
(1)在实验过程中,需要加热的仪器(或区域)有(填仪器或区域的代号A~F)___。
(2)B处发生的化学反应方程式为________________。
(3)C处应出现的现象是_________________,
D处使用碱石灰的作用是__________________,
E处应出现的实验现象是 _____________________,
F处可以添加的固体药品是 ______________。
(4)若本实验中拿去F装置(包括其上附的单孔塞和导管),同时将A试管处原来的双孔塞换成单孔塞用以保证装置的气密性,其它操作不变,则发现C处无明显变化,而E处除了依然有上述(3)中所出现的现象之外,还有气体不断地逸出。由此推断此时B处发生反应的化学方程式为______________。
一位同学为探究元素周期表中元素性质的递变规律,设计了如下列实验。
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:________与盐酸反应最剧烈,________与盐酸反应的速度最慢;________与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为________________
Ⅱ.利用下图装置可验证同主族元素非金属性的变化规律:
(3)仪器B的名称为________,干燥管D的作用为____________。
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液_________________的现象,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用________溶液吸收尾气。
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液________的现象,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有_______溶液的洗气瓶除去。
某同学做元素周期律性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表(记录现象时随手记在纸片上,不对应,需整理):
| 实验方案 |
实验现象 |
| ①用砂纸擦后的镁带与沸水反应再向反应液中滴加酚酞 |
A.浮于水面,熔成小球,在水面上无定向移动随之消失,溶液变成红色 |
| ②向新制的H2S饱和溶液中滴加新制的氯水 |
B.产生大量气体,可在空气中燃烧,溶液变成浅红色 |
| ③钠与滴有酚酞试液的冷水反应 |
C.反应不十分剧烈,产生气体可以在空气中燃烧 |
| ④镁带与2 mol·L-1的盐酸反应 |
D.剧烈反应,产生的气体可以在空气中燃烧 |
| ⑤铝条与2 mol·L-1的盐酸反应 |
E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向氯化铝溶液中滴加氢氧化钠 |
F.生成淡黄色沉淀 |
请帮助该同学整理并完成实验报告。
(1)实验目的:______________________。
(2)实验用品:______________________。
(3)实验内容:
| 实验方案 (填序号) |
实验现象 (填序号) |
有关化学方程式 |
| |
|
|
| |
|
|
| |
|
|
| |
|
|
| |
|
|
| |
|
|
(4)实验结论:_____________________。
(5)请用物质结构理论简单说明具有上述结论的原因___________________
(9分)O3氧化海水中的I-是大气中碘的主要来源,将O3通入稀硫酸酸化的NaI溶液中进行模拟研究。
(1)为探究外界条件对I2生成速率的影响,做了如下三组实验,填写表中的空白处。
| 编号 |
实验目的 |
反应物 |
反应前溶液的pH |
温度 |
| 1 |
对照组 |
O3+NaI+H2SO4 |
5.2 |
25℃ |
| 2 |
①__________ |
O3+NaI+H2SO4+FeCl2 |
5.2 |
②_____ |
| 3 |
探究温度对反应速率的影响 |
O3+NaI+H2SO4 |
③_______ |
5℃ |
(2)为测定生成I2的量,用移液管取20.00mL反应后溶液于锥形瓶中,用 c mol·L-1的Na2S2O3标准液滴定,消耗V mLNa2S2O3溶液。
已知:①H2S2O3是一种弱酸;②2Na2S2O3+ I2= Na2S4O6+2NaI
①该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是_____________;
②该实验中可选用_______(填物质名称)作指示剂。
③反应后溶液中碘的含量为_________ g·L-1。
④甲同学认为在滴定前应微热溶液,以排除溶液中溶解的O3和O2,不然会使滴定结果偏_____(填“低”或“高”)。
如图是某研究性学习小组设计制取氯气,并以氯气为反应物进行特定反应的装置。
(1)要将C装置接入B和D之间,正确的接法是: a→ → →d。
(2)实验开始时先点燃A处酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为 。
(3)D处反应完毕后,关闭旋塞K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是 ,B的作用是 。
(4)用量筒量取20 mL E中溶液,倒入已检查完气密性良好的分液漏斗中,然后再注入10 mL CCl4,盖好玻璃塞(如图),振荡,静置于铁架台上,等分层后取上层液和下层液,呈黄绿色的是 (填“上层液”或“下层液”),再装入如图所示的烧杯中,能使有色布条褪色的是 (同上)。
(5)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由 。
将氯气用导管通入较浓的NaOH和H2O2的混合液中,在导管口与混合液的接触处有闪烁的红光出现。这是因为通气后混合液中产生的ClO-被H2O2还原,发生剧烈反应,产生能量较高的氧分子,它立即转变为普通氧分子,将多余的能量以红光放出。进行此实验,所用的仪器及导管如下图。
| 编号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
| 仪器及 导管 |
 |
 |
 |
 (一个) |
 (一个) |
 橡皮管 |
根据要求填写下列空白:
(1)组装氯气发生器时,应选用的仪器及导管(填写图编号)是 。
(2)实验进行中,按气流方向从左到右的顺序,气体流经的各仪器及导管的编号依次是 。
(3)仪器①的橡皮塞上应有 个孔,原因是 。
(4)实验时,仪器①中除观察到红光外还有 现象。
(5)实验需用约10% H2O2溶液100 mL,现用市售30%(密度近似为1 g·cm-3)H2O2来配制,其具体配制方法是 。
(6)实验时仪器①中ClO-与H2O2反应的离子方程式是 。
甲同学探究NO2的氧化性;设计了如下实验装置:
(1)该装置的明显缺陷是:________________________。
(2)实验开始后,发现Zn溶解,但未发现有气体逸出,同学猜想可能是因为HNO3被还原生成NH4+
写出反应的离子方程式:__________________,如何验证该猜想:_______________。
(3)重新调整HNO3浓度后,发现A中有红棕色气体逸出,设计实验,证明NO2具有氧化性(药品任意选择,合理即可)
| 步骤 |
现象 |
结论 |
| 取少量C中反应后的溶液 置于试管中,__________ |
__________ |
NO2具有氧化性 |
(4)乙同学对甲的实验结果产生质疑,提出假设:
假设一:NO2氧化了SO32-
假设二:HNO3氧化了SO32-
问题1:假设二_____(“是”或“否”)合理,
理由:___________________(用化学方程式回答)
问题2:若要验证NO2具有氧化性,你的实验方案是:_____________________。
(每空2分,共10分)某同学学习过元素周期律、元素周期表后,为了探究同主族元素性质的递变规律,自己设计了一套实验方案,并记录了有关实验现象。现在请你帮助该同学完成实验报告。
Ⅰ.实验目的:探究同一主族元素性质的递变规律。
Ⅱ.实验用品:碘化钠溶液、溴化钾溶液、溴水、氯水、四氯化碳。
仪器:(1) ;(2) 。(请填写两件主要的玻璃仪器)
Ⅲ.实验内容:
| 序号 |
实验方案 |
实验现象 |
| ① |
将少量氯水滴入盛有适量KBr溶液的试管中,振荡;再滴入少量四氯化碳,振荡 |
滴入氯水后,溶液由无色变为橙色,滴入四氯化碳后,水层颜色变浅,四氯化碳层(下层)变为橙红色 |
| ② |
将少量溴水滴入盛有适量NaI溶液的试管中,振荡;再滴入少量四氯化碳,振荡 |
滴入溴水后,溶液由无色变为黄色,滴入四氯化碳后,水层颜色变浅,四氯化碳层(下层)变为紫色 |
Ⅳ.实验结论:(3)_________________________________。
Ⅴ.问题和讨论:
①请用结构理论简单说明得出上述结论的原因:(4) 。
②由于F2如同Na过于活泼,很难设计一个简单的置换反应实验验证其氧化性强弱。试列举一项事实说明F的非金属性比Cl强:(5) 。
某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(1)请写出SO2与过量NaOH溶液反应的离子方程式:__________________________。
(2)吸收尾气(Cl2)一段时间后,吸收液(强碱性)中肯定存在的阴离子有OH-和 、_____。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响)
① 提出合理假设。
假设1:只存在SO32-
假设2:既不存在SO32-,也不存在ClO-;
假设3:_____________。
②要证明假设1是否成立,设计实验方案,进行实验。请写出实验以及预期现象和结论。限选实验试剂:3mol·L-1H2SO4、1mol·L-1NaOH、0.01mol·L-1KMnO4、淀粉-KI溶液。
| 实验 |
预期现象和结论 |
| |
|
某学习小组探究溴乙烷的消去反应并验证产物。
实验原理:CH3CH2Br + NaOH CH2=CH2↑ + NaBr + H2O
CH2=CH2↑ + NaBr + H2O
实验过程:组装如图所示装置,检查装置气密性,向烧瓶中注入10mL溴乙烷和15mL饱和氢氧化钠乙醇溶液,微热,观察实验现象。一段时间后,观察到酸性KMnO4溶液颜色褪去。
(1)甲同学认为酸性KMnO4溶液颜色褪去说明溴乙烷发生了消去反应,生成了乙烯;而乙同学却认为甲同学的说法不严谨,请说明原因: 。
(2)丙同学认为只要对实验装置进行适当改进,就可避免对乙烯气体检验的干扰,改进方法为: 。
改进实验装置后,再次进行实验,却又发现小试管中溶液颜色褪色不明显。该小组再次查阅资料,对实验进行进一步的改进。
资料一:溴乙烷于55℃时,在饱和氢氧化钠的乙醇溶液中发生取代反应的产物的百分比为99%,而消去反应产物仅为1%。
资料二:溴乙烷发生消去反应比较适宜的反应温度为90℃~110℃,在该范围,温度越高,产生乙烯的速率越快。
资料三:溴乙烷的沸点:38.2℃。
(3)结合资料一、二可知,丙同学改进实验装置后,溶液颜色褪色不明显的原因可能是_______,此时发生反应的化学方程式为: 。
(4)结合资料二、三,有同学认为应将实验装置中烧瓶改成三颈烧瓶并增加两种仪器,这两种仪器是① 。② 。
某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略)。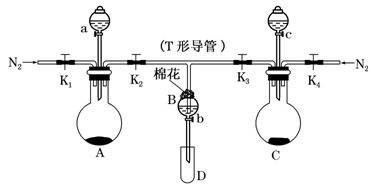
(1)按图连接好装置,检查装置的气密性后添加药品:向A装置的分液漏斗中加入浓盐酸,在圆底烧瓶中加入固体KMnO4;向B装置中加入10 mL FeCl2溶液,棉花浸润________溶液;在C装置的分液漏斗中加入70%的硫酸,向圆底烧瓶中加入固体Na2SO3。
(2)打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2。通入一段时间N2的目的是__________________。
(3)关闭K1,K3,K4,打开活塞a 和K2,逐滴加入浓盐酸,A装置中发生反应的方程式为___________。
(4)当B中溶液变为棕黄色时,停止滴加浓盐酸,夹紧K2,打开活塞b,使约2 mL的溶液流入D试管中,分别取1 mL溶液滴入_______(填试剂名称)和铁氰化钾溶液可以证明其中含有Fe3+和Fe2+。此时B中发生反应的离子方程式为____________。
(5)打开K3和活塞c,逐滴加入70%的硫酸,当B中溶液颜色逐渐变为_____色,停止滴加70%的硫酸,夹紧K3,打开活塞b,使约2 mL的溶液流入D试管中,并检验其中的离子。此时B中发生反应的离子方程式为______________。
(6)结合实验现象判断Fe3+、Cl2、SO2氧化性由强到弱的顺序为___________。
(13分)某研究性学习小组用下图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在 中,再加水稀释。
(2)下列实验方案适用于在装置A中制取所需SO2的是 。
a.Na2SO3固体与浓硝酸 b.Na2SO3固体与浓硫酸
c.CaSO3固体与稀硫酸 d.碳与热的浓硫酸
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)往FeCl3溶液中通入足量SO2,反应的离子方程式为 。
(5)能表明SO2的还原性强于I-的反应现象为__________________。
(6)装置E的作用为________________。
(7)在上述装置中通入过量的SO2,为了验证C中SO2与Fe3+发生了氧化还原反应,取C中的溶液,分成两份,并设计了如下实验:
方案①:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的是 ,理由是 。
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。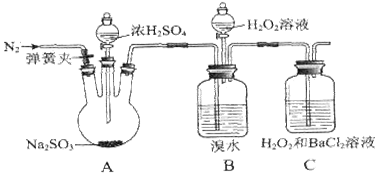
| 实验操作 |
实验现象 |
| ⅰ.打开A中分液漏斗活塞,滴加浓硫酸 |
A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
| ⅱ.取C中沉淀加入盐酸 |
C中白色沉淀不溶解 |
| ⅲ.打开B中分流漏斗活塞,逐滴滴加H2O2 |
开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(1)A中发生反应的化学方程式是_______________________
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是_____________。
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是____________
③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:氧化性H2O2>SO2。
(3)ⅲ中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br―
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是___________________________________
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是________。