在化学课上围绕浓硫酸的化学性质进行了如下实验探究,将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。
请回答下列问题:
(1)生成的黑色物质(单质)是 (填化学式)。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是 (填化学式),反应的化学方程式为 。
(3)据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有 (填序号)。
| A.酸性 | B.吸水性 | C.脱水性 | D.强氧化性 |
(4)将(2)中产生的有刺激性气味的气体通入品红溶液中,可以看到品红溶液 ,说明这种气体具有 性;将(2)中产生的有刺激性气味的气体通入水中可生成一种不稳定、易分解的酸,请写出该反应的化学方程式: 。
(5)能否用澄清石灰水鉴别这两种气体? (填“能”或“不能”),若不能,请填写两种能鉴别的试剂 。
某同学在学习了乙醇的知识后,设计了如图所示的实验。操作步骤及观察到的现象如下:
①在试管里加入2 mL乙醇;
②把一端弯成螺旋状的铜丝放在酒精灯外焰中加热变黑;
③立即将铜丝插入盛有乙醇的试管里,铜丝重新变为红色光亮,反复操作几次。请回答下列问题:
(1)该实验的目的是_________________________________________。
(2)写出总的反应化学方程式___________________________________。
(3)在此过程中,铜丝的作用是_________________________________。
为研究亚氯酸钠(NaClO2)吸收SO2的利用率,某课外小组设计如下图所示实验(加热和夹持装置略去)。
(1)甲装置中发生反应的化学方程式为 。
(2)当观察到丙装置中 时(填现象),停止实验。
(3)探究亚氯酸钠与SO2的反应。
①假设SO2被完全反应,检验乙装置中生成的SO42-和C1-,应选用的试剂是 (酸性条件下ClO2-不干扰检验)。
a.稀硝酸
b.稀盐酸
c.BaCl2溶液
d.Ba(NO3)2溶液
e.AgNO3溶液
②完成乙装置中反应的离子方程式:
(4)测定亚氯酸钠的利用率。实验步骤如下:
ⅰ 将乙装置中溶液取出,加入过量KI晶体,再滴入适量稀硫酸,充分反应(ClO2-+4I-+4H+=2H2O+2I2+C1-)。
ⅱ 将步骤ⅰ所得溶液稀释至100. 00mL,取25.00 mL于锥形瓶中,滴入1~2滴淀粉溶液,用0.500 mol·L-1Na2S2O3标准液滴定(I2+2S2O32-=2I-+S4O62-)。重复进行3次滴定,得Na2S2O3溶液体积的平均值为20.00 mL。
①步骤ⅱ中将溶液稀释至100.00mL,需要用到的玻璃仪器有烧杯、玻璃棒、 、 。
②该实验NaClO2的利用率为 。
(5)实验结束后,课外小组同学经讨论认为:增大SO2的溶解量,有利于提高NaClO2的利用率。增大SO2的溶解量的措施有 (填一种)。
某学习小组为探究维生素C的组成和有关性质,进行了以下实验:
①取维生素C样品研碎,称取该试样0.704 g,置于铂舟并放人燃烧管中,不断通入氧气流。用酒精喷灯持续加热样品,样品逐渐消失最后无任何残留物,将生成物(仅有两种物质)先后通过无水硫酸铜和碱石灰,两者分别增重0.288 g和1.056 g,生成物完全被吸收。
②将少许研碎的维生素C样品和适量的紫色石蕊试液充分混合后,溶液颜色变红。
请解答下列问题:
(1)称取的试样中,含有氢原子的物质的量是 mo1;碳元素的质量是 g。
(2)维生素C中 (填“含”、“不含”或“无法确定是否”)有氧元素,理由是根据实验数据可知 。如你回答“含”有,请计算称取的试样中氧原子的物质的量并填入下一空格中;如你回答“不含”等,则下一空格不必填写。称取试样中氧原子的物质的量为 mol。
(3)如果要确定维生素C的分子式,你认为还需要知道的信息是 。
(4)维生素C和紫色石蕊试液混合后,溶液颜色变红,说明维生素C溶液具有 (填“酸”、“碱”或“中”)性。查阅有关资料显示,维生素C具有还原性。请以淀粉溶液、碘水为试剂,写出验证维生素C具有还原性的实验方法和现象: 。
I下列实验操作或对实验事实的描述中正确的是_______________
①石油的分馏实验必须将温度计的水银球插入反应液中,测定反应液的温度,其中冷凝管起到冷凝回流的作用
②将0.1mol•L﹣1的NaOH溶液与0.5mol•L﹣1的CuSO4溶液等体积混合制得氢氧化铜浊液,用于检验醛基
③不慎将苯酚溶液沾到皮肤上,立即用酒精清洗
④配制银氨溶液:在一定量AgNO3溶液中滴加过量氨水即可
⑤分离苯和苯酚的混合液,加入少量浓溴水,过滤
⑥将10滴溴乙烷加入1mL10%的烧碱溶液中加热片刻后,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子.
II某校学生为探究苯与溴发生反应的原理,用如图装置进行实验.
根据相关知识回答下列问题:
(1)实验开始时,关闭K1,开启K2和分液漏斗活塞,滴加苯和液溴的混合液,反应开始.过一会儿,在(Ⅲ)中可能观察到的现象是____________________________________
(2)整套实验装置中能防止倒吸的装置有________________(填装置序号).
(3)反应结束后要使装置(I)中的水倒吸入装置(Ⅱ)中.这样操作的目的是______________________
(4)你认为通过该实验后,有关苯跟溴反应的原理方面能得出的结论是_______________________
某学生用下图所示的装置测定镁的相对原子质量:
(1)①实验前必须对装置进行气密性检查,具体操作是: ;
(2)如果量气管的最大测量体积为50mL(假设条件为标准状况),则取金属镁条(设纯度为100%)的质量不超过 g;(精确到0.001)
(3)实验结束,在读取数据前必须:a冷却,使温度恢复到原来状态;b ;
(4)该学生实验时称取镁条0.051g(已除去氧化膜),实验结果收集到气体48.00mL(已换算到标准状况,其他实验操作均正确),根据实验测定,镁的相对原子质量为 ;产生误差的原因可能是 (写出一点)。
某课外兴趣小组对H2O2的分解速率做了如下实验探究。
(I)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2制取150mL O2所需的时间(秒)
①研究小组在设计方案时。考虑了浓度和 因素对过氧化氢分解速率的影响。
②上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响 。
(Ⅱ)将质量相同但聚集状态不同的MNO2分别加入到5mL 5%的双氧水中,并用带火星的木条测试。测定结果如下:
| 催化剂(MNO2) |
操作情况 |
观察结果 |
反应完成所需的时间 |
| 粉末状 |
混合 不振荡 |
剧烈反应,带火星的木条复燃 |
3.5分钟 |
| 块状 |
反应较慢,火星红亮但木条未复燃 |
30分钟 |
①写出H2O2发生的化学反应方程式 。
②实验结果说明催化剂作用的大小与 有关。
某课外学习小组在学习了Na2O2与CO2的反应后,认为Na2O2与SO2应该也可以反应。他们设计了下图装置(夹持装置已略去,装置的气密性良好)进行实验,探究SO2与Na2O2反应的产物,请按要求回答下列问题。
Ⅰ﹒写出装置A中发生反应的化学方程式:___________________________
Ⅱ﹒装置D的作用:除了可以防止空气中的CO2、水蒸气等进入C中与Na2O2反应,还可以_____________
Ⅲ﹒在通入足量的SO2与Na2O2充分反应后,他们对C中固体产物提出如下假设:
假设1:只有Na2SO3;
假设2:_________;
假设3:既有Na2SO3,又有Na2SO4。
(1)若假设1成立,写出SO2与Na2O2反应的化学方程式:________________
(2)为进一步确定C中反应后固体产物的成分(Na2O2已反应完全),甲同学设计了如下实验:
甲同学由此得出结论:产物是Na2SO4,该方案是否合理______(填“是”或“否”),理由是_____________
(3)乙同学设计了如下实验验证假设3成立,请帮助他完成下表。
| 实验步骤 |
现象 |
| ①取少量C中固体产物于试管中,加入适量的蒸馏水溶解。 |
固体全部溶解 |
| ②向上试管中加入过量的_____________,将产生的气体通入少量酸性KMnO4溶液中。 |
KMnO4溶液__________ |
| ③向步骤②反应后的试管中,加入适量的BaCl2溶液。 |
产生白色沉淀 |
步骤②中将产生的气体通入少量酸性KMnO4溶液中,发生反应的离子方程式为:__________
某化学兴趣小组利用如下图装置验证元素非金属性的变化规律。
(1)仪器A的名称为________,干燥管D的作用是________。
(2)实验室中现有药品KMnO4、MnO2、浓盐酸、Na2S,请选择合适药品设计实验验证非金属性:Cl>S,装置A、B、C中所装药品应分别为浓盐酸、________、Na2S溶液,装置C中的实验现象为有淡黄色沉淀生成,装置C中发生反应的离子方程式为____________。
(3)若利用上装置证明非金属性:S>C>Si。在A中加入稀硫酸、B中加入Na2CO3溶液、C中加入Na2SiO3溶液,观察到B中产生气泡,试管C中出现________现象,则可以证明非金属性:S>C>Si。
若将A中的稀硫酸改为稀盐酸,试管C中会出现同样的现象,是否可以得出结论:非金属性Cl>C>Si?__________(填“是”或“否”),你的理由是______________________。
草酸亚铁和草酸铁常用作照相显影剂或制药工业。I.某化学兴趣小组的同学进行草酸亚铁晶体(FeC2O4·2H2O)分解产物的实验探究。他们设计了如下装置进行实验(夹持装置未画出),干燥管B、G中装有无水氯化钙,试管D、F、I中盛有澄清石灰水。
(1)烧瓶A中盛有饱和NH4C1和饱和NaNO2的混合液,常用于实验室制N2,则该反应的化学方程式为_____________________________。
(2)实验时先打开活塞a,并加热烧瓶A一段时间,其目的是___________________。
(3)①试管D中出现浑浊,证明分解产物中有____________存在。
②证明分解产物中存在CO的现象是______________________________。
③要证明分解时产生的另一种气态产物的存在,应该如何改进装置______________。
④将C中充分反心后的固体残余物投入经煮沸的稀硫酸中,固体完全溶解且无气体放出,取反应液加入KSCN溶液无血红色,证明固体产物为_____________(填化学式)。
II.三氯化铁是合成草酸铁的重要原料。已知草酸铁晶体在低温时溶解度较小。
(4)利用工业FeCl3(含杂质)制取纯净的草酸铁晶体【Fe2(C2O4)3·5H2O】的实验流程如下图所示:
①溶液X为浓盐酸,目的是_________________。
②上述流程中FeCl3可用异内醚萃取,其原因是__________________。
③所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是___________________。
④为测定所得草酸铁晶体的纯度,实验室中用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于__________(填“酸式”或“碱式”)滴定管中。
有关铝的几个实验如下。请填写下列空白。
实验一 毛刷实验
实验过程如下图。
(1)配制Hg(NO3)2溶液时,为抑制水解,需加入少量的_____。
(2)铝导线放NaOH溶液的目的是除去表面的氧化膜,其化学方程式为_____。
(3)生成白色毛状物的实质是铝发生电化腐蚀生成A12O3,其中作正极材料的是______ (填序号)。
a.O2 b.A1 c.Hg(NO3)2 d.Hg
实验二 探究白色毛状物是否含有结晶水
取适量白色毛状物样品放入仪器X称量,质量为m1 g
(4)仪器X应选用以下哪个装置____________________(填名称)。
(5)上述过程中“冷却"时要在图1所示的装置中进行的原因是______________________.
(6)根据所得实验资料,能说明白色毛状物含结晶水的证据是_________(用代数式表示)。
实验三 验证A12O3对石蜡油裂解的催化作用
按图2连好装置,检查装置的气密性,加入5~6 g Al2O3,加热到500℃左右,往Al2O3上滴入石蜡油。已知:石蜡油为液态烷烃混合物(与汽油类似),沸点164~223 ℃。
一定条件下,其裂解产物为乙烯和烷烃的混合物。
(7)使用装置B的目的是___________________。
(8)需要再补充一个实验才能证明Al2O3对石蜡油裂解反应有催化作用,请简述其实验方案:__________。
(15分)节日期间因燃放鞭炮会引起空气中SO2含量增高,造成大气污染。实验小组同学欲测定空气中SO2的含量,并探究SO2的性质。
I.某实验小组同学拟用下图所示简易装置测定空气中SO2的含量。
实验操作如下:按图连接好仪器,检查装置气密性后,在广口瓶中盛放足量的H2O2水溶液,用规格为20mL的针筒抽气100次,使空气中的SO2被H2O2水溶液充分吸收(SO2+ H2O2=H2S04)。在吸收后的水溶液中加入足量的BaCl2溶液,生成白色沉淀,经过滤、洗涤、干燥等步骤后进行称量,得白色固体0.233mg。
(1)计算所测空气中SO2含量为_______mg·L-1。
(2)已知常温下BaS03的Ksp为5.48x10-7,饱和亚硫酸溶液中c(S032-)=6.3x10-8{mol·L-1。
有同学认为以上实验不必用H2O2吸收SO2,直接用O.1mol·L-1BaCl2溶液来吸收S02即可产生沉淀。请用以上数据分析这样做是否可行________________.
U.另一实验小组同学依据SO2具有还原性,推测SO2能被C12氧化生成SO2C12。
用如图所示装置收集满C12,再通入SO2,集气瓶中立即产生无色液体,充分反应后,将液体和剩余气体分离,进行如下研究。
(3)写出二氧化锰和浓盐酸反应制取氯气的离子方程式____________________.
(4)研究反应的产物。向所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有S042-、C1-,证明无色液体是SO2C12。
写出SO2C12与H2O反应的化学方程式_______________________________________.
(5)研究反应进行的程度。用NaOH溶液吸收分离出的气体,用盐酸酸化后,再滴加BaCl2溶液。产生白色沉淀。
①该白色沉淀的成分是_____________.
②SO2和C12生成SO2C12的反应________可逆反应(填“是”或“不是”),阐述理由___________.
(14)铬是一种银白色金属,化学性质稳定,以+2、+3和+6价为常见价态。工业上以铬铁矿(主要成分为FeO·Cr2O3 ,含有Al2O3、SiO2等杂质)为主要原料生产金属铬和重铬酸钠Na2Cr2O7·2H2O(已知Na2Cr2O7是一种强氧化剂),其主要工艺流程如下:
查阅资料得知:
①常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-
②常温下,Ksp[Cr(OH)3]=6.3×10-31
回答下列问题:
(1)工业上常采用热还原法制备金属铬,写出以Cr2O3为原料,利用铝 热反应制取金属铬的化学方程式 。
(2)酸化滤液D时,不选用盐酸的原因是 。
(3)固体E的主要成分是Na2SO4,根据下图分析操作a为 、 。
(4)已知含+6价铬的污水会污染环境。电镀厂产生的镀铜废水中往往含有一定量的Cr2O72-,处理该废水常用还原沉淀法,具体流程如下:
①Cr(OH)3的化学性质与Al(OH)3相似。在上述生产过程中加入NaOH溶液时要控制溶液的pH不能过高,是因为 ;
②下列溶液中可以代替上述流程中Na2S2O3溶液的是 (填选项序号);
| A.FeSO4溶液 | B.浓H2SO4 | C.酸性KMnO4溶液 | D.Na2SO3溶液 |
③调整溶液的pH=5时,通过列式计算说明溶液中的Cr3+是否沉淀完全 ;
④上述流程中,每消耗0.1molNa2S2O3转移0.8mole-,则加入Na2S2O3溶液时发生反应的离子方程式为 。
工业生产中会产生大量的废铁屑,可将其“变废为宝”制成化工原料氯化铁。实验室中利用下图所示装置探究由废铁屑制备FeCl3·6H2O晶体的原理并测定铁屑中铁单质的质量分数(杂质不溶于水且不与酸反应)。
(1)装置A的名称为 。
(2)检验该装置气密性的具体操作如下:
①关闭 ;打开弹簧夹K1;
②向水准管中加水,使水准管液面高于量气管液面;
③ 。
取m g废铁屑加入B装置中,在A中加入足量的盐酸后进行下列操作:
Ⅰ.打开弹簧夹K1,关闭活塞b,打开活塞a,缓慢滴加盐酸。
Ⅱ.当装置D的量气管一侧液面不再下降时,关闭弹簧夹K1,打开活塞b,当A中溶液完全进入烧杯后关闭活塞a、b。
Ⅲ.将烧杯中的溶液经过一系列操作后得到FeCl3·6H2O晶体。
请回答:
(3)用离子方程式表示烧杯中足量的H2O2溶液的作用: 。
(4)实验结束后,量气管和水准管内液面高度如上图所示,为了使两者液面相平,应将水准管 (填“上移”或“下移”)。
(5)由FeCl3溶液制得FeCl3•6H2O晶体的操作过程中不需要使用的仪器有 (填选项序号)。
a.蒸发皿
b.烧杯
c.酒精灯
d.分液漏斗
e.坩埚
f.玻璃棒
g.漏斗
(6)实验结束后,若量气管内共收集到VmL气体(已换算成标准状况),则此废铁屑中铁单质的质量分数为 。
某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。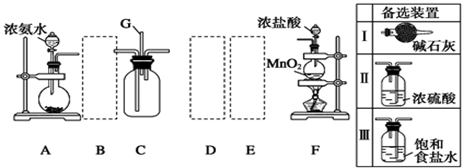
请回答下列问题:
(1)装置F中发生反应的离子方程式:________________________________________。
(2)装置A中的烧瓶内固体可选用_________(选填以下选项的代号)。
A.碱石灰
B.生石灰
C.二氧化硅
D.五氧化二磷
E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择,并将编号填入下列空格:B ,D___________,E 。(均填编号)
(4)通入C装置的两根导管左边较长、右边较短,目的是__ 。
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.请写出反应的化学方程式:___ ;其中氧化剂与还原剂的物质的量之比为 ;当a mol氯气参加反应时,转移的电子总数为b个,则阿伏加德罗数常数为 mol-1(用含a、b的代数式表示);
(6)从装置C的出气管口处逸出的尾气可能含有污染环境的气体,如何处理? 。