下列事实不能用电化学理论解释的是
| A.轮船水线以下的船壳上镶嵌有一定量的锌块 |
| B.黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| C.锌跟稀硫酸反应制取氢气,加入少量硫酸铜能加快反应速率 |
| D.铝在空气中不易腐蚀,不用特殊方法保存 |
如图,缠上金属条的铁钉插在含有酚酞的NaCl溶液中,可以看到在金属条表面的溶液出现粉红色。该金属条可能是 ( )。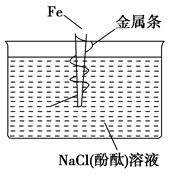
| A.铜 | B.镁 | C.铝 | D.锌 |
以油类为溶剂的防锈漆称为油基防锈漆,由于环保方面的原因,目前要推广使用水基防锈漆,但水基漆较易溶解O2,在干燥之前易导致金属表面产生锈斑,为此要在水基漆中加入缓蚀剂以除去氧气,以下可作为缓蚀剂的是( )
| A.KMnO4 | B.NaNO2 | C.FeCl3 | D.HNO3 |
我国某大城市今年夏季多次降下酸雨。据环保部门测定,该城市整个夏季酸雨的pH平均为3.2。在这种环境中的铁制品极易被腐蚀。对此条件下铁的腐蚀的叙述不正确的是
| A.此腐蚀过程有化学腐蚀也有电化学腐蚀 |
| B.发生电化学腐蚀时的正极反应为2H2O+O2+4e-=4OH- |
| C.在化学腐蚀过程中有氢气产生 |
| D.发生电化学腐蚀时的负极反应为Fe=Fe2++2e- |
下列物质的有关事实与电化学腐蚀无关的是
| A.轮船水线以下的船壳上镶嵌有一定量的锌块 |
| B.镀锌的铁制品比镀锡的铁制品耐用 |
| C.埋在潮湿疏松土壤里的铁管比干燥致密不透气的土壤里的铁管更易被腐蚀 |
| D.在空气中,金属镁、铝的表面可形成一层氧化膜 |
建筑用的钢材在出厂前都要经过烤蓝处理,使其表面生成一层四氧化三铁,其目的是
| A.增加钢材的硬度 | B.增强钢材的抗腐蚀能力 |
| C.使钢材美观 | D.增加钢材的韧性 |
钢铁发生电化腐蚀时,正极上发生的反应是
| A.2H++2e-=H2↑ | B.2H2O+O2+4e-=4OH- |
| C.Fe-2e-=Fe2+ | D.4OH--4e-=O2↑+2H2O |
下列对金属及其制品的防护措施中,错误的是
| A.把Cr、Ni等金属加入到普通钢里制成不锈钢铁 |
| B.通过特殊工艺,增加铝制品表面的氧化膜 |
| C.对于易生锈的铁制品要定期刷防护漆 |
| D.锅用完后,用水刷去其表面的油污,置于潮湿处 |
下列拟采用的金属防腐措施,错误的是
| A.给金属衣架或电线外面包上一层塑料层 |
| B.给自行车钢圈镀上一层金属铬 |
| C.在轮船的外表面焊上一些铜块 |
| D.给铁栅栏表面涂上一层油漆 |
钢铁发生吸氧腐蚀时,正极上发生的电极反应是
A.2H++2e-  H2 H2 |
B.Fe2++ 2e- Fe Fe |
C.2H2O+O2+4e-  4OH- 4OH- |
D.Fe3++e-  Fe2+ Fe2+ |
有关金属腐蚀的叙述正确的是
| A.生铁抗腐蚀能力比纯铁强 |
| B.钢瓶在储存液氯前彻底干燥可减缓腐蚀 |
| C.水库铁闸与直流电源正极相连可减缓腐蚀 |
| D.常温下浓硝酸比浓盐酸更易使铁腐蚀 |
下列说法正确的是
| A.工业上用电解MgCl2溶液的方法制备金属Mg |
| B.在潮湿的空气中,生铁比纯铁更耐腐蚀 |
| C.向鸡蛋清中加入饱和的CuSO4或(NH4)2SO4溶液均产生沉淀,两者原理相同 |
| D.往沸水中滴入饱和的FeCl3溶液,继续煮沸至液体呈透明的红褐色,可制得Fe(OH)3胶体 |
据环保部门测定,我国一些大城市的酸雨pH=3.5。在酸雨季节铁制品极易腐蚀,则在其腐蚀中负极主要发生的反应是
| A.2H++2e-=H2↑ | B.2H2O+O2+4e-=4OH- |
| C.Fe-2e-=Fe2+ | D.4OH--4e-=2H2O+O2↑ |
如图所示各容器中盛有海水,铁在其中被腐蚀由快到慢的顺序是( )

| A.④>②>①>③ | B.②>①>③>④ |
| C.④>②>③>① | D.③>②>④>① |