已知A、B为单质,C为化合物。则下列说法正确的是( )
A+B C
C C溶液
C溶液 A+B
A+B
①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液遇Na2CO3放出CO2气体,则A可能是H2
③若C溶液中滴加KSCN溶液显血红色,则B可能为Fe
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.①② B.③④ C.①③ D.②④
用一种阴、阳离子双隔膜三室电解槽处理废水中的NH4+,模拟装置如图所示。下列说法正确的是
| A.阳极室溶液由无色变成棕黄色 |
| B.阴极的电极反应式为:4OH–-4e–=2H2O+O2↑ |
| C.电解一段时间后,阴极室溶液中的pH升高 |
| D.电解一段时间后,阴极室溶液中的溶质一定是(NH4)3 PO4 |
下列有关实验装置进行的相应实验,能达到实验目的的是( )
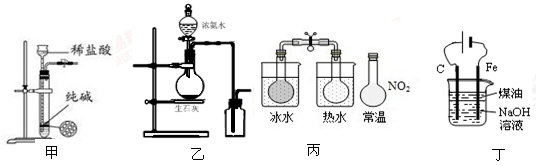
| A.用图甲所示装置控制制取少量的CO2气体 |
| B.用图乙所示装置制取并收集氨气 |
C.用图丙所示装置可以说明反应2NO2(g) N2O4(g)是放热反应 N2O4(g)是放热反应 |
| D.用图丁所示装置可制备Fe(OH)2并能较长时间观察其颜色 |
关于下列各装置图的叙述中,不正确的是
| A.装置①中,d为阳极,c为阴极 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、HC1、NO2等气体 |
| C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
| D.装置④可用于干燥、收集氨气,并吸收多余的氨气 |
下列实验能达到预期目的的是( )
| A.滴定管洗净后,直接注入标准液进行滴定 |
| B.用石墨作电极,电解Mg(NO3)2和Cu(NO3)2的混合溶液,确定铜和镁的金属活动性强弱 |
| C.称取19.0g氯化亚锡(SnC12),用蒸馏水溶解,定容至100mL,配制1.0mol/L SnC12溶液 |
| D.测定NaC1和NaF溶液的pH,确定F、C1两元素非金属性的强弱 |
下列有关化工生产的叙述中,正确的是
| A.工业上可用氯化钠制备化肥NH4Cl |
| B.氯碱工业中,电解槽的阳极区产生NaOH |
| C.在接触室被氧化成SO3,SO3在吸收塔内被水吸收制成浓硫酸 |
| D.工业上用石英制太阳能电池,在高温下用铝热法炼铁制备钢材 |
关于下列装置的说法正确的是

① ②
| A.①中盐桥内的K+移向CuSO4溶液 |
| B.①将电能转变为化学能 |
| C.若②用于铁棒镀铜,则N极为铁棒 |
| D.若②用于电解精炼铜,溶液中的Cu2+浓度保持不变 |
将含有0.4 mol NaCl和0.5 mol Cu(NO3)2的水溶液用惰性电极电解一段时间后,在一个电极上得到0.3 mol Cu,则在另一个电极上逸出的气体(标准状况下)的体积是
| A. 4.48 L | B. 5.6L | C. 6.72L | D. 11.2L |
金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍。电解时,下列有关叙述正确的是(已知氧化性Fe2+<Ni2+<Cu2+)
| A.阳极发生还原反应,其电极反应式:Ni2+ + 2e— = Ni |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C.电解后,溶液中存在的金属阳离子只有Fe2+ 和Zn2+ |
| D.电解后,电解槽底部的阳极泥中只有Cu和Pt |
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是
| A.铁是阳极,电极反应为Fe-6e-+4H2O=FeO42-+ 8H+ |
| B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极 |
| C.若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计) |
将含有0.400molCuSO4和0.200molFeCl3的水溶液1L,用惰性电极电解一段时间后,在一个电极上析出19.2gCu,此时在另一电极上放出的气体在标准状况下的体积为
| A.5.60L | B.6.72L | C.4.48L | D.7.84L |
下列说法正确的是
①实验室里需要480 mL 2.0 mol/L的氢氧化钠溶液,配制溶液时先称量氢氧化钠固体38.4 g,然后再按照溶解、冷却、洗涤、定容、摇匀的步骤进行操作
②用标准盐酸滴定NaOH溶液测其浓度时,酸式滴定管用蒸馏水洗涤后,没用标准盐酸润洗,直接装标准盐酸滴定,所测的碱液浓度偏低
③自发反应在恰当条件下才能实现
④钢铁腐蚀时可能发生的正极反应:2H2O+O2+4e-=4OH-
⑤电解饱和MgCl2溶液时,电解反应式为:2H2O+2Cl- Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
⑥在海轮外壳连接锌块保护外壳不受腐蚀是采用牺牲阳极的阴极保护法
⑦长期使用硫酸铵,土壤酸性增强:草木灰与铵态氮肥不能混合施用
| A.①②⑤⑥ | B.①③⑤⑦ | C.③④⑥⑦ | D.②③④⑤ |
下列说法不正确的是
| A |
B |
C |
D |
| 通电一段时间后, 搅拌均匀,溶液的 pH增大 |
甲电极上的电极反应为: 2Cl--2e-= Cl2↑ |
Pt电极上的电极反应为: O2+2H2O+4e-==4OH- |
总反应的离子方程式 为:2Fe3++Cu=Cu2++ 2Fe2+ |
 |
 |
 |
 |
某兴趣小组设计如下微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl-  Cl2↑+H2↑ Cl2↑+H2↑ |
| B.断开K2,闭合K1时,石墨电极附近溶液变红 |
| C.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e-=2Cl- |
| D.断开K1,闭合K2时,石墨电极作正极 |