将 0.1 L 含有 0.02mol CuSO4和 0.01molNaCl 的水溶液用惰性电极电解。电解一段时间后,一个电极上得到 0.01 mol Cu,另一电极析出的气体( )
| A.只有Cl2 | B.既有Cl2又有O2 | C.只有O2 | D.只有H2 |
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电电解一段时间。假设在电解过程中产生的气体全部逸出,下列说法正确的是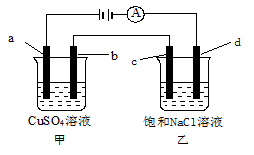
| A.甲、乙两烧杯中溶液的pH均保持不变 |
| B.当b极增重3.2 g时,d极产生的气体为0.56 L(标准状况) |
| C.当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 |
| D.甲烧杯中a电极反应式为:4OH--4e-===O2↑+2H2O |
下列各组中,每种电解质溶液电解时只生成氢气和氧气的是
| A.NaOH、H2SO4、Ba(OH)2 | B.NaOH、CuSO4、H2SO4 |
| C.HCl、CuCl2、Ba(OH)2 | D.NaBr、H2SO4、Ba(OH)2 |
右图是一款笔记本电脑所用甲醇燃料电池的结构示意图。

甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2 = 2CO2+4H2O 下列说法正确的是( )
| A.右电极为电池的正极,b处通入的物质是空气 |
| B.左电极为电池的负极,a处通入的物质是空气 |
| C.正极反应式为:CH3OH+H2O-6e-= CO2+6H+ |
| D.正极反应式为:O2+2H2O+4e-=4OH- |
下列说法正确的是:
| A.工业上常使用电解精炼法将粗铜提纯,在电解精练时,阳极减少的质量等于阴极增加的质量 |
| B.心脏起搏器中使用的新型Li-I2电池的寿命已超过10年,其反应可简单表示为2Li+I2=2LiI,阴极反应为:2Li-2e-=2Li+ |
| C.为了降低某水库的铁闸门被腐蚀的速率,其中焊接在铁闸门上的金属材料可以是锌 |
| D.某物质的溶解度为难溶,则该物质不溶于水 |
甲、乙两个电解池均以Pt为电极,且互相串联。甲池盛有CuSO4溶液,乙池中盛有一定量的某盐溶液。通电一段时间后,测得甲池电极质量增加0.64g,乙池电极上析出0.24 g金属,则乙池中的溶质可能是
| A.MgSO4 | B.Al(NO3)3 | C.CuSO4 | D.Na2SO4 |
将0.1 mol AgNO3和0.2mol Cu(NO3)2固体溶于水配成100 mL溶液,用惰性电极电解一段时间后,在一极上析出0.15 mol O2,此时,另一极上析出的气体体积(标准状况)为( )
| A.1.12L | B.2.24 L | C.3.36 L | D.4.48L |
按图甲装置进行实验,若图乙中横坐标x表示通过电极的电子的物质的量,下列叙述正确的是 ( )
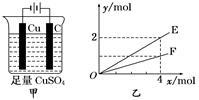
| A.电解过程中,Cu2+浓度不变 |
| B.E表示反应生成O2的物质的量 |
| C.电解过程中,石墨棒附近溶液的pH有所增大 |
| D.若向烧杯中加入2 mol CuO可以使电解质恢复到电解前的浓度,则电解过程中共转移了4mol电子。 |
用a、b两个质量相等的Pt电极电解AlCl3和CuSO4的混合溶液[ n(AlCl3) : n(CuSO4) = 1:9 ]。 t1时刻a电极得到混合气体,其中Cl2在标准状况下为224 mL(忽略气体的溶解);t2时刻Cu全部在电极上析出。下列判断正确的是
| A.a电极与电源的负极相连 |
| B.t2时,两电极的质量相差3.84g |
| C.电解过程中,溶液的pH不断增大 |
| D.t2时,b的电极反应是4OH――4e-=2H2O+O2↑ |
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如右图所示,下列说法中不正确的是
| A.A为电源正极 |
| B.阴极区附近溶液pH降低 |
| C.阳极区溶液中发生的氧化还原反应为Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++7H2O |
| D.若不考虑气体的溶解,当收集到H2 13.44 L(标准状况)时,有0.1 mol Cr2O72-被还原 |
已知某碱性硼化钒(VB3)一空气电池工作时发生反应为:11O2+4VB2=2V2O5+4B2O3。以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
| A.VB2电极发生的电极反应为:2VB2+11H2O-22e-=V2O5+2B2O3+22H+ |
| B.若B装置内的液体体积为400mL,则CuSO4溶液的物质的量浓度为0.025mol/L |
| C.电解过程中,b电极表面先有红色物质析出,然后有气泡产生 |
| D.外电路中电子由a电极流向b电极 |
为增强铝的耐腐蚀性,现以铅蓄电池为外接电源,以A1作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O Al2O3+3H2↑,在电解过程中,以下判断正确的是
Al2O3+3H2↑,在电解过程中,以下判断正确的是
下列有关电化学装置的说法正确的是
| A.利用图a装置处理银器表面的黑斑Ag2S,银器表面的反应为Ag2S+2e-=2Ag+S2- |
| B.图b电解一段时间,铜电极溶解,石墨电极上有亮红色物质析出 |
| C.图c中的X极若为负极,则该装置可实现粗铜的精炼 |
| D.图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀 |
用碱性氢氧燃料电池为电源进行电解的实验装置示意图如下所示。下列说法中正确的是
| A.燃料电池工作时,负极反应为:H2-2e- = 2H+ |
| B.若要实现铁上镀铜,则a极是铁,b极是铜 |
| C.若a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下当电池中消耗H222.4L(标准状况)时,a极析出铜64g |