用惰性电极电解200mL一定浓度的硫酸铜溶液,实验装置如图①所示,如果向所得的溶液中加入0.1molCu(OH)2后,使溶液恰好恢复到电解前的浓度和pH,电解过程中转移的电子为( )

| A.0.2mol | B.0.4mol | C. 0.6mol | D.0.8mol |
在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是
| A.X是电源的负极 |
| B.阴极的反应式是:H2O+2eˉ=H2+O2ˉCO2+2eˉ=CO+O2ˉ |
C.总反应可表示为:H2O+CO2 H2+CO+O2 H2+CO+O2 |
| D.阴、阳两极生成的气体的物质的量之比是1︰1 |
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以A1作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O Al2O3+3H2↑ 电解过程中,以下判断正确的是( )
Al2O3+3H2↑ 电解过程中,以下判断正确的是( )

将0.2molAgNO3、0.4molCu(NO3)2、0.6molKCl溶于水,配成100mL溶液,用惰性电极电解一段时间后,若在一极析出0.3molCu,此时在另一极上产生的气体体积(标准状况)为
| A.3.36L | B.4.48L | C.5.6L | D.6.72L |
下图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5 mol·L -1,工作一段时间后,测得有0.02 mol电子通过,若忽略溶液体积的变化,下列叙述正确的是
| A.产生气体体积 ①=② |
| B.①中阴极质量增加,②中正极质量减小 |
| C.电极反应式:①中阳极:4OH- - 4e- = 2H2O+O2 ↑ ②中负极:2H + +2e-=H2 ↑ |
| D.溶液的pH变化:①减小,②增大 |
用惰性电极电解一定量的硫酸铜溶液,实验装置如图甲。电解过程中的实验数据如下图乙,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况下)。则下列说法不正确的是( )

| A.电解过程中,a电极表面先有红色物质析出,后有气泡产生 |
| B.b电极上发生反应的方程式为:4OH--4e-=2H2O+O2↑ |
| C.曲线O~P段表示氧气的体积变化 |
| D.从开始到Q点时收集到的混合气体的平均摩尔质量为12g/mol |
用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是
| A.用石墨作阳极,铁作阴极 |
| B.阳极的电极反应式为:Cl-+ 2OH--2e-= ClO-+ H2O[ |
| C.阴极的电极反应式为:2H2O + 2e- = H2↑ + 2OH- |
| D.除去CN-的反应:2CN-+ 5ClO-+2H+ =N2↑+2CO2↑+5Cl-+H2O |
一些科学家采用高质子导电性的SCY陶瓷(能传递H+),实现了氨的电化学合成。该过程N2和H2的转化率远高于现在工业上使用的氨合成法。对于电化学合成氨的有关叙述正确的是
| A.N2在阴极上被氧化 |
| B.可选用铁作为阳极材料 |
| C.阳极的电极反应式是N2+6e-+6H+ = 2NH3 |
D.该过程的总反应式是N2+3H2 2NH3 2NH3 |
观察下列几个装置示意图,有关叙述不正确的是( )

| A.装置①中阴极上析出红色固体 |
| B.装置②的待镀铁制品应与电源负极相连 |
| C.装置③中a为负极,发生的电极反应式为H2+2OH﹣+2e﹣=2H2O |
| D.装置④中在阴极可以得到氢气和氢氧化钠,离子交换膜可选用阳离子交换膜 |
如图是乙醇燃料电池的实验装置图,下列有关说法一定正确的是
| A.若用此装置给铁棒上镀上层银,则N电极改用铁电极,M电极改用银电极 |
| B.甲池中负极的电极反应式为:CH3CH2OH-12e-+3H2O=2CO2+12H+ |
| C.甲池KOH溶液中经过0.05mol电子时,理论上乙池中的M电极质量增加5.40g |
| D.M电极上的电极反应式为:Ag++e-=Ag |
已知某碱性硼化钒(VB3)一空气电池工作时发生反应为:11O2+4VB2=2V2O5+4B2O3。以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
| A.VB2电极发生的电极反应为:2VB2+11H2O-22e-=V2O5+2B2O3+22H+ |
| B.若B装置内的液体体积为400mL,则CuSO4溶液的物质的量浓度为0.025mol/L |
| C.电解过程中,b电极表面先有红色物质析出,然后有气泡产生 |
| D.外电路中电子由a电极流向b电极 |
有关下列电化学装置的说法中正确的是( )

| A.图a是原电池装置,可以实现化学能转化为电能 |
| B.图b电解一段时间后,加入适量CuO固体,可以使硫酸铜溶液恢复到原浓度 |
| C.图c中的X极若为负极,则该装置可实现粗铜的精炼 |
| D.图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀 |
我国科学家最新研发的固体透氧膜提取金属钛工艺,其电解装置如右图所示:将TiO2熔于NaCl-NaF融盐体系,以石墨为阴极,覆盖氧渗透膜的多孔金属陶瓷涂层为阳极,固体透氧膜把阳极和熔融电解质隔开,只有O2-可以通过。下列说法不正确的是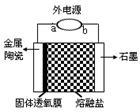
| A.a 极是电源的正极,O2-在熔融盐中从右往左迁移 |
| B.阳极电极反应式为2O2--4e- = O2↑ |
| C.阳极每产生4.48L的O2,理论上能生成0.2mol钛 |
| D.NaCl-NaF融盐的作用是降低熔化TiO2需要的温度 |
在1LK2SO4和CuSO4的混合溶液中,c(SO42-)="2.0" mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L(标准状况)气体,则原溶液中K+的物质的量浓度为
| A.2.0 mol·L-1 |
| B.1.5 mol·L-1 |
| C.1.0 mol·L-1 |
| D.0.5 mol·L-1 |