在一定温度下,向AgI的饱和溶液中:(填“增大”、“减小”或“不变”)
(1)若加入AgNO3固体,c(I-) 。
(2)若加入更多的AgI固体,则c(Ag+) 。
(3)若加入固体AgBr,c(I-) 。
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
提示:BaSO4(s)  Ba2+(aq)+SO42- (aq)的平衡常数Ksp=c(Ba2+)•c(SO42-),称为溶度积常数。
Ba2+(aq)+SO42- (aq)的平衡常数Ksp=c(Ba2+)•c(SO42-),称为溶度积常数。
| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.d点无BaSO4沉淀生成 |
| D.a点对应的Ksp大于c点对应的Ksp |
在含有浓度均为0.01mol•L-1的Cl-、Br-、I-离子的溶液中,缓慢加入AgNO3稀溶液,析出三种沉淀的先后顺序是( )
| A.AgCl、AgBr、AgI | B.AgI、AgBr、AgCl |
| C.AgBr、AgCl、AgI | D.三种沉淀同时析出 |
某温度下向100g澄清的饱和石灰水中加入5.6g生石灰,充分反应后恢复原来的温度.下列叙述正确的是( )
| A.沉淀物的质量为5.6g |
| B.沉淀物的质量为7.4g |
| C.饱和石灰水的质量大于98.2g |
| D.饱和石灰水的质量小于98.2g |
下列叙述不正确的是( )。
| A.向Mg(OH)2悬浊液中加少量NH4Cl固体,溶液变澄清 |
| B.向AgI在水中的平衡体系中加入Na2S溶液沉淀会转化为黑色 |
| C.用水洗涤BaSO4比用稀硫酸洗涤损失的沉淀要少 |
| D.MgCO3在水中加热可以转化为Mg(OH)2 |
已知:室温时,Ksp(AgCl)= 1.8×10-10mol2·L-2。请回答:
(1)饱和AgCl溶液的浓度是 mol/L。
(2)将2.0×10-5mol·L-1的AgNO3溶液与2.0×10-5mol·L-1的NaCl溶液等体积混合则混合后C(Ag+)= ,Qc= , 因为Qc Ksp(填“>”或“<”),所以 (填“有”或“无”)AgCl沉淀析出。
下列关于沉淀溶解平衡的说法正确的是( )
| A.只有难溶电解质才存在沉淀溶解平衡过程 |
| B.沉淀溶解平衡过程是可逆的 |
C.在平衡状态时 |
| D.达到沉淀溶解平衡的溶液不一定是饱和溶液 |
向50 mL 0.018 mol/L的AgNO3溶液中加入50 mL 0.02 mol/L的盐酸生成沉淀。已知:Ksp(AgCl)=1.8×10-10 mol2·L-2,则生成沉淀后的溶液中c(Ag+)与pH分别为
| A.1.8×10-7 mol/L,2 | B.1×10-7 mol/L,2 | C.1.8×10-7 mol/L,3 | D.1×10-7 mol/L,3 |
[2012·安徽卷] 已知室温下,Al(OH)3的Ksp或溶解度远大于Fe(OH)3。向浓度均为0.1 mol·L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。下列示意图表示生成Al(OH)3的物质的量与加入NaOH溶液的体积的关系,合理的是( )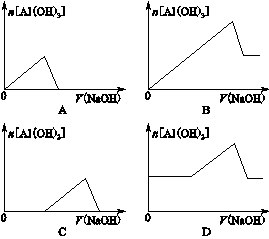
海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案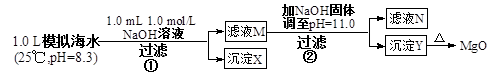
| 模拟海水中的 离子浓度(mol/L) |
Na+ |
Mg2+ |
Ca2+ |
Cl― |
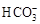 |
| 0.439 |
0.050 |
0.011 |
0.560 |
0.001 |
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;
实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;
Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12。
下列说法正确的是( )
A.沉淀物X为CaCO3
B.滤液M中存在Mg2+,不存在Ca2+
C.滤液N中存在Mg2+、Ca2+
D.步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
已知[Ksp(AgBr) ]=5.4×10-13,[Ksp(AgCl) ]=2.0×10-10。
(1)向浓度均为0.1mol·L-1的KBr、NaCl混合溶液中滴入0.1mol·L-1的AgNO3溶液,首先生成的沉淀是 。
(2)当容器中同时出现AgCl和AgBr沉淀,溶液中c(Br-)/c(Cl-)= 。
在一定温度下,硫酸铜晶体的培养皿中存在下列平衡: Cu2++SO42-+x H2O  CuSO4·xH2O,当向硫酸铜溶液中加少量无水硫酸铜粉末后,下列说法中正确的是
CuSO4·xH2O,当向硫酸铜溶液中加少量无水硫酸铜粉末后,下列说法中正确的是
| A.溶液中Cu2+浓度增大 | B.溶液中Cu2+数目减少 |
| C.该硫酸铜晶体体积增大 | D.溶液的蓝色变浅 |
在下列溶液中,BaSO4的溶解度最大的是( )
| A.1 mol/L H2SO4溶液 | B.2 mol/L Na2SO4溶液 |
| C.0.1 mol/L BaCl2溶液 | D.纯水 |
下列说法正确的是
| A.在一定温度下AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数; |
| B.AgCl的Ksp = 1.8×10-10,在任何含AgCl固体的溶液中,c(Ag+) = c(Cl-)且Ag+与Cl-浓度的乘积等于1.8×10-10; |
| C.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液; |
| D.向饱和AgCl水溶液中加入盐酸,Ksp值变大。 |