2013届新课标高三配套月考(四)化学试卷(B卷)
[2012·山东卷] 下列实验操作正确的是( )
| A.中和滴定实验时,用待测液润洗锥形瓶 |
| B.盛放NaOH溶液时,使用带玻璃塞的磨口瓶 |
| C.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| D.NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 |
[2012·德州一模] 下列关于有机物的叙述不正确的是( )
| A.油脂在空气中完全燃烧生成二氧化碳和水 |
| B.蛋白质溶液中加入浓的硫酸铵溶液会发生盐析 |
| C.乙酸乙酯中混有的乙酸杂质可以用饱和碳酸钠溶液除去 |
D.由CH2=CH—COOCH3合成的聚合物为 |
[2012·临沂一模]实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )
| A.装置①:常用于分离互不相溶的液体混合物 |
| B.装置②:可用于吸收NO2或HCl气体,并防止倒吸 |
| C.装置③:先从b口进气集满二氧化碳,再从a口进气,可收集一氧化氮 |
| D.装置④:可用来证明碳的非金属性比硅强 |
[2012·淮安二模]下列有关实验原理或实验操作正确的是( )
| A.在蒸发皿中灼烧CuSO4·5H2O晶体以除去结晶水 |
| B.用量筒量取20 mL 0.500 0 mol·L-1 H2SO4溶液于烧杯中,加水80 mL,配制成0.100 0 mol·L-1 H2SO4溶液 |
| C.实验室用图甲所示的装置制取少量氨气 |
| D.实验室用图乙所示的装置除去Cl2中的少量HCl |
[2012·泉州第二质检] 下列实验操作或装置符合实验目的的是( )
| 选项 |
A |
B |
C |
D |
| 目的 |
用酸性KMnO4溶液滴定Na2SO3溶液 |
配制稀硫 酸溶液 |
在铁制品上镀铜 |
检查装置 气密性 |
| 装置 或 操作 |
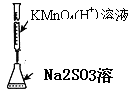 |
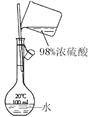 |
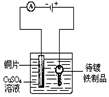 |
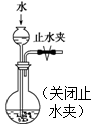 |
[2012·保定一模]桶烯(Barrelene)结构简式如图所示,则下列有关说法一定正确的是( )
| A.桶烯与苯乙烯(C6H5CH=CH2)互为同分异构体 |
| B.桶烯在一定条件下能发生加成反应,不能发生加聚反应 |
| C.桶烯二氯取代产物只有三种 |
| D.0.1mol桶烯完全燃烧需要消耗氧气22.4L |
[2012·课标全国卷] 分子式为C5H12O且可与金属钠反应放出氢气的有机化合物有(不考虑立体异构)( )
| A.5种 | B.6种 | C.7种 | D.8种 |
某同学通过系列实验探讨Mg及其化合物的性质,操作正确且能达到目的的是( )
| A.将水加入浓硫酸中得稀硫酸,置镁片于其中探讨Mg的活泼性 |
| B.将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成 |
| C.将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
| D.将Mg(OH)2沉淀转入表面皿中,加足量稀盐酸,加热蒸干得无水MgCl2固体 |
[2012·江苏卷] 下列根据实验操作和现象所得出的结论正确的是( )
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 |
均有固体 析出 |
蛋白质均发生变性 |
| B |
向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 |
出现白色沉淀 |
溶液X中一定含有SO42- |
| C |
向一定浓度的Na2SiO3溶液中通入适量CO2气体 |
出现白色 沉淀 |
H2SiO3的酸性比H2CO3的酸性强 |
| D |
向浓度均为0.1 mol·L-1 NaCl和NaI混合溶液中滴加少量AgNO3溶液 |
出现黄色 沉淀 |
Ksp(AgCl)>Ksp(AgI) |
[2012·泉州第二质检]有一无色溶液,可能含有K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的一种或几种。为确定其成分,进行如下实验:①取部分溶液,逐滴滴入NaOH溶液至过量,只观察到白色沉淀先增多后又部分溶解,无其它明显现象;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,无沉淀产生。下列推断正确的是
| A.肯定有Al3+、Mg2+、Cl-,可能有K+ |
| B.肯定有Al3+、Mg2+、Cl-,可能有NH4+ |
| C.肯定有Al3+、Mg2+、HCO3-,肯定没有MnO4- |
| D.肯定有K+、Al3+、MnO4-,可能有HCO3- |
海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案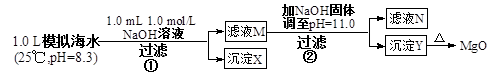
| 模拟海水中的 离子浓度(mol/L) |
Na+ |
Mg2+ |
Ca2+ |
Cl― |
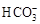 |
| 0.439 |
0.050 |
0.011 |
0.560 |
0.001 |
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;
实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;
Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12。
下列说法正确的是( )
A.沉淀物X为CaCO3
B.滤液M中存在Mg2+,不存在Ca2+
C.滤液N中存在Mg2+、Ca2+
D.步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
某化学小组的同学到实验室学习。在实验桌上摆有下列仪器:
(1)甲同学想用d进行实验,请你说出该仪器(已经洗涤干净)使用时的第一步操作:__________________________________。
(2)关于e的用途,乙同学说可组成防倒吸装置。你还能说出其他两种用途吗?
①_____________________________;②____________________________。
(3)丙同学想用下图装置用大理石和稀盐酸反应制取CO2。教师指出,这需要太多的稀盐酸,造成浪费。该同学选用了上面的一种仪器,加在装置上,解决了这个问题。请你把该仪器画在图中合适的位置。
[2012·北京朝阳区一模]某同学为了验证碳和硅两种元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验操作步骤:
Ⅰ. 打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ. A中看到白色沉淀时,…,关闭活塞a。
请回答:
(1)B中反应的离子方程式是__ ____。
(2)通过步骤Ⅰ得知盐酸具有的性质是________(填字母)。
| A.挥发性 | B.还原性 | C.氧化性 | D.酸性 |
(3)C装置的作用是________,X是________(写化学式)。
(4)为了验证碳的非金属性强于硅,步骤Ⅱ中未写的操作和现象是______ __,
D中反应的化学方程式是_____ ___。
(5)碳、硅的非金属性逐渐减弱的原因是________(从原子结构角度加以解释)。
[2012·石家庄质检]某研究性学习小组为探究Cu(OH)2受热分解产物及产物性质,设计如下实验。
(1)取0.98 g Cu(OH)2固体加热,质量随温度变化的曲线如图1所示,产物A、B的化学式分别为 和 。
(2)取少量产物B加入足量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在,该反应的离子方程式为 。
(3)为证明产物A在加热时能与NH3反应,某同学设计了如图Ⅱ(夹持装置未画出)所示实验装置。
①简述检查该装置气密性的方法 。
②实验过程中观察到两个明显现象:
i直玻璃管中固体由黑色变为红色;ii装置乙中固体由白色变为蓝色。
能证明产物A与NH3发生了反应的判断依据的是 (填选项字母)。
a.只有i可以 b.只有ii可以 c.i或ii都可以
[2012·山东卷] 实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下:
(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入________(填“A”或“B”),再滴加另一反应物。
(2)如下图所示,过滤操作中的一处错误是____________________________。
(3)判断流程中沉淀是否洗净所用的试剂是________。高温焙烧时,用于盛放固体的仪器名称是________。
(4)无水AlCl3(183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
装置B中盛放饱和NaCl溶液,该装置的主要作用是________。F中试剂的作用是_____________________________。
用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为________。
[2012·漳州质检]某研究学习小组为探究Fe3+离子是否能氧化SO2,设计了如下的实验装置(假设实验中所用装置的气密性良好)。
(1)甲同学利用以上实线框内装置制取SO2并进行探究实验。
①装置A中发生反应的化学方程式为 。
②装置B的作用是 。
③反应一段时间后,甲同学取装置C中少量溶液,往其中加入HCl酸化的BaCl2溶液观察到有白色沉淀产生。由此他得出结论:Fe3+可氧化SO2。
(2)乙同学认为甲同学的实验不严谨,他用以上虚线框内装置替代装置A,先使装置E内试剂反应一段时间后,关闭活塞1,打开活塞2,又反应片刻后,取装置C中少量溶液,往其中加入酸性KMnO4溶液,观察到KMnO4溶液紫红色褪去。由此他得出结论:Fe3+已被SO2还原成Fe2+。
①该实验制H2时需用浓硫酸配制450mL3mol/L的稀硫酸,配制中所需的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需 。
配制过程中若其它操作无误,但没有洗涤烧杯与玻璃棒,则所配制溶液的浓度会 (填“偏高”、“偏低”或“无影响”)。
②在该实验过程中H2所起得作用是 。
(3)丙同学认为甲、乙的实验均不严谨,为此他沿用乙同学的实验装置及操作,重新实验。待装置F内反应一段时间后,取装置C中少量溶液,往其中加入HCl酸化的BaCl2溶液,得出与甲同学相同的结论。请你分析回答:
①甲同学实验不严谨的原因是 。(选填序号)
| A.SO2溶解量太小 |
| B.SO2不与Fe3+发生反应 |
| C.H2SO3与BaCl2不反应 |
| D.装置中的空气与SO2进入水中也可生成H2SO4 |
②乙同学的实验结论不严谨的原因是 。
[2012·江苏卷] 废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)回收 Cu并制备ZnO的部分实验过程如下:
(2)①铜帽溶解时加入H2O2的目的是______ _____________________(用化学方程式表示)。
②铜帽溶解完全后,需将溶液中过量的H2O2除去。除去H2O2的简便方法____ ___。
(3)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点。上述过程中反应的离子方程式如下:
2Cu2++4I-===2CuI(白色)↓+I2
2S2O32-+I2===2I-+S4O62-
①滴定选用的指示剂为________,滴定终点观察到的现象____________________。
②若滴定前溶液中的H2O2没有除尽,所测定的Cu2+含量将会________(填“偏高”、“偏低”或“ 不变”)。
已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
| |
开始沉淀的pH |
沉淀完全的pH |
| Fe3+ |
1.1 |
3.2 |
| Fe2+ |
5.8 |
8.8 |
| Zn2+ |
5.9 |
8.9 |
实验中可选用的试剂:30% H2O2、1.0 mol·L-1 HNO3、1.0 mol·L-1 NaOH。
由除去铜的滤液制备ZnO的实验步骤依次为:
①____________________________________________________________;
②__________________________________________________________________;
③过滤;
④___________________________________________________________________;
⑤过滤、洗涤、干燥;
⑥900 ℃煅烧。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号