榴石矿石可以看作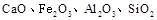 组成,由榴石矿石制取氯化钙和氧化铝的实验步骤如下:
组成,由榴石矿石制取氯化钙和氧化铝的实验步骤如下: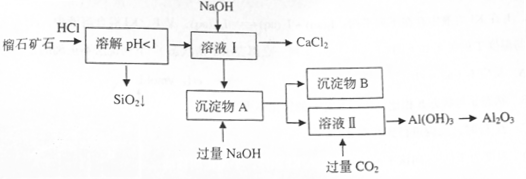
(1)榴石矿加盐酸溶解后,溶液里除了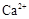 外,还含有的金属离子是 。
外,还含有的金属离子是 。
(2)对溶液I进行操作时,控制溶液PH=9~10(有关氢氧化物沉淀的PH见下表)
NaOH不能过量,若NaOH过量可能会导致 溶解, 沉淀。
(3)写出向沉淀物A中加入过量氢氧化钠溶液的离子方程式 。
(4)①某同学在实验室中用图I装置制取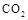 气体并通入溶液II中,结果没有沉淀产生,可能的原是 ;为了能产生沉淀该同学对图I装置进行了改进,改进的方法为 。
气体并通入溶液II中,结果没有沉淀产生,可能的原是 ;为了能产生沉淀该同学对图I装置进行了改进,改进的方法为 。
②若将二氧化碳气体通入澄清石灰水中,石灰水变浑浊,混合体系中除存在电离平衡、水解平衡外,还存在溶解平衡,用方程式表示该溶解平衡关系 。
实验室配制氯化亚铁溶液时是把氯化亚铁溶解于煮沸过的蒸馏水中,并加入_________________,向氯化亚铁溶液中加入氢氧化钠溶液时能观察到的现象是________________________反应的化学方程式是__________________________、
_______________________________________.
某同学用18 mol/L的浓硫酸配制200mL 0.9mol/L的稀硫酸,并进行有关实验。请回答下列问题:
(1)需要量取浓硫酸 mL。
(2)容量瓶是一种颈部细长的梨形瓶,由于其颈部细长,所以在向容量瓶中移入液体时,需要一定的耐心和技巧。有人建议将容量瓶的瓶颈改粗,对该建议的正确评价是( )
| A.可以按此建议改进,便于使用容量瓶 |
| B.不能按此建议改进,因为会降低容量瓶的精确度 |
| C.如果加粗瓶颈,可将原来刻在容量瓶瓶颈上的刻度改刻在容量瓶的瓶身上 |
| D.不必加粗瓶颈,因为向容量瓶中转移液体时,有少量液体倒出瓶外,不会对溶液的浓度产生太大影响 |
(3)配制该稀硫酸时使用的仪器除量筒、烧杯、200mL容量瓶外,还必须用到的仪器有
、 等。
(4)若硫酸溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度 0.9 mol·L-1(填“大于”、“等于”或“小于”,下同)。
(5)取所配制的稀硫酸100 mL,与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.448 L,则参加反应的锌的质量为 g;设反应后溶液的体积仍为100 mL ,则反应后溶液中H+的物质的量浓度为 mol/L。
使用启普发生器制取气体,具有随时可控制反应进行和停止的优点。某化学兴趣小组制作了如图所示的装置 ,代替启普发生器。
,代替启普发生器。
(1)图中A仪器的名称是 ,缺少的仪器是 ,
(2)制作B使用的是( )
A、铁片 B、铝箔 C、纸片 D、塑料片
(3)在该装置中用下列反应制气体,反应原理可行,且可能达到上述优点的是( )
A、Na2CO3·10H2O+HCl→CO2↑ B、Cu+H2SO4→H2↑ C、CaCO3+HNO3→CO2↑
(4)若用该装置进行锌粒与稀硫酸反应制取氢气的实验;对装置作气密性检查的方法是 ,
(5)向装置中加入锌粒的方法是 。
(6)当需反应停止时的操作和发生的现象是 。
以白云石(化学式表示为MgCO3·CaCO3)为原料制备Mg(OH)2的工艺流程如下图所示。
(1)研磨的作用是 。
(2)该工艺中可循环使用的物质是 、 (写化学式)。
(3)白云石轻烧的主要产物是MgO·CaCO3,而传统工艺是将白云石加热分解为MgO和CaO后提取,白云石轻烧的优点是 。
(4)加热反应的离子方程式为 。
(5)①加热反应时,在323k和353k溶液中c(NH4+)与反应时间的关系如下图所示,请在下图画出373k的曲线。
②由图可知,随着温度升高: 。
实验室需要0.80 mol/L NaOH溶液475 mL和0.40 mol/L硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号),配制上述溶液还需用到的玻璃仪器是 (填仪器名称)。
(2)下列操作中,容量瓶所不具备的功能有 (填序号)。
| A.配制一定体积准确浓度的标准溶液 |
| B.量取一定体积的液体 |
| C.测量容量瓶规格以下的任意体积的液体 |
| D.准确稀释某一浓度的溶液 |
E.贮存溶液
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为 g。在实验中其他操作均正确,若定容时俯视视刻 度线,则所得溶液浓度 0.8 mol/L(填“大于”、“等于”或“小于”,下同)。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度 0.8 mol/L。
度线,则所得溶液浓度 0.8 mol/L(填“大于”、“等于”或“小于”,下同)。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度 0.8 mol/L。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为 mL(计算结果保留一位小数)。如果实验室有10 mL、15 mL、20 mL、50 mL量筒,应选用 mL量筒最好。
某同学用10mol·L—1的浓盐酸配制250mL 1 mol·L—1的稀盐酸,并进行有关实验。请回答下列问题:
(1)需要量取浓盐酸 mL。
(2)配制该稀盐酸时使用的仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有
等。
(3)取所配制的稀盐酸100mL与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.896L,则参加反应的锌的质量为多少克?(写出计算过程)
(4)设反应后溶液的体积仍为100mL,则反应后溶液中H+物质的量浓度是多少?(写出计算过程)
过氧化氢是一种重要的化学产品,在工农业生产和日常生活中有着广泛应用,工业采用烷基薏醌法生产
根据生产过氧化氢原理和工艺,回答下列问题:
(1)该生产过氧化氢的原理中,原子利用率为 。
(2)该工艺中有机溶剂为液态烷烃和酯类,能否用乙醇代替?
(3)为了提高经济效益,该工艺氢化反应,除了加催化剂外,还可采取的措施是 。
A.适当加热 B.加压 C.增大工作液中有机溶剂的量
(4)该工艺中“后处理”的目的是 。
(5)该工艺中由35%的H2O2得到70%的H2O2可采取操作方法是 。
(6)硫酸酸化的过氧化氢溶液可溶解金属铜,试写出该反应的离子方程式为 。
在下图所示的实验装置中,A中盛有品红溶液,B 中盛有NaOH溶液。
请回答下列问题:
(1) 若向A中通入足量的二氧化硫气体,A中的现象是 。
(2) 若向A中通入足量的氯气后,再加热A,A中的溶液
(填“能”或“不能”)恢复到原来的颜色。
工业上用软锰矿(主要成分MnO2,杂质金属元素Fe、Al等) 制备MnSO4·H2O 的一种工艺流程如下:
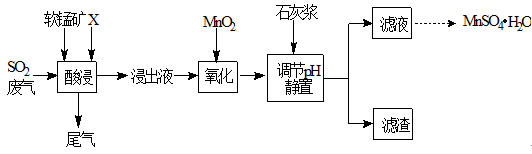
已知:
1.浸出过程中发生的主要反应化学方程式为:MnO2+SO2 =MnSO4
2.浸出液中阳离子主要有Mn2+、Fe2+、Al3+等
回答下列问题:
(1)物质X最好选用
a.盐酸 b.硫酸 c.硝酸
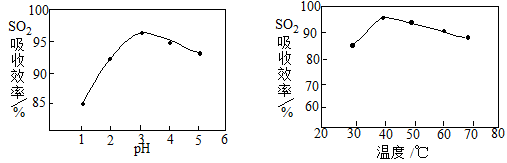
(2)酸浸时SO2的吸收效率与pH、温度的关系如下图所示,为提高SO2的吸收效率,酸浸适宜的条件是 。
(3) 流程中“氧化”步骤主要反应的离子方程式是 。
(4) 加入石灰浆调节pH,可将氧化后的浸出液中Fe3+、Al3+形成氢氧化物除去。检验Fe3+是否除尽的最佳方法是 。
(5) 用MnSO4可测定水中溶解氧,方法是:取100 mL 水样,迅速加入足量MnSO4溶液及含有NaOH的KI溶液,立即塞上塞子、振荡,使之充分反应;打开塞子,迅速加入适量的稀硫酸,此时有I2生成;再用5.00×10-3 mol·L-1 Na2S2O3溶液和I2反应,当消耗Na2S2O3溶液 12.0 mL时反应完全。有关化学反应方程式如下:
① 2Mn2++O2+4OH-=2MnO(OH)2(反应很快);
② MnO(OH)2+2I-+4H+=Mn2++I2+3H2O;
③ I2+2S2O32-=S4O62-+2I-。
计算水样中溶解氧的浓度(以mg·L-1为单位),写出计算过程。
如下图所示,A、B、C是实验室常用的三种制取气体的装置,提供的药品有:大理石、浓盐酸、稀盐酸、锌粒、二氧化锰、氯化铵、熟石灰。现欲利用这些药品分别制取NH3、Cl2、H2、CO2四种气体,试回答以下问题。
(1)选用A装置可制取的气体有 ;选用B装置可制取的气体有 ;通常选用C装置制取的气体有 。若用亚硫酸钠和浓硫酸来制取二氧化硫气体应选用装置 (填装置的编号字母)。
(2)写出利用上述有关药品制取氯气的化学方程式: 。
(3)若要制得干燥的氨气,可选用下列干燥剂中的 (填序号)。
A.生石灰 B.浓硫酸 C.五氧化二磷
(4)标号①的仪器除可用于在气体发生装置中添加试剂外,在实验中常用于 (填实验操作名称)。
请回答下列实验室中制取气体的有关问题。
(1)如图是用KMnO4与浓盐酸反应制取适量氯气的简易装置。
装置B,C,D的作用分别是:B ;C ;D 。
(2)在实验室欲制取适量NO气体。
①下图中最适合完成该实验的简易装置是 (填序号);
②根据所选的装置完成下表;(不需要的可不填)
| |
应加入的物质 |
所起的作用 |
| A |
|
|
| B |
|
|
| C |
|
|
| D |
|
|
③简单描述应观察到的实验现象 。
⑴用18mol/L浓硫酸配制100mL 1.0mol/L的稀硫酸,若实验仪器有:
A.100mL量筒 B.玻璃棒 C.托盘天平 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
实验时必须选用的仪器是(填入字母)
|
⑵在配制过程中,下列操作不正确的是
A.使用容量瓶前需检查它是否漏水实验室常用浓硫酸和乙醇混合加
 热制取乙烯。
热制取乙烯。
(1) 实验室制乙烯的化学方程式为 。
(2)实验室用浓硫酸和乙醇混合加热制乙烯可用如上图所示装置,下列说法正确的是 。
A.浓硫酸只作催化剂
B.在反应容器中放入几片碎瓷片防止混合液暴沸
C.反应温度缓慢上升至170℃
D.用排水法或向下排气法收集乙烯
E.园底烧瓶中装得是4mL乙醇和12mL3mol/L H2SO4混合液
F.温度计应 插入反应溶液液面下,以便控制温度
插入反应溶液液面下,以便控制温度
G.反应完毕后先熄灭酒精灯,再从水中取出导管
(3)若将此装置中的温度计换成分液漏斗,则还可以制取的气体有(酒精灯 可用可不用) 。
可用可不用) 。
A.CO2 B.NH3 C.O2 D.SO2 E.NO2 F.Cl2
(4) 如温度过高,反应后溶液颜色变 。某同学设计下列实验以确定上述混合气体中含有乙烯和SO2。
①I、II、III、IV装置可盛放的试剂是(请将下列有关试剂的序号填入空格内):
A、品红 B、NaOH溶液 C、浓硫酸 D、酸性KMnO4溶液
I  ;II ;III ;IV 。
;II ;III ;IV 。
②能说明SO2气体存在的现象是
③使用装置II的目的是 ;
④使用置III的目的是 ;
⑤确定含有乙烯的现象是 。
某同学用胆矾晶体(CuSO4·5H2O )配制0.40mol/L的CuSO4溶液1000mL,
回答下列问题:
(1)所需仪器为:(1000mL)容量瓶、托盘天平、药匙、 胶头滴管 ,还需要哪些玻璃仪器才能完成该实验,请写出:①___________ ,②___________
(2)写出该实验步骤 ①计算 ②称量胆矾__________g ③ ___________ ④转移 ⑤洗涤并转移 ⑥定容 ⑦摇匀
(3)下列情况对所配制的CuSO4溶液浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.容量瓶用蒸馏洗涤后残留有少量的水________________
B.所用过的烧杯、玻璃棒未洗涤________________
C.定容时俯视刻度线________________