有下列6种物质:Na2SO4、Na2SO3、K2SO4、I2、H2SO4、KIO3组成一个氧化还原反应,请回答下列问题:
(1)将这6种物质分别填入下面对应的横线上,组成一个未配平的化学方程式:
________+Na2SO3+________→________+________+________+H2O
(2)反应物中发生氧化反应的物质是_________(填化学式),被还原的元素是_______。
(3)反应中1mol氧化剂_______(填“得到”或“失去”)________mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:
□__________ +□__________ +□__________ →
H2O2是在医疗、化工方面应用广泛的化学试剂。
(1)Na2O2、CaO2以及BaO2都可与酸作用生成过氧化氢,实验室通过上述某种过氧化物与适量稀硫酸作用,过滤后即可制得较纯净的H2O2溶液,则应选择的过氧化物是________;
(2)实验室可用H2O2与次氯酸钠反应制氧气,其中还原剂是__________,写出该反应的化学方程式 ,生成0.5mol氧气,转移电子______mol;
(3)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:
H2O2 + KMnO4 + H2SO4 → MnSO4 + K2SO4 + O2↑ + H2O ,若滴定中消耗0.50mol/L的高锰酸钾溶液40.00mL,则此双氧水溶液中溶质的质量为____________ g。
把19.2 g 的Cu放入500mL 2 mol∙L−1稀硝酸中,充分反应,Cu完全溶解。求:
(1)写出Cu与稀硝酸反应的离子方程式: ;
(2)铜完全溶解时转移电子数目为 (用含NA的式子表示);
(3)氧化剂与还原剂的物质的量比为 。
(4)反应后溶液中C(H+)为 (体积变化忽略不计)
已知下列两个反应①Fe+H2SO4(稀)=FeSO4+H2↑
②Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O。试回答下列问题:
CuSO4+SO2↑+2H2O。试回答下列问题:
(1)反应①中 元素被还原,反应②中 元素被还原.
(2)当反应①生成2gH2时,消耗H2SO4的物质的量是 。
(3)反应②若有1mol H2SO4作氧化剂时,转移电子的物质的量为 ,若有4mol H2SO4参加反应时,被还原元素的质量是 g。
有下列6种物质:Na2SO4、Na2SO3、K2SO4、I2、H2SO4、KIO3组成一个氧化还原反应,请回答下列问题:
(1)将这6种物质分别填入下面对应的横线上,组成一个未配平的化学方程式:
________+Na2SO3+________→________+________+________+H2O
(2)反应物中发生氧化反应的物质是_________(填化学式),被还原的元素是_______。
(3)反应中1mol氧化剂_______(填“得到”或“失去”)________mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:
□__________ +□__________ +□__________ →
I.已知有如下氧化还原反应:Zn+2HNO3+NH4NO3=N2↑+Zn(NO3)2+3H2O,则:
(1)该反应的还原剂为 ,还原产物为 。(写化学式)
(2)若产生的N2在标准状况下体积为2.24L,则反应中转移的电子数为 NA。
II.化学与我们的生活密切相关,请用化学方程式描述以下生活中的实例:
(1)盛有NaHCO3的干粉灭火器用于灭火
(2)铁质菜刀的“淬火”工艺:将红热的菜刀浸入水中急速冷却
(3)饲养金鱼用的自来水必须经过太阳暴晒后才能使用
把Cl2通入浓氨水中,发生下述反应:3Cl2 + 8NH3 = 6NH4Cl + N2,发生化学反应的Cl2与NH3的分子数之比为: ,反应中发生电子转移的Cl2与NH3的分子数之比为:
对反应3Cl2 + 8NH3== 6 NH4Cl + N 2
(1)该反应中的氧化剂是__________ ,被氧化的元素是 。
(2) 1 mol Cl2参加反应,被氧化的NH3的物质的量是 mol。
(3) 标出该反应中电子转移情况 。
(4) 若有68g NH3参加反应,电子转移的物质的量是 mol。
过量铁粉与稀硝酸反应的方程式为:
3Fe + 8HNO3 (稀)= 3Fe(NO3)2 + 2NO↑ + 4H2O
① 标出电子转移的方向和数目
② 该反应的氧化剂是 ,还原产物是 ;
③ 标准状况下,当生成2.24L NO气体时, 有 g Fe参加反应,转移的电子总数为个,有 mol氧化剂被还原。
亚硝酸钠(NaNO2)又称工业盐,其外观类似食盐,但有剧毒。近年来,建筑工地多次发生民工误食工业盐而中毒的事件。利用如下反应可鉴别NaNO2和NaCl。
___KMnO4+___NaNO2+___H2SO4=___MnSO4+___K2SO4+___NaNO3+___H2O
(1)配平上述反应的化学方程式;
(2)指出该反应的氧化剂 ;
(3)当有2mol氧化剂被还原时,则转移的电子是 mol。
(6分) 氯气在生产生活中应用广泛。
(1)工业上可用MnSO4溶液吸收氯气,获得Mn2O3,Mn2O3广泛应用于电子工业、印染工业等领域。请写出该化学反应的化学方程式 。
(2)海底蕴藏着丰富的锰结核矿,其主要成分是MnO2 。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的MnO2,其制备过程如下图所示: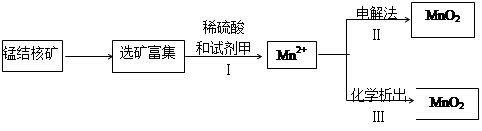
①步骤I中,试剂甲必须具有的性质是 (填序号)。
a. 氧化性 b.还原性 c.酸性
②步骤Ⅲ中,以NaClO3为氧化剂,当生成0.050 mol MnO2时,消耗0.10 mol·L-1的NaClO3溶液200 mL ,该反应的离子方程式为________________。
(每格2分,共8分)配平该化学方程式
□K37ClO3 + □H35Cl —□KCl+□Cl2 +□H2O.
该反应中HCl体现了_______性,若反应中有1.5mol电子发生转移生成Cl2________mol,所得Cl2的相对分子质量是_________(保留小数点后一位) 。
已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中含有Cl 、ClO
、ClO 、
、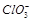 ;三种含氯元素的离子,其中C1O
;三种含氯元素的离子,其中C1O 、
、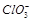 两种离子的物质的量(n)与反应时间(t)的曲线如右图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如右图所示。
(1)t1前,氧化产物是 (填化学式)。
(2)t2时,Ca(OH)2与Cl2发生反应的总的离子方程式为:
(3)该石灰乳中含有Ca(OH)2的物质的量是 mol
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是 (填字母)。
| A.NaCl、Cl2 | B.NaCl、NaClO |
| C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
(5)配平下列离子方程式: Fe(OH)3+ ClO + OH
+ OH ————
———— 


已知反应:3I-(aq)+S2O82-(aq)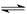 I3-(aq)+2SO42- (aq)
I3-(aq)+2SO42- (aq)
(1)写出反应的平衡常数表达式K= ;
(2)右图表示反应过程中有关物质的能量,则反应的 0(填“>”、“<”或“=”);
0(填“>”、“<”或“=”);
(Ⅰ)、(Ⅱ)两线中,使用催化剂的是 线;
(3)反应中发生反应的I-与被氧化的I-的物质的量比为 ;
(4)反应的速率可以用 与加入的淀粉溶液反应显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,记录的数据如下:
与加入的淀粉溶液反应显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,记录的数据如下:
| 实验编号 |
① |
② |
③ |
④ |
⑤ |
| c(I-)/mol·L-1 |
0.040 |
0.080 |
0.080 |
0.160 |
0.160 |
c( )/mol·L-1 )/mol·L-1 |
0.040 |
0.040 |
0.080 |
0.080 |
0.040 |
| t/s |
88 |
44 |
22 |
11 |
t1 |
则:该实验的目的是 ,显色时间t1= 分析表中数据,得出的结论是 。