12.8 g铜片与某浓度的硝酸反应后,铜片全部溶解,生成气体的体积在标准状况下为4.48 L。试计算:
(1)被还原的硝酸的物质的量为 ;
(2)4.48 L气体中各成分的物质的量为 。
已知钙的金属活泼性介于钾和钠之间,其化学性质与钠相似。钙及其化合物的有关反应如下:
①Ca+2H2O Ca(OH)2+H2↑ ②CaO+H2O
Ca(OH)2+H2↑ ②CaO+H2O Ca(OH)2
Ca(OH)2
③CaO2+H2O ④CaO+CO2
④CaO+CO2 CaCO3
CaCO3
⑤2CaO2+2CO2 2CaCO3+O2
2CaCO3+O2
结合所学知识完成下列问题:
(1)完成上述③的化学方程式: CaO2 + H2O ;
;
(2)用双线桥标出反应①的电子转移方向和数目:Ca+2H2O Ca(OH)2+H2↑
Ca(OH)2+H2↑
(3)写出以钙为原料制取过氧化钙(CaO2)的化学方程式: ;
(4)在CaO2的水溶液中,滴入酚酞溶液,预期的实验现象可能是 ;在该溶液中加入少量的MnO2固体,有气泡生成,写出该反应的化学方程式 。
某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀CuI。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
已知:I2+2S2O32-=S4O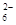 +2I-
+2I-
①可选用_____作滴定指示剂,滴定终点的现象是_______________________________ 。
②CuCl2溶液与KI反应的离子方程式为_______________________________________。
③该试样中CuCl2·2H2O的质量百分数为________。
氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
NO3-+4H++3e-→NO↑+2H2O
KMnO4、Na2CO3、FeO、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的离子方程式:
(2)若有0.3mol甲参加反应,标准状况下可生成NO L。
木炭与浓硫酸反应可表示为:C +2H2SO4(浓) CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(1)木炭作 (填“氧化剂”或“还原剂”),硫酸 (填“被氧化”或“被还原”)。
(2)若消耗了1 mol H2SO4,则生成 mol SO2。
K2Cr2O7是一种橙红色具有强氧化性的化合物,当它在酸性条件下被还原成正三价铬时,颜色变为绿色。据此,当交警发现汽车行驶不正常时,就可上前阻拦,并让司机对填充了吸附有K2Cr2O7的硅胶颗粒的检验装置吹气。若发现硅胶变色达到一定程度,即可证明司机是酒后驾车。这时酒精被氧化为醋酸其反应原理如下:
2K2Cr2O7+3CH3CH2OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O
请结合上面的描述回答下列问题:
(1)将上述反应改写为离子方程式: 。
(2)如果司机属于醉酒驾车,则检验装置中的硅胶将由 色变为 色。
(3)上述反应中氧化剂是 ,还原剂是 ,氧化产物是 ,还原产物是 。(本题中的四个空都需填写物质的化学式)
(4)在上述反应中当有69g酒精发生反应时消耗K2Cr2O7的物质的量是
(1)用稀硫酸浸泡由黄铜矿(主要成分CuFeS2)冶炼铜得到的滤渣,取少量所得溶液,滴加KSCN溶液后呈红色,则溶液中存在 (离子符号)。
写出上述反应的离子方程式:_______ _________。
(2)铜在自然界存在于多种矿石中,如
| 矿石名称 |
黄铜矿 |
斑铜矿 |
辉铜矿 |
孔雀石 |
| 主要成分 |
CuFeS2 |
Cu5FeS4 |
Cu2S |
CuCO3·Cu(OH)2 |
请回答下列问题:
①上表所列铜化合物中,铜的质量百分含量最高的是 (填化学式)。
②工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。该工艺的中间过程会发生反应:2Cu2O+Cu2S 6Cu+SO2↑(Cu2S中S的化合价为-2),该反应的氧化剂是__________。若此反应得到64克铜,则过程中转移的电子数________。
6Cu+SO2↑(Cu2S中S的化合价为-2),该反应的氧化剂是__________。若此反应得到64克铜,则过程中转移的电子数________。
(10分)向淀粉溶液和碘水的蓝色混合溶液中通氯气,溶液褪为无色,该反应体系有反应物和生成物共五种物质:I2、HIO3、H2O、Cl2、HCl。
(碘单质遇淀粉变蓝)
(1)该反应中发生氧化反应的物质是__________,氧化剂是___________,
(2)写出该反应的化学方程式,并用双线桥标出电子转移的方向和数目 ,
(3)如反应转移了0.3 mol电子,则至少需要氯气体积(标准状况下)为_________。
实验室里迅速制备少量氯气可利用以下反应:
KMnO4+ HCl  KCl + MnCl2 + Cl2↑ + H2O
KCl + MnCl2 + Cl2↑ + H2O
(1)请配平上述化学方程式,并在上面用“双线桥” 标明电子转移的方向和数目:
(2)该反应的氧化产物是 ,KMnO4发生 反应。
(3)用该浓盐酸制得了标况下560mlCl2,则被氧化的HCl为 mol,转移电子数为 。
(8分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3— + 4H+ + 3e- NO↑+2H2O; KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
NO↑+2H2O; KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式: 。
(2)反应中硝酸体现了 等化学性质。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是 mol。
(4)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是 。
(1)(6分)已知实验室制备氯气的反应:MnO2 +4HCl(浓) MnCl2 + Cl2↑+ 2H2O其中氧化剂是 ,还原剂是 ,氧化产物是 ,还原产物是 ,氧化剂和还原剂之比是 。
MnCl2 + Cl2↑+ 2H2O其中氧化剂是 ,还原剂是 ,氧化产物是 ,还原产物是 ,氧化剂和还原剂之比是 。
(2)配平氧化还原反应方程式:
__ C2O42-+__MnO4-+__H+=__CO2+__Mn2++__H2O
(3)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)2、H2O、H2O2 已知该反应中H2O2只发生如下过程:H2O2→ O2
①该反应中的氧化剂是 。
②该反应中,发生还原反应的过程是 → 。
③写出该反应的化学方程式,并标出电子转移的方向和数目 。
④如反应转移了0.6mol电子,则产生的气体在标准状况下体积为 。
(10分)已知砒霜As2O3与Zn可以发生如下反应:
As2O3+6Zn+6H2SO4===2AsH3↑+6ZnSO4+3H2O
(1)请用双线桥法标出电子转移的方向和数目。_____________________________。
(2)As2O3在上述反应中显示出来的性质是____________________。
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
(3)该反应的氧化产物是__________,还原产物是________。
(4)若生成0.2 mol AsH3,则转移的电子数为_____________________。
近年来,我国对储氢纳米碳管的研究获得了重大进展,电弧法合成的纳米碳管常伴有大量物质——碳纳米颗粒。这种碳纳米颗粒可用氧化法提纯。其反应的化学方程式为:
C + K2Cr2O7+ H2SO4(稀)="=" CO2+ K2SO4+ Cr2(SO4)3+
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂是 ,氧化产物是 。
(3)H2SO4在上述反应中表现出来的性质是 。
| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
(4)上述反应中若产生11.2 L(标准状况下)的气体物质,则转移的电子数目为 。
摩尔盐[(NH4)aFeb(SO4)c·zH2O]是一种重要化工原料。其组成可通过下列实验测定:
①称取1.5680 g 样品,准确配成100 mL溶液A。
②量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固体0.4660 g。
③再量取25.00 mL溶液A,滴加适量稀硫酸,用0.0200 mol·L-1KMnO4溶液滴定至终点,生成Mn2+,消耗KMnO4溶液10.00 mL。
(1)(NH4)aFeb(SO4)c·zH2O中存在a+2b-2c=0,则该物质中铁元素的化合价为 。
(2)③中发生反应的离子方程式为 。
(3)通过计算确定样品中n(NH4+)∶n(H2O)(必须写出计算过程)。