向体积为Va的0.05mol/L CH3COOH溶液中加入体积为Vb的0.05mol/LKOH溶液,下列关系错误的是:
| A.Va>Vb时:C(CH3COOH)+ C(CH3COO-)>C(K+) |
| B.Va=Vb时:C(CH3COOH)+ C(H+)="=" C(OH-) |
| C.Va<Vb时:C(CH3COO-)>C(K+)>C(OH-)>C(H+) |
| D.Va与Vb任意比时:C(K+)+C(H+)==C(OH-)+C(CH3COO-) |
往含有S2-和Cl-的稀溶液中逐滴加入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如右图所示。则原溶液中c(S2-)/c(Cl-)的比值为:
| A.2V1/V2 | B.2(V2-V1)/V1 | C.2V2/V1 | D.V1/2(V2-V1) |
下列化学用语或叙述正确的是( )
| A.-OH与OH-均是10电子粒子 | B.H2O2的电子式:H+[:O: O:]2-H+ |
| C.在分子晶体中不一定有化学键 | D.在晶体中,有阳离子就一定有阴离子 |
欲使0.1mol/L的稀氨水中,C(NH3·H2O)/C(OH-)逐渐减小,可采取的措施是:
| A.加入少量Al(OH)3固体 | B.加入少量NaOH晶体 |
| C.加入少量NH4Cl晶体 | D.继续加0.1mol/L的稀氨水 |
设NA表示阿伏加德罗常数,下列说法中正确的是( )
| A.1mol甲基正离子(CH3+)所含电子数为8NA |
| B.NA个H2分子的质量约为2g,它所占的体积约为22.4L |
| C.标准状况下,11.2LCHCl3中所含的分子数为0.5N |
| D.500mL 0.5mol/L的Ca(ClO)2溶液中,含有ClO-的数目为0.5N |
用98%的浓H2SO4(ρ=1.84g/cm3)配制成1.84mol/L的稀H2SO4 500ml,计算所需浓H2SO4的体积。(注意:要求写出简单的计算步骤。)
化学知识中有很多的“相等”,下列说法中不正确的是( )
| A.参加化学反应的物质的总质量等于反应后生成的物质的总质量 |
| B.化合物中元素化合价的正价总数与负价总数的数值相等 |
| C.溶液加水稀释前后溶质的质量相等 |
| D.在原子中原子核内的质子数和中子数都相等 |
将一定质量的Zn放入18mol/L的浓H2SO4中,充分反应后,共收集到标况下的气体4.48L,且1mol该气体的质量为48.5克。在反应后的溶液中,加入足量的BaCl2溶液,生成58.25克的沉淀。则求:
(1)所得气体的成份和各自的体积。
(2)所用Zn的质量。
(3)消耗浓H2SO4的体积为多少毫升(保留小数点一位)。
下列有关化学用语使用正确的是
A.磷(P)基态原子最外层轨道表示式: |
B.钢铁发生吸氧腐蚀的正极反应式- |
C.葡萄糖的实验式: |
D.氰基细电子式: |
判断下列有关化学基本概念的依据正确的是 ( )
| A.溶液与胶体:本质不同的原因是能否发生丁达尔效应 |
| B.氧化还原反应:有元素化合价升降 |
| C.强弱电解质:溶液的导电能力大小 |
| D.共价化合物:是否含有共价键 |
向等质量的a、b两份锌粉中,分别加入过量的稀H2SO4,同时向a中加入少量的CuSO4溶液。下图表示产生H2的体积(V)与时间(t)的关系,其中正确的是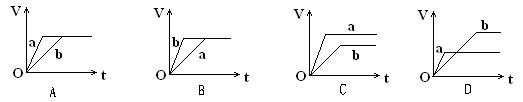
如图所示,2个X分子反应生成1个Y分子和3个Z分子,下列判断不正确的是
| A.根据质量守恒定律可推知,1个Z分子中含有2个A原子 |
| B.该反应属于分解反应 |
| C.该反应属于氧化还原反应 |
| D.X、Y、Z三种物质均属于非电解质 |
NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.标准状况下,11.2 L NO和11.2 L O2混合后气体的分子总数为0.75NA |
| B.室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
| C.常温下,pH=2的稀盐酸中所含有的H+离子数大于0.01 NA |
| D.1mol CH3+(碳正离子)中含有电子数为10NA |
设NA为阿伏加德罗常数,下列叙述中正确的是:
| A.常温下11.2L的甲烷气体含有甲烷分子数为0.5NA个 |
| B.标准状况下,11.2L四氯化碳所含分子数为0.5 NA |
| C.14g乙烯和丙烯的混合物中总原子数为3NA个 |
| D.1L、0.1mol/LH2SO3溶液中含SO32-离子数为0.1NA个 |
已知在T°C和一定压强下,往容积可变的密闭容器中充入2molSO2和1molO2,此时容器容积为VL,保持恒温恒压,使反应:2SO2(g)+O2(g)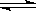 2SO3(g)在5min末达到平衡,测得SO3的体积分数为0.4;试回答下列问题:(1)平衡混合气体中SO2的体积分数为 ,平衡过程中O2的转化率为 ;(2)另选一容积固定不变的容器,仍控制温度为T°C,充入2molSO2和1molO2使反应,达到平衡时SO3的体积分数仍为0.4,则密闭容器的体积为: L。
2SO3(g)在5min末达到平衡,测得SO3的体积分数为0.4;试回答下列问题:(1)平衡混合气体中SO2的体积分数为 ,平衡过程中O2的转化率为 ;(2)另选一容积固定不变的容器,仍控制温度为T°C,充入2molSO2和1molO2使反应,达到平衡时SO3的体积分数仍为0.4,则密闭容器的体积为: L。