A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。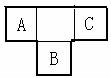
(1)B元素位于元素周期表中第 周期,第 族。
(2)由元素C与Mg元素形成的化合物的化学键的类型 。
(3)由元素A与氢元素形成的化合物的结构式 。
(4)由元素B与氢元素形成的化合物的电子式 。
(5)写出A的气态氢化物与B的最高价氧化物对应的水化物反应的化学方程式: 。
四种常见的短周期非金属元素在周期表中的相对位置如下所示,其中乙元素原子核外最外层电子数是其电子层数的3倍。
| 甲 |
乙 |
|
| |
丙 |
丁 |
请用化学用语回答:
(1)丙在元素周期表中的位置是 。
(2)丁单质的电子式是 。
(3)乙的两种常见单质分别是 、 。
(4)甲、乙、丙、丁的气态氢化物水溶液显酸性的是 、___________。
(5)氢元素和乙组成的化合物中,既含有极性共价键又含有非极性共价键的是____________ (填化学式)。此化合物可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为 。
(6)电解丙的饱和钠盐溶液的离子方程式为 。
(7)若甲的元素符号为X。已知:①X2(g)+2O2(g)===X2O4(l) ΔH=-19.5 kJ·mol-1;
②X2H4(l)+O2(g)===X2(g)+2H2O(g)ΔH=-534.2 kJ·mol-1。
则液态X2H4和液态X2O4反应生成气态X2和气态H2O的热化学方程式为 。
二氧化氯(ClO2)是国际公认高效、安全的杀菌、保鲜剂,是氯制剂的理想替代品。工业上制备ClO2的方法很多,NaClO3和NaClO2是制取ClO2的常见原料。
完成下列填空:
(1)以下反应是制备ClO2的一种方法:H2C2O4 + 2 NaClO3 + H2SO4 → Na2SO4 + 2 CO2↑ + 2 ClO2↑ + 2 H2O,上述反应物中属于第三周期的元素的原子半径大小顺序是__________;其中原子半径最大元素的原子,其核外有 种不同能量的电子。
(2)ClO2的分子构型为“V”形,则ClO2是______________(选填“极性”、“非极性”)分子,其在水中的溶解度比氯气__________(选填“大”、“小”、“一样”)。
(3)ClO2具有强氧化性,若ClO2和Cl2在消毒时自身均被还原为Cl-,ClO2的消毒能力是等质量Cl2的___________倍(保留2位小数)。
(4)若以NaClO2为原料制取ClO2,需要加入具有________(填“氧化”、“还原”)性的物质。
(5)工业上将氯碱工业和制取NaClO3联合进行。研究发现,电解时,不同反应环境下的总反应分别为:
4 NaCl + 18 H2O → 4 NaClO3 + 3 O2↑+ 18 H2↑(中性环境)
NaCl + 3 H2O → NaClO3 + 3 H2↑(微酸性环境)
①电解时,氢气在__________极产生。
②更有利于工业生产NaClO3的反应环境是___________,理由__________________。
今有aX、bY、cZ三种元素。已知:①各原子序数a、b、c均小于20,且a+b+c=25; ②元素Y的原子价电子构型为ns2npn+2; ③X和Y在不同条件下可形成X2Y和X2Y2两种化合物,Y和Z在不同条件下可形成ZY和ZY2两种化合物; ④Z的硫化物的相对分子质量与Z氯化物的相对分子质量之比为38︰77。回答下列问题:
(1)X: (写元素名称);Z的价电子排布图为: 。
(2)X2Y2的电子式 ,属于 化合物(填“离子”或“共价”)。
(3)Z的硫化物的VSEPR模型为 ,分子空间构型为 ;Z的氯化物的VSEPR模型和分子空间构型分别是 、 ,其中Z原子分别以 杂化轨道成键,根据原子轨道成键方式分,Z的硫化物分子中含有的键的种类及数目是 、 。
A、B、C、D、E、F为原子序数依次增大的短周期元素,G为第四周期元素,B、C相邻且同周期,A、D同主族。A、C能形成两种化合物甲和乙,原子个数比分别为2∶1和1∶1,甲为常见的溶剂。E是地壳中含量最多的金属元素。F元素为同周期电负性最大的元素。D和F可形成化合物丙,E和F可形成化合物丁。G为第四周期未成对电子数最多的元素。请回答下列问题:
(1)写出G基态原子的电子排布式
(2)B和C比较,第一电离能较大的元素是 (填元素符号),其原因为
(3)A与B形成的化合物易溶于化合物甲,其主要原因是
(4)甲、乙两分子中含有非极性共价键的是 (填分子式),它中心原子的杂化方式是
(5)已知化合物丁熔点190℃,沸点183℃,结构如右图所示。
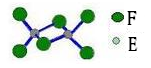
①丙和丁比较,熔点较低的化合物是 (填化学式),其原因为
②则丁含有的作用力有 (填序号)。
A.离子键 B.共价键 C.金属键
D.配位键 E.范德华力
现有下列物质,用编号填空回答下列问题:
A.干冰
B.金刚石
C.氦
D.过氧化钠
E.二氧化硅
F.溴化铵
G.H2O2
H.氢氧化钠
(1)通过非极性键形成的原子晶体是: 。
(2)含有极性键的离子化合物是: 。
(3)含有离子键、共价键、配位键的化合物是: 。
(4)含有极性共价键的非极性分子是 。
(5)含有极性共价键和非极性共价键的极性分子是 。
(6)A、B、C、D四种物质的熔点从低到高的顺序为________________。
Ⅰ.根据下列6种符号回答问题:
① 1H ② 2 H ③ 3 H ④ 14C ⑤ 14N ⑥16O
(1)共有 种核素,属于 种元素。
(2)互为同位素的是 。(填序号,下同)
(3)质量数相等的是 ,中子数相等的是 。
Ⅱ.现有6种物质: ①MgCl2 ②HCl ③SO2 ④ K2CO3 ⑤ CaO ⑥ NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物是 。
(2)只含离子键的化合物是 。
(3)含共价键的离子化合物是 。
已知有五种元素的原子序数的大小顺序为C > A> B> D > E;A和C同周期,B和C同主族;A和B形成离子化合物A2B 中,所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子的分子.试回答下列问题:
(1)写出以下元素的名称: A B E
(2)用电子式表示离子化合物A2B 的形成过程:
(3)写出D元素形成单质的结构式:
(4)写出下列物质的电子式:E与B形成的化合物:
A、B、E形成的化合物:
(5)A和B两元素形成的化合物A2B2中存在的化学键的类型是 。
有X、Y、Z三种短周期元素,分别位于不同的周期。已知X和Y原子最外层电子数相同,Z原子次外层只有2个电子,X和Z可以形成离子化合物X2Z,Y和Z可以形成共价化合物Y2Z
(1)写出X、Y、Z三种元素的元素符号:X是 ,Y是 ,Z是 ;
(2)X2Z的电子式 ,Y2Z的电子式 ;
(3)X2Z和 Y2Z反应的化学方程式 。
X、Y、Z、W、M、Q为原子序数依次增大的六种短周期元素,常温下,六种元素的常见单质中三种为气体,三种为固体。X与M,W与Q分别同主族, X是原子半径最小的元素,且X能与Y、Z、W分别形成电子数相等的三种分子,W是地壳中含量最多的元素。试回答下列问题:
(1)W、M、Q四种元素的原子半径由大到小的排列顺序是 > > (用元素符号表示)。
(2)元素M和Q可以形成化合物M2Q,写出M2Q的电子式 。
(3)Z、W、Q三种元素的简单气态氢化物中稳定性最强的是 (用分子式表示)。
(4)W的一种氢化物含18个电子,该氢化物与QW2化合时生成一种强酸,其化学方程式为
Z、W、Q四种元素组成的阴阳离子个数比为1:1的化合物A,已知A既能与盐酸反应生成气体,又能与氢氧化钠的浓溶液反应生成气体,且能使氯水褪色,写出A与足量氢氧化钠溶液在加热条件下反应的离子方程式 。
下表为长式周期表的一部分,其中的编号代表对应的元素。
| ① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |
② |
|
|
|
|
|
|
|
|
|
|
|
③ |
|
|
|
|
| |
④ |
|
|
|
|
|
|
|
|
|
|
⑤ |
|
|
⑥ |
⑦ |
|
| |
⑧ |
|
|
|
|
|
⑨ |
|
|
⑩ |
|
|
|
|
|
|
|
请回答下列问题:
(1)按电子排布,可把周期表中的元素划分成5个区,请在上图中划出区域并注明。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为 ;③和⑦形成的一种常见溶剂的化学式为 ,其立体构型为__________,键角为______。
(3)某元素原子的价电子排布式为nsnnpn+1,该元素原子的最外电子层上孤电子对数为 ;该元素与元素①形成的最简单分子X属于 分子(填“极性”或“非极性”)。
(4)元素④的第一电离能 元素⑤(选填“>”、“=”、“<”)的第一电离能;元素⑥的电负性 元素⑦(选填“>”、“=”、“<”)的电负性。
(5)元素⑥和①形成的化合物的结构式为 ; 元素⑨的基态原子核外电子排布式是 。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式
(8分)共价键都有键能之说,键能是指拆开1 mol共价键所需要吸收的能量或形成1mol共价键所放出的能量。
(1)已知H—Cl键的键能为431.4 kJ/mol,下列关于键能的叙述正确的是______。
A.每生成1 mol H—Cl键放出431.4 kJ能量
B.每生成1 mol H—Cl键吸收431.4 kJ能量
C.每拆开1 mol H—Cl键放出431.4 kJ能量
D.每拆开1 mol H—Cl键吸收431.4 kJ能量
(2)参考下表中的数据,判断下列分子受热时最稳定的是________。
| 化学键 |
H—H |
H—F |
H—Cl |
H—Br |
| 键能/kJ/mol |
436 |
565 |
431 |
368 |
A.HF B.HCl C.HBr D.H2
(3)能用键能大小解释的是________。
A.氮气的化学性质比氧气稳定
B.常温常压下,溴呈液态,碘呈固态
C.稀有气体一般很难发生化学反应
D.硝酸易挥发而硫酸难挥发
(4)已知:4HCl+O2═2Cl2+2H2O,该反应中,4mol HCl被氧化,放出115.6kJ的热量.断开1mol H﹣O键与断开1mol H﹣Cl键所需能量相差约为 kJ.
下表是元素周期表中的一部分,根据A~I在元素周期表中的位置,用元素符号或化学式回答下列问题:
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 |
A |
|
|
|
|
|
|
|
| 2 |
|
|
|
D |
E |
|
G |
I |
| 3 |
B |
|
C |
|
F |
|
H |
|
(1)上表中,化学性质最不活泼的元素是_____,氧化性最强的单质是_____,还原性最强的是_____。
(2)最高价氧化物对应水化物的碱性最强的元素是________,酸性最强的元素是________。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的是___________。
(4)请用电子式表示化合物BG的形成过程________________。
(5)写出C的最高价氧化物对应水化物与B的最高价氧化物对应水化物反应的离子方程式:______________。
A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)B在周期表中的位置为第___________周期第___________族。
(2)E元素形成的氧化物对应的水化物的化学式为________________。
(3)元素C、D、E形成的离子半径大小关系是________>________>__________(用离子符号表示)。
(4)用电子式表示化合物D2C的形成过程________________________。C、D还可形成化合物D2C2,D2C2含有的化学键是__________________。
(5)由A、B、C三种元素形成的离子化合物的化学式为______________,它与强碱溶液共热,发生反应的离子方程式是____________________。
(6)某一反应体系中含有D2E、D2EC3、D2EC4三种物质,若此反应为分解反应,则此反应的化学方程式为______________________(化学式用具体的元素符号表示)。
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为________________;A、B、C的电负性由大到小的顺序为___________;(均用“<”或“>”连接)
(2)B的氢化物的分子空间构型是_____________。其中心原子采取_____________杂化。
(3)写出化合物AC2的电子式____________;一种由B、C组成的化合物与AC2互为等电子体,其化学式为____________。
(4)E的价层电子排布式是____________,在形成化合物时它的最高化合价为_____________,ECl3形成的配合物的化学式为________________。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是________________。