下图各物质中,A、B、C是常见金属单质,甲、乙、丙是气体且乙是有特殊颜色的气体(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出:H的化学式_________,乙的两种重要用途________________________________
(2)写出有关反应的离子方程式:
反应①__________________________________________________________
反应②__________________________________________________________
(3)判断反应③己经发生的常用试剂是______________________
(4)胶态磁流体(液溶胶)在医学上有重要用途,C单质对应元素的某种纳米级氧化物是磁流体中的重要粒子,该磁流体的主要制备过程如下:(Ⅰ)将NH3通入F、G的混合溶液(F、G物质的量比为1:2)中会生成两种碱。(Ⅱ)这两种碱恰好反应就得到该氧化物。写出(Ⅱ)中反应的化学方程式为:_________________________,确定该磁流体己成功制取的方法_________________________________
已知气体X2和气体Y2在一定条件下能化合生成气体C,并知C的化学式只有三种可能:XY、X2Y、X3Y。为确定C的化学,某同学分别取同温同压下,体积都为V1的X2和Y2两种气体充入一恒压、容积可变的密闭容器中,在一定条件下反应完全并恢复到原温后,再测出容器的容积(V2)。请填写下列结论与分析
(1)若实验结果(用V1、V2间关系来表示)是___________,则生成物C的化学式为XY,判断的依据是_____________________________________________________
(2)当生成物C的化学式为X2Y时,则实验结果是_____________,生成C的化学方程式为____________
已知某无色溶液只由Fe3+、Mg2+、Cu2+、Al3+、NH4+、Cl-、HCO3- 、OH-中的几种组成,向此溶液中加入一种淡黄色粉末状固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀。继续加入淡黄色粉末时,产生无刺激性气味的气体,白色沉淀只能部分溶解,则此溶液中一定大量含有的离子 ( )
| A.Mg2+、Al3+、NH4+、Cl- | B.Mg2+、Al3+、NH4+ |
| C.Mg2+、Cu2+、NH4+、HCO3- | D.Mg2+、Cu2+、NH4+、Cl- |
A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种,现利用另一种溶液X,用如图所示的方法可将它们依次确定
试确定A、B、C、D、X各代表何种溶液。A:______,B:______,C:_____, D:_____,X:_______。
已知B、C为用途广泛的金属,H具有磁性氧化物,I是一种白色胶状沉淀,它们有如图所示的转化关系(部分产物未列出):
回答下列问题:
1.E和G的化学式分别为
2.写出反应的化学方程式:
① ③
写出反应的离子方程式
② ④
某白色粉末A在农业上用作杀菌剂,进行下列实验:
(1)白色粉末溶解在水中,得到蓝色溶液,分成等量的两份
(2)在其中一份蓝色溶液中加入适量的盐溶液B,恰好沉淀完全,过滤,得到白色沉淀和蓝色溶液;向该蓝色溶液中加入AgNO3并加入HNO3,生成白色沉淀且不溶解。
(3)在另一份蓝色溶液中加入适量C溶液,恰好沉淀完全,过滤,得到蓝色沉淀和纯净的硫酸钾溶液。
根据实验现象推断:
A B C
某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如右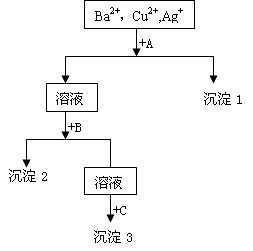
(1).沉淀的化学式:沉淀1 ,
沉淀2 ,沉淀3 ;
(2).写出混合液+A的离子方程式
溶液+B的离子方程式
已知:A、B为常见的非金属单质且均为气体;甲、乙为金属单质,乙在I的浓溶液中发生钝化;C、H、J的溶液均呈碱性.各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):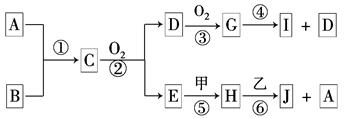
(1)写出反应②的化学方程式为_________________________________________。
(2)反应④中每消耗1 mol G,转移电子的物质的量为______________。
(3)反应⑥的离子方程式是___________________________________________。
(4)实验室中保存I的方法是____________________________。
煤的“气化”是使煤变成清洁能源的有效途径之一,其主要反应为: C+H2O CO+H2甲酸苯丙酯(F)是生产香料和药物的重要原料。下面是用煤为原料合成甲酸苯丙酯的路线图(部分反应条件和生成物已略去),其中D的分子式为C9H10O,且能发生银镜反应。
CO+H2甲酸苯丙酯(F)是生产香料和药物的重要原料。下面是用煤为原料合成甲酸苯丙酯的路线图(部分反应条件和生成物已略去),其中D的分子式为C9H10O,且能发生银镜反应。
根据上述转化关系回答下列问题:
(1)写出A、D的结构简式:A: ,D: 。
(2)D→E的反应类型为 。
(3)B与新制Cu(OH)2浊液反应也能生成C,写出其化学方程式:
(4)写出C与E反应生成F的化学方程式 。
(5)上图中所标注的6个反应,其中有4个原子利用率达到100%,请写出这4个反应 (填写反应序号)。
(6)F有多种同分异构体,写出满足下列条件的两种同分异构体的结构简式。
①属于酯类,且能发生银镜反应。②苯环上的一氯取代物只有两种结构。③分子结构中只有两个甲基。
、 。
根据反应框图填空,已知反应①~⑤均为工业生产及应用中常见反应,其中B、G、I、J、L均为常见单质,B、D、J、L为气体。A是工业生产F的重要矿石原料的主要成份,其相对分子质量为120。
(1)I元素在元素周期表中的位置_ ______;M中阴离子的结构示意图: 。
(2)固体A中所包含的化学键与固体Na2O2类似,则A的电子式为 。
(3)写出反应①所使用设备的名称___________________。
(4)写出下列化学反应的离子方程式:
① 反应⑤:______________________________________________ ___;
② G与N的反应:________________________________________________;
③ K与L的反应:________________________________________________。
(5)已知每生成16 gD,放出106.5 kJ热量,则反应① 的热化学方程式为:
的热化学方程式为:
。
中学化学中几种常见物质的转化关系如下:
将 D滴入氢氧化钠溶液中可得到F的红褐色沉淀。请回答下列问题:
(1)A、B、C、D、 E、F、H的化学式:A B __
E、F、H的化学式:A B __ _________、D ___________、E 。
_________、D ___________、E 。
(2)写出 C的酸性溶液与双氧水反应的离子方程:________________________。
(3)写出鉴定E中阳离子的离子方程式: 。
(1)仅根据上述信息就能够确定的元素是 (选填A、B、C、D)。
(2)在所有满足上述信息的短周期元素中,酸性最强的最高价氧化物的水化物是(填化学式) ;由A、D两元素构成的化合物A2D2的电子式为(用元素符号填写,下同): 。
(3)在满足上述信息的短周期元素中,若B2、CD和由B、C、D形成的化合物X的混合物 mg,在一定条件下与过量氧气充分反应后,将产物通过足量的固体A2D2,最终发现固体质量增重mg,则符合此条件的X的分子组成可用通式____________________来表示。
已知物质M由同一短周期的X、Y两种元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数和为6。M与其他物质的转化关系如下(部分产物已略去):
(1)工业电解M溶液的化学方程式为 。
(2)若A是X、Y同周期的一种常见金属,则A元素在周期表中的位置是 ,写出A与B溶液反应的化学方程式是 。
(3)若A是一种常见酸性氧化物,可用于制造光导纤维,则A元素原子结构示意图为
,写出E与F反应的离子方程式是 。
(4)举例说明M物质的一种用途 。
奥运五环“象征五大洲的团结,全世界的运动员以公正、坦率的比赛和友好的精神,在奥运会上相见”。右下图所示五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素;五种化合物由四种短周期元素形成,每种化合物仅含有两种元素。A是工业制取硝酸的主要原料之一;B、E分子中所含电子数都为18,B不稳定,具有较强的氧化性,E是由六个原子构成的分子,可作火箭燃料;C是工业制光导纤维的主要原料;D中所含的两种元素的原子个数之比为3∶4。根据以上信息回答下列问题:
(1)A用于工业制取硝酸所发生反应的化学方程式 。
(2)D的化学式是 ,E分子中含有 键和 键。
(3)B的水溶液呈弱酸性,其电离方程式可表示为 ,B在实验室中可以用于制取某种常见气体,其反应的化学方程式为 。
(4)B与E反应可生成单质G和一种常见的液体H,其反应的化学方程式为
。
(5)用化学方程式表示C的另一种用途 。
某些化学反应可用下式表示:A + B  C + D + H2O
C + D + H2O
请回答下列问题:
(1)若A、D均可用于消毒,且C是家家户户的厨房必备的物质之一,写出该反应的离子方程式: 。
(2)若A为水垢的主要成分之一,B是日常生活常见有机物,写出该反应的化学方程式: 。
(3)若A为黑色固体,C是黄绿色的单质气体,写出该反应的离子方程式: 。
(4)若A为亮红色单质,B为第二周期某种元素的最高价氧化物的水化物,A、B、C、D中只有D是气体,若D无色,写出该反应的化学方程式: 。
(5)若C、D均为气体且都能使澄清石灰水变浑浊,则只用 或 (任写两种试剂的名称)就可以鉴别C、D两种气体。