甲、乙、丙、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)
试回答下列问题:
(1)若X是强氧化性单质,则甲可能是__________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向丙的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀。则乙的化学式为________________;丙溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示)__________________________。
(3)若甲、乙、丙为含有金属元素的无机化合物,X为强电解质,甲溶液与丙溶液反应生成乙;反应①的离子方程式为____________________,或____________________。
(9分)已知X、Y、Z是阳离子,K是阴离子,M、N是分子。它们都由短周期元素组成,且具有以下结构特征和性质:
①它们的核外电子总数都相同;
②N溶于M中,滴入酚酞,溶液变红;
③Y和K都由A.B两元素组成,Y核内质子数比K多2个;
④X和N都由A、C两元素组成,X和Y核内质子总数相等;
⑤X和K的浓溶液在加热条件下生成M和N;
⑥Z为单核离子,向含有Z的溶液中加入少量含K的溶液,有白色沉淀生成,再加入过量的含K或Y的溶液,沉淀消失。
回答下列问题:
(1)Y的化学式为 ;N的电子式为
(2)试比较M和N的稳定性:M (填“>”或“<”)N。
(3)写出Z和N的水溶液反应的离子方程式: ;
(4))上述六种微粒中的两种可与硫酸根形成一种含三种离子的盐,向该盐的浓溶液中逐滴加入0.1 的NaOH溶液,出现了如图中a、b、c三个阶段的图像,
的NaOH溶液,出现了如图中a、b、c三个阶段的图像,
①写b出阶段的离子方程式:
②根据图像判断该盐的化学式为 。
(10分)A、B、C为三种单质(其中A为固体,B、C为气体),D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色,B、C反应的产物易溶于水得到无色溶液E.它们之间的转化关系如下图:
填写下列空白:
(1)物质A是________,B是________,C是________.
(2)F中加入NaOH溶液,并在空气中放置的化学方程式是________, .
A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第_____周期、第_____族;
(2)写出反应①的化学方程式______________________________________________;
(3)写出反应④的离子方程式______________________________________________;
(4)写出反应③的电极方程式:
阳极:_______________________ 阴极:___________________________
(5)从能量变化的角度看,①②③反应中属于△H<0的反应是___________。(填序号)
纳米TiO2作为一种光催化剂越来越受到人们的关注,现正广泛开发运用。
(1)制取纳米TiO2的方法很多,氢氧火焰水解法是将TiCl4气体导入氢氧火焰中(700~1000℃)进行水解,其化学反应式为: ▲ 。
(2)纳米二氧化钛可光解挥发性有机污染物(VOCs),若无水蒸气存在,三氯乙烯降解反应为:C2HCl3+2O2→2CO2+HCl+Cl2,若有足够量的降解后的尾气,实验室检验产物中有氯气的简单方法是: ▲ ;通过质谱仪发现还有多种副反物,其中之一为: ,则该有机物核磁共振氢谱有 ▲ 个峰。
,则该有机物核磁共振氢谱有 ▲ 个峰。
(3)利用半导材料TiO2与染料、铂电极及I 和I-的混合物作电解质(I2+I-
和I-的混合物作电解质(I2+I- I
I ),可构成染料敏化太阳能电池(DSSCs)工作原理如右图,该电池工作时,正极的电极反应为: ▲ 。
),可构成染料敏化太阳能电池(DSSCs)工作原理如右图,该电池工作时,正极的电极反应为: ▲ 。
(4)在不同的载体(钛片、铝片、陶瓷)表面制备二氧化钛薄膜,来考察不同载体TiO2薄膜光催化使甲基橙脱色,每次光照20min取一次样,实验结果如下。 w ww.k s5u. co m
w ww.k s5u. co m
下列说法正确的是 ▲ 。
(a)不同载体,无论何种温度一定是钛片最好
(b)约在520℃时,钛片载体的光催化活性最好
(c)无论何种载体,催化活性总是随温度的升高而升高
(d)不同负载TiO2薄膜的光催化活性不同
粉煤灰是燃煤电厂排出的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为43.4%,还有含量较多的SiO2(其他成分不含Al和Si)。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4(霞石)、Na2SiO3和NaAlO2,有关化学方程式为:
Al6Si2O13 + 3Na2CO3 → 2NaAlSiO4+ 4NaAlO2 + 3CO2↑ ①
Al6Si2O13 + 5Na2CO3→ 2Na2SiO3 + 6NaAlO2 + 5CO2↑ ②
SiO2 + Na2CO3→ Na2SiO3 + CO2↑ ③
(1)粉煤灰中铝的质量分数为 % 。
(2)用1 mol Al6Si2O13 和 4 mol SiO2制得5mol NaAlO2、1mol NaAlSiO4,还应制得Na2SiO3____________mol,共消耗Na2CO3 mol(得到的固体中无SiO2)。
(3)若粉煤灰中 Al6Si2O13 与 SiO2的物质的量之比为1:2,则1kg粉煤灰与6mol Na2CO3反应(反应物全部都参与反应),可制得NaAlO2_________________mol。
(4)若用100 mol Al6Si2O13同时生产NaAlSiO4和NaAlO2,且n(NaAlSiO4):n(NaAlO2) = x,消耗Na2CO3 y mol,试确定y与x的关系式。
在下图转化关系中,固体甲的焰色反应呈黄色,M为常见的液体物质,酸G是重要的化工产品和化工原料;固体H能溶解在A溶液和酸G中,且H为良好的耐火材料(图中部分产物没有列出)。
(1)写出M和过量的固体甲反应的化学方程式:
(2)如图表示的是生产酸G的工业流程:
①设备乙的名称为 ;
②气体X的主要成分为 ;
③写出设备甲中常见的化学反应 ;
(3)固体乙与M反应的化学方程式为 。
无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业制备无水AlCl3的流程如下: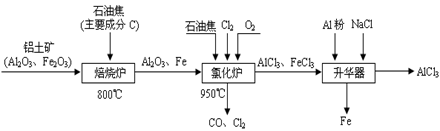
(1)已知:C(s)+O2(g)=CO(g);△H=-110.5kJ·mol-1 ①
2Fe(s)+O2(g)=Fe2O3(s) ;△H=-822.1kJ·mol-1 ②
请写出C还原Fe2O3生成CO的热化学方程式:
。
(2)氯化炉中通入O2的目的是 。
(3)氯化炉中Al2O3、C12和C反应的化学方程式是 。
(4)氯化炉中导出的气体,通常用亚硫酸钠溶液来吸收,请写出用Na2SO3溶液处理尾气时发生反应的离子方程式 。
(5)在升华器中加入铝粉的目的是 。
仔细阅读下图,已知B、D、E、F、G是氧化物,F、K是氢化物;C、H是日常生活中最为常见的金属单质,J是气态非金属单质,O是白色沉淀,且B、H、L、M、N、O中含有同种元素(图中部分反应物或产物已略去)。
请按要求回答:
(1)反应①既是分解反应,又是氧化还原反应,产物B、D、E、F的物质的量之比1:1:1:14。A强热分解的化学反应方程式为 。
(2)写出反应②在工业生产上的一种用途: 。
(3)反应③的离子方程式为 ;
反应④的化学方程式为 。
(4)常以C或H制成容器盛装和运输I的浓溶液,其原理是
。
 有关物质存在如图所示的转化关系(部分产物已省略)。通常
有关物质存在如图所示的转化关系(部分产物已省略)。通常为气体单质,
为紫黑色固体单质。实验室中,常用固体
在
的催化下加热制取气体单质
。




 请回答下列问题:
请回答下列问题:
 (1)反应①的化学方程式为
(1)反应①的化学方程式为
 (2)反应②的离子方程式为
(2)反应②的离子方程式为
(3)写出另外一种实验室制取的化学方程式
 (4)
(4)溶液与
溶液混合可形成沉淀,此沉淀的
=7.0×10-9。将等体积的
溶液与
溶液混合,若
的浓度为1×10-2
,则生成沉淀所需
溶液的最小浓度为。