关于溶液中微粒的浓度,下列说法正确的是
| A.0.1mol·L-1的(NH4)2SO4溶液中:c(SO42-) > c(NH4+) > c(H+) > c(OH-) |
| B.等浓度等体积的NaHSO3溶液与NaClO溶液混合后:c(Na+) + c(H+) = c(HSO3-) + c(ClO-) + c(SO32-) + c(OH-) |
| C.等浓度等体积的NaHCO3溶液与NaCl溶液混合后:1/2 c(Na+) = c(HCO3-) + c(CO32-) + c(H2CO3) |
| D.标况下,将2.24L SO2气体通入到100ml 1mol·L-1的NaOH溶液中,完全反应后溶液呈酸性,则该溶液中:c(Na+) > c(HSO3-) > c(SO32-) >c(H+) > c(OH-) |
下列溶液中有关微粒的物质的量浓度关系正确的是
| A.pH=4的0.1 mol·L-1的NaHC2O4溶液中:c(HC2O4-)>c (H2C2O4)>c(C2O42-) |
| B.0.1 mol·L-1的NaHCO3溶液中:c(OH-)=c(H+)+ c(HCO3-)+2c(H2CO3) |
| C.常温下,将醋酸钠、盐酸两溶液混合呈中性的溶液中:c(Na+)>c(Cl—)=c(CH3COOH) |
| D.常温下,等物质的量浓度的三种溶液:①(NH4)2SO4②NH4Cl③(NH4)2Fe(SO4)2中c(NH4+):①<②<③ |
在0.1 mol·L-1的NaHS溶液中,下列关系式正确的是
| A.c(Na+)=c(HS-)+2c(S2-)+c(H2S) |
| B.c(HS-)=c(Na+)+c(H+)-c(OH-)-c(S2-) |
| C.c(OH-)=c(H+)+c(H2S)+c(S2-) |
| D.c(H+)=c(OH-)+c(S2-)-c(H2S) |
归纳法是髙中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:(均在常温下)
①pH=1的强酸溶液,加水稀释后,溶液中离子浓度都降低。
②pH=2的盐酸和pH=l的盐酸,C(H+)之比为2 :1
③pH相等的三种溶液:a.CH3COONa b.NaHCO3 c.NaOH,其溶质物质的量浓度由小到大顺序为:c、b、a
④反应2A(s)+B (g)="2C" (g)+D (g)不能自发进行,则该反应△H一定大于0;
⑤已知醋酸电离平衡常数为Ka,醋酸根水解常数为Kb,水的离子积为Kw,则三者关系为:Ka•Kb=Kw
⑥若反应A(g)="2" B (g) 正反应的活化能为EakJ·mol-1,逆反应的活化能为EbkJ·mol-1,则△H=(Ea-Eb)kJ·mol-1
上述归纳正确的是
| A.全部 | B.③④⑤⑥ | C.②④⑤⑥ | D.①②④⑤ |
下列说法不正确的是
| A.25℃时,pH="11" NaOH溶液和pH="3" CH3COOH混合,若溶液显酸性,则所得溶液中离子浓度可能为c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| B.取c(H+)=0.01mol/L的盐酸和醋酸各100mL,分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大 |
| C.25℃时,某溶液中由水电离出的c(H+)=10-a mol/L,若a>7时,该溶液pH一定为14-a |
| D.含等物质的量的NaHC2O4和Na2C2O4的溶液中存在:2c(Na+)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
将体积为1mL,浓度为0.5mol/L的乙酸和体积为2mL,浓度为0.25mol/L的NaOH溶液混和,所得溶液中离子浓度由大到小的顺序是 ( )
| A.c(Na+)>c(CH3COO-)>c (OH-)>c(H+) |
| B.c(Na+)=c(CH3COO-),c(CH3COO-)>c (OH-)>c(H+) |
| C.c(Na+)> c (OH-) > c(CH3COO-) >c(H+) |
| D.c(Na+)> c (OH-) > c(H+)> c(CH3COO-) |
下列叙述错误的是 ( )
| A.把a L 0.1 mol/L 的CH3COOH溶液与b L 0.1 mol/L的 KOH溶液混合,所得溶 液中一定存在:c (K+)+ c (H+) =" c" (CH3COO-) + c (OH-) |
| B.氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-) |
| C.把0.1 mol/L 的NaHCO3溶液与0.3 mol/L 的Ba(OH)2溶液等体积混合,所得溶 液中一定存在:c (OH-) >c (Ba2+)>c (Na+)> c (H+) |
| D.常温下,在pH=3的CH3COOH溶液和pH=11的NaOH溶液中,水的电离程度相同 |
常温下,下列溶液中,有关微粒的物质的量浓度关系正确的是
| A.0.1 mol·L-1 (NH4)2Fe(SO4)2溶液: c(NH4+)> c(SO42-)>c(Fe2+)>c(H+) |
| B.0.1 mol·L-1 Na2CO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| C.等物质的量浓度的NH4HSO4、NH4Cl和NH4HCO3三种溶液中,pH大小:c (NH4HCO3) > c(NH4Cl) > c(NH4HSO4-) |
| D.0.01 mol·L-1NaOH溶液与等体积pH=2的醋酸混合后的溶液中:c (CH3COO-) > c (Na+) > c (H+)> c (OH-) |
室温时,向20mL 0.1mol·L-1的醋酸溶液中不断滴人0.1mol·L-1的NaOH溶液,溶液的pH变化曲线如图所示。在滴定过程中,关于溶液中离子浓度大小关系的描述不正确的是( )
| A.a点时:c( CH3COOH)>c( Na+)>c( CH3COO-)>c( H+)>c( OH -) |
| B.b点时:c( Na+) ="c(" CH3COO-)>c(H+)="c(" OH-) |
| C.c点时:c(H+)=c(CH3COOH) +c( OH-) |
| D.d点时:c(Na+)>c(CH3COO -)>c(OH-)>c(H+) |
常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是:
A.某HCl溶液的pH值为2,则溶液中由水电离的c(H+)=10-2mol•L-1
B.0.1 mol•L-1的KHA溶液,其pH=10, c(K+)>c(A2-)>c(HA-)>c(OH-)
C.等体积、等物质的量浓度的Na2CO3溶液与NaHCO3溶液混合:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
D.将0.2 mol•L-1的某一元酸HA溶液和0.1 mol•L-1NaOH溶液等体积混合后溶液pH>7,则反应后的混合液:c(HA)>C(Na+)>c(A-)
下列有关物质浓度关系的描述中,正确的是
| A.25℃时,NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-7mol·L-1 |
| B.25℃时,向0.1mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性: c(Na+)>c(NH4+)>c(SO42—)>c(OH—)=c(H+) |
| C.0.1mol·L-1的NaHCO3溶液中:c(OH-)+2c(CO32-)=c(H+)+c(H2CO3) |
| D.同温下,pH相同时,溶液物质的量浓度: |
c(CH3COONa)>c(NaHCO3)>c(C6H5ONa)>c(Na2CO3)
常温下,向20.00 mL 0.1000 mol·L—1 (NH4)2SO4溶液中逐滴加入0.2000 mol·L—1NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。下列说法正确的是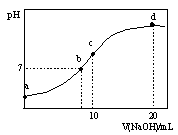
| A.点a所示溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-) |
| C.点c所示溶液中:c(SO42-)+ c(H+)= c(NH3·H2O )+ c(OH-) |
| D.点d所示溶液中:c(SO42-)>c(NH3·H2O )>c(OH-)>c(NH4+) |
25°C时,c(CH3COOH)+ c(CH3COO-)=0.1mol/L的醋酸、醋酸钠混合溶液中,c(CH3COOH)、 c(CH3COO-)与pH的关系如图所示。下列有关该溶液的叙述不正确的是
| A.pH=4的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| B.W点所表示的溶液中:c(Na+)+ c(H+)= c(CH3COOH)+c(OH-) |
| C.将W点所表示的1.0L溶液稀释到10L,用pH计测量,溶液的pH应为5.75 |
| D.pH=5.5的溶液中:c(Na+)+ c(H+)- c(OH-)+c(CH3COOH)=0.1mol/L |
已知常温下CH3COOH的电离平衡常数为Ka。常温下,向20 mL 0.1 mol/L CH3COOH溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化曲线如图所示(忽视温度变化)。下列说法中不正确的是
| A.a点表示的溶液中由水电离出的H+浓度为1.0×10-11 mol/L |
| B.b点表示的溶液中c(CH3COO-)>c(Na+) |
| C.c点表示CH3COOH和NaOH恰好反应完全 |
| D.当NaOH溶液加入20 mL时, c(CH3COO-) + c(CH3COOH)="c" (Na+) = 0.05mol/L(忽略混合时溶液体积的变化) |
下列微粒的浓度关系一定正确的是
| A.醋酸钠和醋酸的混合溶液中:c(CH3COO-)>c (Na+)>c(H+)>c(OH一) |
| B.常温下,物质的量浓度相等的①(NH4)2SO4、②(NH4)2Fe (SO4)2、③NH4HSO4、④NH4C1溶液中c(NH4+)的大小顺序为:②>①>③>④ |
| C.pH=3的盐酸与pH=ll的氨水等体积混合液中:c(H+)=c(OH一) |
| D.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH一)+c(HA一)+c(A2-) |