下列离子方程式正确的是
| A.电解氯化镁溶液:2Cl¯+ 2H2O ═ 2OH¯ + H2↑+ Cl2↑ |
| B.将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-═SO32-+2HClO |
| C.将少量CO2气体通入苯酚钠溶液中:2C6H5O- + CO2 + H2O→2C6H5OH +CO32- |
| D.硫酸亚铁酸性溶液中加入过氧化氢:2Fe2+ + H2O2 +2H+ = 2Fe3+ + 2H2O |
(12分)高氯酸钠可用于制备高氯酸。以精制盐水等为原料制备高氯酸钠晶体(NaClO4·H2O)的流程如下:
(1)由粗盐(含Ca2+、Mg2+、SO42-、Br-等杂质)制备精制盐水时需用到NaOH、BaCl2、Na2CO3等试剂。Na2CO3的作用是____________;除去盐水中的Br-可以节省电解过程中的电能,其原因是________________。
(2)“电解Ⅰ”的目的是制备NaClO3溶液,产生的尾气除H2外,还含有______________(填化学式)。“电解Ⅱ”的化学方程式为_____________________。
(3)“除杂”的目的是除去少量的NaClO3杂质,该反应的离子方程式为_______________________。“气流干燥”时,温度控制在80~100 ℃的原因是__________________。
下列离子方程式正确的是
| A.向碘化亚铁溶液中滴加溴的四氯化碳溶液2Br2+2Fe2++2I-=I2+4Br-+2Fe3+ |
| B.向含等物质的量浓度AgNO3和Cu(NO3)2的溶液中缓慢加入镁粉4Cu2++2Ag++5Mg=4Cu+2Ag+5Mg2+ |
| C.氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O |
| D.向0.3mol/LNaClO溶液中滴加等体积的0.2mol/LNaHSO3溶液: |
2HSO3-+4ClO-=2SO42-+2Cl-+2HClO
能正确表示下列反应的离子方程式的是
| A.Fe3O4溶于足量稀HNO3中:Fe3O4+8H+===Fe2++2Fe3++4H2O |
| B.NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-===BaCO3↓+H2O |
| C.将过量的SO2通入Ca(ClO)2溶液中: SO2+ClO-+H2O===HClO+ HSO3- |
| D.将0.2 mol·L-1 NH4Al(SO4)2溶液与0.3 mol·L-1 Ba(OH)2溶液等体积 |
混合:2Al3++3SO42-+3Ba2++6OH-===2Al(OH)3↓+3BaSO4↓
下列离子方程式书写正确的是
A.用Pt电极电解少量的MgCl2溶液:2H2O+2Cl- H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
| B.H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2↑ |
| C.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-= CaCO3↓+H2O |
| D.FeSO4溶液中加H2O2溶液:Fe2++2H2O2+4H+= Fe3++4H2O |
下列是某同学对相应的离子方程式所作的评价,其中评价合理的是
| 编号 |
化学反应 |
离子方程式 |
评 价 |
| A |
碳酸钙与醋酸反应 |
CO32-+2CH3COOH =CO2↑+H2O+2CH3COO- |
错误,碳酸钙是弱电解质,不应写成离子形式 |
| B |
NaAlO2溶液中通入过量CO2 |
2AlO2-+CO2+3H2O==2Al(OH)3↓+CO32- |
正确 |
| C |
NaHCO3的水解 |
HCO3-+H2O CO32-+H3O+ CO32-+H3O+ |
错误,水解方程式误写成电离方程式 |
| D |
等物质的量的FeBr2和Cl2反应 |
2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl - |
错误,离子方程式中Fe2+与Br-的物质的量之比与化学式不符 |
下列事实、离子方程式及其对应关系均正确的是
A.向Ag2S 浊液中滴加少量稀NaCl 溶液,黑色沉淀逐渐变成白色: Ag2S +Cl- AgCl +S2- AgCl +S2- |
| B.向K2Cr2O7 溶液中滴加少量浓H2SO4,溶液变为黄色: Cr2O72-(橙色) + H2O  2CrO42-(黄色) +2H+ 2CrO42-(黄色) +2H+ |
| C.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝: 4H+ + 4I- + O2= 2I2 + 2H2O |
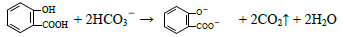
D.向水杨酸(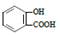 )中滴加NaHCO3溶液,放出无色气体: )中滴加NaHCO3溶液,放出无色气体: |
下表中评价合理的是
| 选项 |
化学反应及离子方程式 |
评价 |
| A |
Fe3O4与稀硝酸反应:2Fe3O4 + 18H+= 6Fe3++ H2↑+ 8H2O |
正确 |
| B |
向MgCO3中加入稀盐酸:CO32- + 2H+ ═ CO2↑+ H2O |
错误,MgCO3不应写成离子形式 |
| C |
向(NH4)2CO3溶液中加入Ba(OH)2溶液: Ba2++CO32-= BaCO3 |
正确 |
| D |
FeBr2溶液与等物质的量的Cl2反应: 2Fe2++ 2Br-+ 2Cl2 = 2Fe3++Br2+4Cl- |
错误,Fe2+与Br-的化学计量数之比应为1:2 |
近期发现, 是继NO、CO之后第三个生命体系气体信号分子,它具有参与调解神经信号传递、舒张血管减轻高血压的功能.回答下列问题:
(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是(填标号).
| A. | 氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以 |
| B. | 氢硫酸的导电能力低于相同浓度的亚硫酸 |
| C. | 的氢硫酸和亚硫酸的pH分别为4.5和2.1 |
| D. | 氢硫酸的还原性强于亚硫酸 |
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理.

通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为________、________,制得等量H 2所需能量较少的是________.
(3) 与 在高温下发反应:生 .在610k时,将 与 充入2.5L的空钢瓶中,反应平衡后水的物质的量分数为0.02.
① 的平衡转化率 =________%,反应平衡常数K=________.
②在620K重复试验,平衡后水的物质的量分数为0.03, 的转化率 ________ , 该反应的△H________0.(填">""<"或"=")
③向反应器中再分别充入下列气体,能使 转化率增大的是________(填标号)
| A. |
|
B. |
|
C. |
COS |
D. |
|
下列离子方程式与所述事实相符且正确的是( )
A.实验室用MnO2和浓盐酸制取Cl2:MnO2+4HCl(浓) Mn2++2Cl﹣+Cl2↑+2H2O Mn2++2Cl﹣+Cl2↑+2H2O |
| B.Ca(HCO3)2溶液中加入少量烧碱溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| C.向NaHSO4溶液中滴加Ba(OH)2溶液至呈中性:2H++SO42﹣+Ba2++2OH﹣=2H2O+BaSO4↓ |
| D.向次氯酸钠溶液中通入SO2:2ClO−+SO2+H2O=SO32-+2HClO |
海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

请填写下列空白:
(1)步骤①所需要的硅酸盐仪器是___________ ,步骤③的实验操作是___________。
(2)步骤⑤中,某学生选择用苯来提取碘水中的单质碘的理由是 _______ 。(选填序号)
a.单质碘与苯不发生化学反应 b.碘在苯中溶解度小
c.碘在苯中溶解度大 d.苯与水互不相溶
(3)提取碘的过程中,不能使用的有机溶剂是 ___ 。(选填序号)
a.酒精 b.汽油 c.四氯化碳
(4)步骤④中所发生的离子反应方程式 _____________。
(5)已知:2Fe3++2I-→2Fe2++I2 氯气既可以氧化Fe2+,也可以氧化I-。 往FeI2溶液中通入一定量的 Cl2,反应完成后,溶液中有1/2Fe2+被氧化,请写出该反应的化学反应方程式:__________。
现有下列十种物质:①液态氯化氢②小苏打 ③固体纯碱 ④二氧化碳⑤葡萄糖 ⑥氢氧化钾 ⑦氢氧化铁胶体 ⑧氨水 ⑨空气 ⑩硫酸铁溶液
(1)上述十种物质中,属于电解质的有 ,属于非电解质的有 。
(2)有两种物质在水溶液中可发生反应,离子方程式为:H++OH-=H2O,该反应的化学方程式为 。
(3)除去③中少量②的操作是 ,化学方程式为 。
(4)标准状况下,___________L ④中含有0.4mol 氧原子。
(5)现有100 mL⑩溶液中含Fe3+ 5.6g,则溶液中SO42-的物质的量浓度是 。
(6)若在⑦中缓慢加入⑥,产生的现象是 。
(7)将①加入到⑧中,⑧的导电能力变化为__________(填“增强”、“减弱”或“基本不变”)。
下列离子组中所给离子在水溶液中能大量共存,且当加入试剂后反应的离子方程式书写完全且正确的是
| 选项 |
离子组 |
加入试剂 |
发生反应的离子方程式 |
| A |
Fe3+、S2ˉ、Clˉ、Na+ |
NaOH溶液 |
Fe3++3OHˉ=Fe(OH)3↓ |
| B |
Na+、Al3+、Clˉ、SO42ˉ |
少量KOH溶液 |
Al3++3OHˉ=Al(OH)3↓ |
| C |
H+、Fe2+、SO42ˉ、NO3ˉ |
BaCl 2溶液 |
SO42ˉ+Ba2+=BaSO4↓ |
| D |
Na+、K+、ClOˉ、SO42ˉ |
通入少量SO2 |
2ClOˉ+SO2+H2O=2HClO+SO32ˉ |
I. 书写下列反应的化学方程式
(1) 用FeCl3溶液作为腐蚀液刻制铜印刷电路板 ;
(2) 工业上粗硅的制取:
II. 与量有关的离子方程式书写
(1) Ba(OH)2溶液与NaHSO4溶液反应后溶液呈中性:
离子方程式 ;
(2) Ca(HCO3)2溶液与少量NaOH溶液反应
离子方程式 ;
(3) Al2(SO4)3溶液与过量NaOH溶液反应
离子方程式 ;
(学法题)书写此类离子方程式的关键是: 。