甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成。甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子。A元素原子核内质子数比E的少l,D、E同主族。某同学为探究甲的组成而进行如下实验:

①取mg甲的晶体溶于蒸馏水,配成500 mL溶液;
②取少量甲溶液于试管中,逐滴滴入Ba(OH)2溶液,生成沉淀的物质的量与滴入Ba(OH)2溶液体积的关系如图所示;
③取20 mL甲溶液于试管中,加入过量NaOH溶液后加热并收集产生的气体,然后折算成标准状况下的体积为224 mL。
回答下列问题:
(1)D在元素周期表中的位置为_ 。
(2)经测定晶体甲的摩尔质量为453 g·mol-1,其中阳离子和阴离子物质的量之比为1:1。则晶体甲的化学式为_ _。
(3)图像中V(Oa):V(ab):V(bc)= _ 。
(4)写出ab段发生反应的离子方程式:_ 。
(5)配成的甲溶液物质的量浓度是_ 。
A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。试回答:
(1)E元素在周期表中的位置为 ,写出E的最高价氧化物与D的最高价氧化物的水化物反应的离子方程式 。
(2)由A、B、W三种元素组成的18电子微粒的结构简式为 。
(3)经测定A2W2为二元弱酸,其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式 。常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式 。
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式 。
(5)元素D的单质在一定条件下,能与A单质化合生成一种氢化物DA,熔点为800℃。DA能与水反应放氢气,若将1mol DA和1 mol E单质混合加入足量的水,充分反应后生成气体的体积是 L(标准状况下)。
有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:
| 元素编号 |
元素特征信息 |
| A |
A的单质是密度最小的物质 |
| B |
B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| C |
C的原子最外层电子数是其内层电子数的三倍 |
| D |
D与B同周期,该周期中D的简单离子半径最小 |
| E |
B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分 |
| F |
F元素最高正价与最低负价的代数和为4 |
(1)D的离子结构示意图是___________;化合物Y所含的化学键名称___________;B2C2的电子式表示为 。

(2)D、E、F的简单离子半径由大到小的顺序是(用化学式表示)________________。
(3)写出两种均含A、B、C、F四种元素的化合物在溶液中相互
反应的离子方程式 。
(4)将一定质量的Mg和D的混合物投入500mL稀硫酸中,
固体全部溶解并产生气体.待反应完全后,向所得溶液中加入
NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则固体混合物中Mg的质量为 ;原稀硫酸溶液的物质的量浓度为 。
原子序数依次增大的A、B、C、D、E五种短周期元素,可以两两形成多种原子个数比为1:1的化合物,其中的甲、乙、丙、丁4种化合物有两种属于离子化合物。A、B的原子序数之和是元素D的一半。B既是组成蛋白质的必要元素,也是某些化肥的组成元素。只有C为金属元素,焰色反应呈黄色。请回答下列问题:
(1)元素E 的原子结构示意图为 。
(2)B和D形成的化合物甲,其相对分子质量在170~190之间,且D的质量分数约为70%,则该化合物的化学式为 。
(3)A和B形成的化合物乙为B4A4,在一定条件下可以电离出两种离子,其中一种为10e-的离子,该物质一定条件下的电离方程式为 。
(4)化合物C2D溶液在空气中长期放置会变质生成丙C2D2,用化学方程式表示该过程 。
(5)D和E形成的化合物丁中所有原子均满足8电子稳定结构,该化合物的电子式为 ;该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,已知X是能使品红褪色的气体,Y在标准状态下的密度为1.63g/L,该混合气体相对于H2的密度为21,上述过程对应的化学方程式为 。
某研究小组同学为确定干燥的X和Y混合气体中Y 的存在,设计方案如下:把干燥的X和Y与干燥的NH3混合,出现白烟,则证明有Y气体,你认为此方案 (填“正确”或“不正确”),理由是 。
已知A、B、C、D、E、F、G是原子序数依次递增的短周期元素,已知A和D,C和F为同一主族元素,A与B、A与G形成共价化合物,B原子的最外层电子数比次外层多3,G元素的最高正化合价与最低负化合价的代数和为6,E是同周期中离子半径最小的元素,F形成的化合物是造成酸雨的主要原因。请回答下列问题:
(1)七种元素中,非金属性最强的元素在周期表中的位置是 。
(2)由C、D形成的一种淡黄色固体的电子式 。画出G离子的结构示意图 。
(3)G元素的单质有毒,可用D的最高价氧化物对应的水化物的溶液吸收,其离子方程式为 。
(4)将两份足量的E单质分别加入到等体积等浓度的硫酸和NaOH溶液中,充分反应生成的气体的体积比为 。
(5)由A、B、C所形成的常见离子化合物是 (写化学式),该化合物与D的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为 。
(6)已知一包白色晶体的混合物,经元素分析仪分析,包含以上七种元素中的若干种,为测定其组成,进行如下实验:
①称取固体2.37g溶于水,得到无色澄清溶液,再滴加过量的氯化钡溶液和稀盐酸,得到的白色沉淀经过滤、洗涤、干燥后,称得质量为4.66g
②再取等质量的该固体溶于水,逐滴滴加1mol/L的氢氧化钠溶液,得到的沉淀和滴加的氢氧化钠溶液体积的关系如图,该白色晶体的组成(用化学式表示)为 。

A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X; D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。请回答下列问题:
(1)X的名称为_________,A、C、D构成的化合物中含有的化学键有 。
(2)下列各项中,能说明元素C比E非金属性强的事实有____________(填序号)。
①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
④C与E组成化合物,C显负价
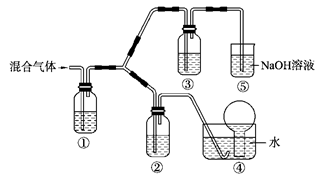
(3)将由BC和BC2组成的混合气体通入下图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强。
已知(ⅰ)浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC。
(ⅱ)NaOH溶液与BC2反应的化学方程式为:
 2NaOH+2BC2 NaBC2+NaBC3 + H2O, NaOH溶液与BC气体不反应。
2NaOH+2BC2 NaBC2+NaBC3 + H2O, NaOH溶液与BC气体不反应。
装置①、②、③中盛放的药品依次是______、______、 ______。
(4)通入混合气体之前,应先通入一段时间某另外一种气体,试推测先通入的该气体可以是______(填一种气体的化学式)。
有A、B、C、D、E、F六种元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D、F为常见金属元素。A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759 g·L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族。均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应,均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应。请回答下列问题:

(1)单质B的结构式:_____ ____。
(2)F元素周期表中的位置:_____ _____。
(3)均含有F元素的乙与丁在溶液中发生反应的离子方程式 。均含有D元素的乙与丁在溶液中发生反应的离子方程式_______ 。
(4)由A、C元素组成的化合物庚和A、E元素组成的化合物辛,相对分子质量均为34。其中庚的熔沸点比辛_________(填“高”或“低”),原因是___________________。
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属, K是一种红棕色气体。
请填写下列空白:
(1)在周期表中,组成单质I的元素位于第__________周期_________族。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为___________________。
(3)在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是__________(填序号)
(4)反应④的离子方程式是__________________________________。
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是 _________________________。
A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为 。
(2)由A、B、W三种元素组成的18电子微粒的电子式为 。
(3)经测定A2W2为二元弱酸,其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式 ,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式 。
(4)废印刷电路反上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式 。
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,DA能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是 。(标准状况下)。
(6)D的某化合物呈淡黄色,可与氯化亚铁溶液反应。若淡黄色固体与氯化亚铁反应的物质的量之比为1:2,且无气体生成,则该反应的离子方程式为 。
有A、B、C、D、E、F六种元素,原子序数依次增大,A、B、C、D、E均为短周期元素,A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g•L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族.均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应:均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应.
请回答下列问题:
(1)单质B的结构式:________________________。
(2)F元素周期表中的位置:_______________________。
(3)均含有F元素的乙与丁在溶液中发生反应的离子方程式___________________;均含有D元素的乙与丁在溶液中发生反应的离子方程式________________________。
(4)由A、C元素组成化合物良和A、E元素组成的化合物辛,式量均为34.其中庚的溶沸点比辛_______(填“高”或“低”),原因是_________________。
Ⅰ.A、B、C、D、E、F是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分反应条件略去):

(1)若所有转化都是非氧化还原反应,B、D、E含有同种金属元素,F为强碱(部分产物略去)则B+D→E的离子方程式为________________,C为同周期元素构成的1:1型化合物,则C的电子式为___________________。
(2)若A、D、F为单质,B、C、E为化合物,B为两种非金属元素所组成的化合物,则E的化学式为___________,A+B→C+D的化学方程式为______________________。
Ⅱ.亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取来氯酸钠的工艺流程:

已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用 ②ClO2气体在中性和碱性溶液中不能稳定存在。
(1)反应生成ClO2气体需要X酸酸化,X酸可以为_______________。
A.盐酸 B.稀硫酸 C.硝酸 D.H2C2O4溶液
(2)吸收塔内的温度不能过高的原因为__________________________。
(3)ClO2被S ClO2被S2-还原为ClO2-、Cl-转化率与pH关系如图。

写出pH≤2时ClO2与S2-反应的离子方程式:_______________。
A、B、C、D、E、F六种物质在一定条件下有如下图所示的相互转化关系。
(1)若下列反应①为不同短周期、不同主族元素间置换反应,A、D为固体单质,其中D为非金属。则反应①的化学方程式为

(2)若下列反应②中E为一种一元强碱, C的大量排放产生温室效应。则在反应②中,若C、E的物质的量之比为11:17,则反应的离子方程式为

(3)若下列反应③中B为一种淡黄色固体,绿色植物的光合作用和呼吸作用可实现自然界中E的循环。则B的电子式为 反应③的化学方程式为

A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题: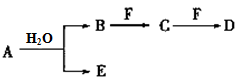
(1)若常温下A为有色气体。
①当F是一种金属单质时,请写出一定浓度的B溶液和适量F反应生成C与气体E的离子方程式:________________。
②当C是一种产生温室效应的气体分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为_________;D中所含化学键的类型______________。
(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的式量相等。
①用离子方程式表示F的水溶液呈酸性的原因__________________。
②A可由对应的单质直接化合生成,生成39gA时,放出255.5kJ的热量,写出该反应的热化学方程式_____________。
(3)若A中一种元素原子的最外层电子数为内层电子总数的1/5 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:____;B转化为C的化学方程式为_______________。
甲、乙、丙三种物质均由短周期元素组成,一定条件下,存在下列转化关系:甲+乙→丙+H20
(1)若丙为Na2C03,反应的化学方程式为 (任写一个)。 溶液中,所含的离子按物质的量浓度由大到小的顺序排列为 。
溶液中,所含的离子按物质的量浓度由大到小的顺序排列为 。
(2)若甲是石油裂解气的主要成分之一,乙为O2,且甲分子和乙分子具有相同的电子数。25℃、101 kPa时,1g甲完全燃烧生成CO2气体与液态水,放出50.5 kJ的热量,该反应的热化学方程式为 ;利用该反应设计的燃料电池中,通入甲的电极为电池的 (填“正极”或“负极”)。
(3)若甲、乙是同主族元素的化合物,丙为单质。
①丙所含元素在元素周期表中的位置为 ;
②甲与水相比,热稳定性较强的是 (填化学式)。
甲、乙、丙、丁四种短周期元素可以组成下列框图中除Br2和L以外的物质,其原子序数依次增大。甲和乙可形成常见液态化合物K,固体A中含有丙元素的正一价阳离子,其电子层结构与氖原子相同,丁元素原子的最外层电子数是其电子层数的2倍。在一定条件下,下列各物质可发生如图所示的变化(反应中生成的水没有写出):
试回答:
(1)A的电子式为 ;所含化学键类型为 ;A晶体的晶胞中阳离子和阴离子的个数比为 。
(2)溴元素在周期表的位置 丁元素的阴离子结构示意图为 。
(3)甲、乙、丙、丁四元素的离子半径由大到小的顺序为(用离子符号表示) ;甲、乙、丙、丁四元素的第一电离能由大到小的顺序为(用元素符号表示) 。
(4)F分子的空间构型为 ;H分子的空间构型为 ;