湖北省孝感高中高二上学期9月调研考试化学试卷
化学与生产、生活、社会密切相关。下列有关说法中,错误的是
| A.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 |
| B.血液透析是利用了胶体的性质 |
| C.在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
| D.点燃爆竹后,硫燃烧生成SO3 |
下列有关化学用语使用正确的是
A.硫离子(S2‾)结构示意图: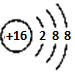
B.NH4Cl的电子式: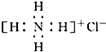
C.原子核内有8个质子、10个中子的氧原子: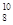 O
O
D.H、D、T互为同素异形体
下列有关性质的比较,不能用元素周期律解释的是
| A.酸性:H2SO4>H3PO4 | B.非金属性:Cl>Br |
| C.碱性:NaOH>Mg(OH)2 | D.热稳定性:Na2CO3>NaHCO3 |
下列实验过程中,始终无明显现象的是
| A.NO2通入FeSO4溶液中 |
| B.CO2通入CaCl2溶液中 |
| C.SO2通入已酸化的Ba(NO3)2溶液中 |
| D.NH3通入AlCl3溶液中 |
下列各组数据中,前者刚好是后者两倍的是
| A.2 mol水的摩尔质量和1 mol水的摩尔质量 |
| B.200 mL 1 mol/L氯化钙溶液中c(Cl-)和100 mL 2 mol/L氯化钾溶液中c(Cl-) |
| C.64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数 |
| D.20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度 |
关于Na2CO3和NaHCO3比较中,下列说法不正确的是
| A.NaHCO3固体受热容易分解,而Na2CO3固体受热不容易分解 |
| B.等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,前者消耗盐酸的物质的量比后者多 |
| C.等物质的量浓度的Na2CO3和NaHCO3溶液分别滴加2滴酚酞试液,前者颜色比后者深 |
| D.Na2CO3溶液和NaHCO3溶液分别与Ba(OH)2溶液反应的离子方程式相同[来源 |
下列离子方程式正确的是
| A.向硫酸铝溶液中滴加过量的氨水:Al3++ 4OH‾═ AlO2‾+ 2H2O |
| B.金属铜与浓硝酸反应:3Cu+8H++2NO3‾═3Cu2++2NO↑+4H2O |
C.实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl‾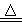 Cl2↑+Mn2++H2O Cl2↑+Mn2++H2O |
| D.向NaAlO2溶液中通入过量CO2气体:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
NA表示阿伏加德罗常数,下列说法正确的是
| A.46gNO2和N2O4的混合气体中,含氮原子数目是NA |
| B.1.0L 0.1mol/L的NaF溶液中,含F-离子数目是0.1NA |
| C.11.2L的H2中,含有的电子数目是NA |
| D.1molFeCl3跟沸水完全反应转化为氢氧化铁胶体,其中胶体粒子的数目是NA |
下列关于物质或离子检验的叙述正确的是
| A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ |
| B.气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气 |
| C.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+ |
| D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2 |
某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是
| A.AlCl3 | B.Na2O | C.FeCl2 | D.SiO2 |
在新制的氯水中加入少量的碳酸钠粉末,下列说法正确的是
| A.pH减小,HClO浓度减小 | B.pH减小,Cl-浓度增大 |
| C.pH增大,Cl-浓度减小 | D.pH增大,HClO浓度增大 |
下列有关溶液组成的描述合理的是
| A.无色溶液中可能大量存在Al3+、NH4+、Cl‾、S2- |
| B.酸性溶液中可能大量存在Na+、ClO‾、SO42-、I‾ |
| C.弱碱性溶液中可能大量存在Na+、K+、Cl‾、HCO3‾ |
| D.中性溶液中可能大量存在Fe3+、K+、Cl‾、SO42‾ |
下列有关试剂的保存方法正确的是
①NaOH固体保存在配有橡皮塞的细口瓶中;
②Na2CO3溶液通常保存在配有橡皮塞的细口瓶中;
③液溴通常用水封保存;
④锂保存在煤油中;
⑤浓硝酸通常保存在棕色细口瓶中
| A.①③⑤ | B.②③⑤ | C.②④⑤ | D.①③④ |
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)= K2S(s)+N2(g)+3CO2(g) ΔH=" x" kJ·mol-1
已知:碳的燃烧热 ΔH1=" a" kJ·mol-1
S(s)+2K(s)= K2S(s) ΔH2=" b" kJ·mol-1
2K(s)+N2(g)+3O2(g)= 2KNO3(s) ΔH3=" c" kJ·mol-1
则x为
| A.3a+b-c | B.c +3a-b | C.a+b-c | D.c+a-b |
在一密闭容器中,mA(g)+bB(g)⇌pC(g)反应平衡时,测得 c(A)为 0.5mol•L‾1,在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得 c(A)为 0.3mol•L‾1,则下列判断中正确的是
A.平衡向正反应方向移动 B.物质C的质量分数增加
C.化学计量数:m+b<p D.物质B的转化率减小
下列指定条件下的结果正确的是
A.0.1mol·L‾1氨水中,c(OH‾)=c(NH4+)
B.10mL 0.02mol·L‾1HCl溶液与10mL 0.02mol·L‾1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=7
C.在0.1mol·L‾1 CH3COONa溶液中,c(OH‾)=c(CH3COOH)+c(H+)
D.0.1mol·L‾1某二元弱酸盐NaHA溶液中,c(Na+)=2c(A2‾)+c(HA‾)+c(H2A)
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题: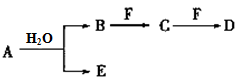
(1)若常温下A为有色气体。
①当F是一种金属单质时,请写出一定浓度的B溶液和适量F反应生成C与气体E的离子方程式:________________。
②当C是一种产生温室效应的气体分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为_________;D中所含化学键的类型______________。
(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的式量相等。
①用离子方程式表示F的水溶液呈酸性的原因__________________。
②A可由对应的单质直接化合生成,生成39gA时,放出255.5kJ的热量,写出该反应的热化学方程式_____________。
(3)若A中一种元素原子的最外层电子数为内层电子总数的1/5 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:____;B转化为C的化学方程式为_______________。
乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4·xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定。学习小组的同学设计了滴定的方法测定x值。
①称取2.520 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4。
③用浓度为0.100 0 mol·L-1的KMnO4标准溶液进行滴定,达到终点时消耗20.00 mL。
(1)写出草酸(H2C2O4)与酸性高锰酸钾溶液反应的化学方程式____________。
(2)滴定时,将酸性KMnO4标准液装在如图中的________(填“甲”或“乙”)滴定管中。
(3)本实验滴定达到终点的标志是__________。
(4)通过上述数据,求得x=________。
讨论:①若滴定终点时仰视滴定管刻度,则由此测得的x值会_______(填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会________。
一定温度下,在容积固定的V L密闭容器中加入n mol A、2n mol B,发生反应:A(g)+2B(g) 2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
(1)一段时间后上述反应达到平衡。则下列说法中正确的是________(填字母)。
A.物质A、B的转化率之比为1∶2
B.起始时刻和达到平衡后容器中的压强之比为3n∶(3n-nx)
C.充入惰性气体(如Ar),平衡向正反应方向移动
D.当2v正(A)=v逆(B)时,反应一定达到平衡状态
(2)K和x的关系满足K=____________。
(3)该反应的逆反应速率与时间的关系如图所示。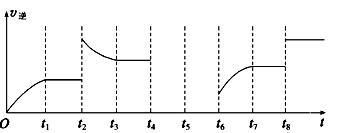
①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的条件:
t2时_________________________;
t8时_________________________。
②t2时平衡向__________(填“正反应”或“逆反应”)方向移动。
③若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线。
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH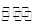 CH3COO‾+H+ ΔH>0。
CH3COO‾+H+ ΔH>0。
(1)常温常压下,在 pH =5的稀醋酸溶液中,c(CH3COO‾)=__________;下列方法中,可以使0.10 mol·L‾1CH3COOH的电离程度增大的是___________。
a.加入少量0.10 mol·L‾1的稀盐酸
b.加热CH3COOH溶液
c.加入少量冰醋酸
d.加水稀释至0.010 mol·L‾1
e.加入少量氯化钠固体
f.加入少量0.10 mol·L‾1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)______V(醋酸),反应的最初速率为:υ(盐酸)_____υ(醋酸)。
(3)常温下,向体积为Va mL pH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与Vb的关系是:Va____Vb;溶液中各离子的浓度按照由大到小排序为___________。
(4)已知:90℃时,水的离子积常数为Kw = 38×10‾14,在此温度下,将pH=3的盐酸和pH = 11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=____________(保留三位有效数字)。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号