下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:① ________,⑤ ________,⑦ ________。
(2)画出原子的结构示意图:④________,⑥ ________,⑧________。
(3)在这些元素中,最活泼的金属元素是________,最活泼的非金属元素是________,最不活泼的元素是________。
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是________,碱性最强的是________,呈两性的氢氧化物是________。
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
X溶液与Y溶液反应的离子方程式为___________________________________,
N→⑥的单质的化学方程式为______________________________________________,
(6)在③与④中,化学性质较活泼的是________,怎样用化学实验证明?
答:____________________________________________________________;
在⑧与⑫中,化学性质较活泼的是________,请用化学方程式来说明。
答:___________________________________________________________。
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A是地壳中含量最高的元素,B、C、D同周期,E和其他元素既不在同周期也不在同主族,D的氢化物和最高价氧化物的水化物均为强酸,且B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。据此回答下列问题:
(1)写出A单质的结构式___________。B的最高价氧化物的水化物的电子式__________。
(2)用电子式表示B2A的形成过程:__________________________________。
(3)A和D的氢化物中,沸点较高的是__________(写出化学式)。
(4)写出E离子的离子结构示意图__________。元素D在元素周期表中的位置是______________。
(5)A、D、E可以形成多种盐,其中一种盐中A、D、E三种元素的原子个数比为2:2:1,该盐的名称为 _________。它的水溶液与D的氢化物的水溶液反应可生成D的单质,该离子方程式为____________。
下表列出了A~M 13种元素在周期表中的位置:
| 族 周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
| 1 |
A |
|
|
|
|
|
|
|
| 2 |
|
|
|
B |
C |
D |
E |
|
| 3 |
F |
G |
H |
|
|
I |
J |
K |
| 4 |
L |
M |
|
|
|
|
|
|
(1)这些元素中,金属性最强的元素是___________(填元素名称),非金属性最强的元素是________(填元素名称),最不活泼的元素是________(填元素符号),原子半径最小的元素是_______(填元素符号)。
(2)写出C元素的气态氢化物与I元素的最高价氧化物的水化物反应的化学方程式:______________。
(3)将C、D、E三种元素的氢化物按还原性增强的顺序排列为________。(用化学式表示)
(4)I2—、J-、L+、M2+等微粒中,半径最大的是_________(填离子符号)。
(5)A与D形成的化合物A2D2是______化合物(填共价或离子),其电子式为__________。
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10,X和Ne的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的吸引电子的能力在同周期主族元素中最大。请回答下列问题:
(1)X元素位于元素周期表中位置是 ;
(2)Z的气态氢化物和溴化氢相比,较稳定的是 (写化学式)
(3)用元素符号将W、X、Y按照原子半径由大到小的顺序排列出来
(4)X的一种氧化物与W的氢化物反应能够生成W的单质,该氧化物中含有化学键的类型是 。
A、B、C、D、E、F六种短周期元素,且原子序数逐渐增大。已知:A、C、F三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应。D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。回答下列问题:
(1)写出D的元素名称 ,D的气态氢化物的化学式 E的最高价氧化物的水化物的化学式 。
(2)画出B元素的离子结构示意图 。
(3)若构成F元素的一种核素的中子数为18,写出该核素的表示符号 。
(4)C与F元素最高价氧化物的水化物反应的离子方程式为 。
(5)将A、C、F的简单离子按照半径由大到小的顺序排列 (用离子符号表示)

(1)在上面元素周期表中的A、B、、C、D四个区域中,全部是金属元素的区域为 。
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素,金属性较强的是 (填名称),能验证该结论的实验是 (填编号)
a.将在空气中放置已久的这两种元素的块状单质分别放入热水中
b.将这两种元素单质的粉末分别和同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性
元素X、Y、Z、W、M、N原子序数依次增大,X与M、W与N分别同主族,且元素X、Y、Z、W分属两个短周期,它们四者原子序数之和为22,最外层电子数之和为16,在化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构,请回答下列问题:
(1)Y元素在周期表中的位置是__________________________,X、Y、Z、W、M的原子半径由大到小的顺序为:_______________(用元素符号表示)。
(2)写出Y2X2的电子式____________;Z2X4结构式 _______________。
(3)X、Z、W形成的化合物,水溶液一定显酸性的盐是______________,其原因是_____________(用离子方程式表示),该物质所含化学键的类型是_____________。
(4)均含X、W、M、N四种元素的两种化合物相互反应有刺激性气味气体放出,反应的离子方程式为_______________。
(5)火箭发动机曾经利用Z2X4作燃料X2W2作助燃剂,产物环保无污染,写出二者反应的方程式___________________。
(6)写出N W2通入硝酸钡溶液中的离子方程式 ______________。
X、Y、Z、W、E五种短周期元素在元素周期表的位置如图。其中W的原子序数是Y的2倍。
(1)能证明X、Z两元素非金属性强弱的离子方程式为
(2)一定条件下,在恒容容器中,充人一定量的WY2 (g)和XY (g),发生反应: 时,各物质的平衡浓度如下表:
时,各物质的平衡浓度如下表:
①若温度升高到 T2℃时,反应的平衡常数为6.64,则该反应的逆反应为______反应(填“吸热”或“放热”)。
②其他条件不变,若该反应在恒压条件下进行,平衡时XY的转化率a2______a1(T1℃时的转化率)(填“<”“>”“=”)
(3)室温下,Mg(OH)2饱和溶液______(填“能”或“不能”)使石蕊试液变蓝,通过计算说明原因(已知: 。答
。答
(4)化学反应 在工业生产中有重要的地位,若要提高E2的转化率,可采取的措施是______(填字母代号)
在工业生产中有重要的地位,若要提高E2的转化率,可采取的措施是______(填字母代号)
a.升高温度 b.加催化剂 c.增加H2的浓度 d.分离出EH3
一定条件下,1mol E2与3molH2在密闭容器中反应达到平衡,E2的转化率为25%且放出23.lkJ能量,则该条件下反应的热化学反应方程式为____________________.
(5)电化学降解法可用于治理水中硝酸盐的污染,其原理如图所示。其中B为电源的______极,其电极反应式为______。
【原创】甲、乙、丙、丁、戊、己是六种短周期元素,原子序数依次增大。甲、乙两元素最高正价与最低负价之和均为0;戊与甲同主族;丁、己分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)丁在元素周期表中的位置为________________。
(2)六种元素原子半径由大到小的顺序是(写元素符号)_________________________。
(3)甲和戊的化合物的电子式为___________;甲和戊化合物与水反应放出气体的化学方程式为____________。
(4)甲、丁两元素能形成两种化合物的电子式分别为 和 。
(5)甲和丙的单质在一定条件下反应生成物质庚,化学方程式为:______________。
(6)己的氧化物和戊的最高价氧化物对应的水化物反应的化学方程式是__________________。
(6分,每空1分)已知A、B、C、D均为短周期元素,它们的原子序数依次递增。 A是最外层为一个电子的非金属元素,C 原子的最外层电子数是次外层的3倍; C和D可形成两种固态化合物,其中一种为淡黄色固体;B和C可形成多种气态化合物。A、B、C三种元素可以形成离子晶体,该晶体中各元素原子的物质的量之比为A:B:C=4:2:3。
请回答下列问题:
(1)写出B的原子结构示意图 ,写出C和D形成的淡黄色固体化合物的电子式 。
(2)元素原子的物质的量之比为A:B:C="4:2:3" 的晶体名称为 。
(3)请写出与A2C和BA3分子中电子数相同,且仍由A、B、C元素中任意两种元素组成的微粒的符号(举两例) 、 。
(4)写出由B、C元素组成且元素原子质量比为B:C=7:12的化合物的化学式 。
I.有X、Y、Z、R四种短周期元素,Y、Z、R同周期。相关信息如下:
| |
相关信息 |
| X |
单质为双原子分子。若低温蒸发液态空气,因其沸点较低可先获得X的单质 |
| Y |
含Y元素的物质焰色反应为黄色 |
| Z |
同周期元素中原子半径最小 |
| R |
R元素原子的最外层电子数是K层电子数的3倍 |
(1)Z元素在周期表的位置是 ,Y、Z、R简单离子的半径从大到小的顺序是 (用离子符号表示);
 (2)由X、Z两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子里X、Z两种原子最外层均达到8个电子的稳定结构。甲遇水蒸气可形成一种常见的漂白性物质。则甲的结构式为 ;
(2)由X、Z两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子里X、Z两种原子最外层均达到8个电子的稳定结构。甲遇水蒸气可形成一种常见的漂白性物质。则甲的结构式为 ;
(3)化合物乙(Y2R)溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Y2R2,其溶液显黄色。则Y2R2的电子式为 ,写出乙溶液在空气中变质过程的化学方程式 。
II.元素X与氢可形成多种化合物,如丙、丁、戊。
(4)丙与醋酸类似,为一元弱酸,对热十分稳定但受撞击就爆炸。8.6 g丙爆炸分解生成H2和6.72 L(标况下)X2。写出其爆炸的化学方程式 ;
(5)丁为离子化合物,遇水反应生成H2和气体戊,标况下戊的密度为0.76 g·L-1,则物质丁的化学式为 ;
(6)戊在高温条件下能还原Fe2O3,生成两种单质,写出该反应的化学方程式 ,有人提出生成的产物中可能还有FeO,请设计实验方案验证(用化学方法) 。
(Ⅰ)短周期元素X、Y、Z、W原子序数依次增大,X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中,请回答:
(1)X在元素周期表中的位置是 ;Y氢化物的电子式 。
(2)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈 。(填“酸性”、“碱性”或“中性”),用离子方程式表示其原因是 。
(3)Y-AgO电池是应用广泛的鱼雷电池,其原理如图所示,该电池的负极反应式 。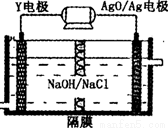
(4)由Z和W组成的化合物遇水立即水解产生两种酸,写出此反应的化学方程式 。
(Ⅱ)A、B、C分别是由H、C、O、N、Na、Cu六种元素中的两种或多种元素组成的化合物。现对A、B、C三种化合物分别做以下实验:
A是一种蓝色固体,B是无色晶体,其式量为68,C是白色固体,分别取A、B、C三种物质少量于三支试管中,加适量水溶解,发现A不溶于水,B、C都能溶于水,并且用pH试纸测定,B与C的水溶液都显碱性。
(1)取A物质少量于一支试管中,后加适量稀盐酸溶解,并用酒精灯微热,发现固体溶解时,伴有气泡产生。将56.8gA隔绝空气加热分解生成40g黑色固体X、无色酸性气体Y(标准状况下,密度为1.96g/L)和水,生成的Y折合成标准状况下的体积为6.72L,则A的化学式为 。
(2)取B的水溶液2ml与新制Cu(OH)2混合加热,发现能出现砖红色沉淀,则物质B为 。
(3)取16.8gC固体加强热,将生成的气体依次通过经称量过的装CaCl2固体的干燥管和装足量Ba(OH)2水溶液的洗气瓶,后经再次称量发现干燥管增重1.8g,洗气瓶增重4.4g。写出C物质加入水后的溶液显碱性的原因 。(用离子方程式和必要文字解释)
A、B、C、D、E五种短周期元素,A与D同周期,A的单质既可与盐酸反应,又可与NaOH溶液反应,B的单质在放电条件下能与氧气反应,C元素的离子不含电子,D元素原子的最外层电子数是其次外层电子数的3/4,E元素原子的最外层电子数是其次外层电子数的3倍。
(1)A的原子结构示意图为 。
(2)0.1 mol/L A的硫酸盐溶液与0.1 mol/L NaOH溶液等体积混合,反应的离子方程式为 。
(3)以A的单质和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池总反应的化学方程式是 。
(4)化合物甲由元素A、B组成,具有良好电绝缘性。化合物甲能与水缓慢反应生成含B的化合物乙,乙分子中含有10个电子。写出该反应的化学方程式: 。工业用A的单质和化合物乙在高于1700K反应制备甲。已知该反应可以认为是置换反应,该反应的化学方程式是 。
(5)D和E两种元素相比较,非金属性较强的是(填元素名称) ,可以验证该结论的是(填写编号) ;
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
(6)C、D、E间可形成丙、丁两种分子,它们均含有18个电子,则丙与丁反应生成D单质的化学方 程式为 ;
已知甲、乙、丙分别代表中学化学中的常见物质,请根据题目要求回答下列问题:
Ⅰ.若甲的化学式为RCl3,其溶液在加热蒸干并灼烧时可发生反应:
a.甲+H2O 乙+丙
乙+丙
b.乙 氧化物+H2O
氧化物+H2O
①若甲为某用途广泛的金属元素的氯化物,其溶液在上述变化中生成的氧化物为红棕色粉末,则甲发生a反应的化学方程式为: ;
②若甲为某短周期金属元素的氯化物,则该金属在周期表中的位置是: ;
若向30 mL 1 mol/L的甲的溶液中逐渐加入浓度为4 mol/L的NaOH溶液,若产生0.78 g白色沉淀,则加入的NaOH溶液的体积可能为 (选填编号).
| A.3 mL | B.7.5 mL | C.15 mL | D.27.5 mL |
③将以上两种金属单质用导线连接,插入一个盛有NaOH溶液的烧杯中构成原电池,则负极发生的电极反应为 。
Ⅱ.若甲,乙、丙均是短周期中同一周期元素形成的单质或化合物,常温下乙为固体单质,甲和丙均为气态化合物,且可发生反应:甲+乙 丙。则:
丙。则:
①写出上述反应的化学方程式 。
②0.5 mol气体甲与足量的过氧化钠反应,转移电子的数目为 。
③将一定量气体甲通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(甲)的关系如图所示,溶液A中各离子浓度由大到小的顺序为 。

【改编】SO2、NOx、CO2是对环境影响较大的气体,控制和治理SO2、NOx、CO2是减少酸雨、光化学烟雾和解决温室效应的有效途径。
(1)碳元素在元素周期表的位置: 。
(2)标况下2.24LSO2恰好被1L 0.2mol·L-1的NaOH溶液完全吸收,请写出吸收后溶液中离子浓度由大到小的顺序为 。
(3)已知汽车尾气NO与CO净化反应生成无污染气体,3g NO参加该反应放出37.99 kJ热量,请写出该反应的热化学方程式: 。
(4)某科研小组想以如图所示装置用原电池将 SO2转化为重要的化工原料。
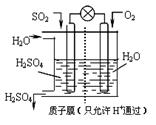
①其负极反应式: ,
②当有1mol SO2被吸收,则通过质子(H+)交换膜的H+离子数为 。
(5)某科研小组用CO2通过下面反应方程式来生产甲醇,
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH= —49.0kJ·mol-1
CH3OH(g)+H2O(g) ΔH= —49.0kJ·mol-1
现将6molCO2和8molH2充入一容积为2L的恒温密闭容器中,测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标)。
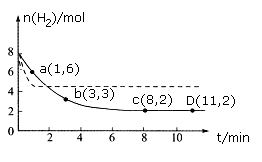
回答下列问题:
①此温度下该反应的平衡常数的数值K= 。
②仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比,虚线改变的条件可能是 。