月球表面土壤里有一种非常有用的资源——He,它是可控核聚变的原料,关于He的叙述正确的是
| A.3He和4He是同种原子 |
| B.3He和4He互为同位素 |
| C.核聚变时,原子核发生了变化,发生了化学反应 |
| D.在3He中存在:质子数=中子数=核外电子数 |
运用元素周期律研究元素及其化合物的性质具有重要的意义。
I.部分短周期主族元素的最高价氧化物对应的水化物(浓度均为0.01mol.L-1)溶液的PH和原子序数的关系如下图所示。

(1)元素R在周期表中的位置是 。
(2)元素Y和W形成的Y2W2型化合物中含有化学键的类型为 。
(3)测定Z元素最高价氧化物对应水化物溶液物质的量浓度的方法为 。
II.短周期元素C、O、S能形成多种化合物,如CO2、CS2、COS等
(1)下列能说明碳、硫两种元素非金属性相对强弱的是 (填序号)
A.相同条件下水溶液的PH:Na2CO3 >Na2SO4
B.酸性:H2SO3 >H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和CO2相似
①羰基硫(COS)的电子式为: 。
②羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下:

已知A是一种正盐,则A的化学式为 ;若气体a为单质,反应 II的离子方程式为 。
在通常情况下,稀有气体很难与其他元素发生化学反应,其原因是
| A.稀有气体最外层电子数均为8个,很稳定 |
| B.稀有气体的电子层数比较多,很稳定 |
| C.稀有气体的最外层电子数均达到稳定结构 |
| D.稀有气体的原子核所带电荷较多 |
下列有关化学用语表示正确的是
A.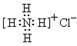 :可以表示氯化铵的电子式 :可以表示氯化铵的电子式 |
B. :可以表示中子数为18的氯原子结构示意图 :可以表示中子数为18的氯原子结构示意图 |
C.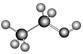 :可以表示乙醇分子的球棍模型 :可以表示乙醇分子的球棍模型 |
D. :既可以表示甲烷分子,也可以表示四氯化碳分子 :既可以表示甲烷分子,也可以表示四氯化碳分子 |
在多电子原子中,轨道能量是由以下哪些因素决定( )
①能层 ②能级 ③电子云的伸展方向 ④电子自旋状态
| A.①② | B.①②④ | C.①②③ | D.①③④ |
下列说法正确的是
| A.用核磁共振氢谱不能鉴别1-丙醇和2-丙醇 |
B.实验证实 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 |
C. 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 |
D. 的单体是CH3-C≡C-CH3和CH2=CH-CN 的单体是CH3-C≡C-CH3和CH2=CH-CN |
短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X原子核外最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z、W是常见金属,Z的氧化物可做耐火材料,W的简单离子是同周期中离子半径最小的,Q的p能级上有一个未成对电子.试回答下列问题:
(1)比较第一电离能:Z_________W(填“>”、“<”或“=”,后同);电负性:X________Y。
(2)写出Q的价电子排布图_____________,YF3的结构式_____________,
(3)向硫酸铜溶液中逐滴滴入Y的氢化物的水溶液至过量,用离子方程式表示该过程出现的现象变化:答:________________________________________。
下列说法正确的是
| A.熔点:Na-K合金<Na<氯化钠 |
| B.非金属氢化物的稳定性顺序:H2O>H2S>H2Se,HCl<H2S<PH3 |
| C.CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应只生成Na2SO3和O2 |
| D.同一原子中,2p、3p、4p能级的轨道数依次增多 |
A、B、C、D均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为19。下列说法正确的是( )
A.单质的沸点:A>B B.B与C不能存在于同一离子化合物中
C.氧化物的水化物的酸性:C<D D.阴离子的半径:C>D
填空题
(1)碳原子最外电子层含有__________个电子,一个碳原子可以跟其他非金属原子形成__________共价键。
(2)在有机合成过程中,引入碳碳双键的三种方法是_____________、________________、_____________。
(3)根据官能团不同,单糖可分为_______________和________________________。
(4)核酸分为DNA和RNA,DNA的主要功能是________________;RNA的主要功能是____________。
卤族元素的单质能与H2反应
| H2+F2=2HF |
在暗处能剧烈化合并发生爆炸 |
| H2+Cl2=2HCl |
光照或点燃发生反应 |
| H2+Br2=2HBr |
加热至一定温度才能反应 |
| H2+I2=2HI |
不断加热才能缓慢反应,生成的HI会分解 |
(1)卤族元素位于周期表中的__________族。
(2)用电子式表示HCl的形成过程__________。
(3)依据上表,可以推测出:随着原子序数的递增,__________(填字母)。
a. 单质的熔沸点逐渐升高 b. 元素的非金属性逐渐减弱
c. 卤化氢的还原性依次减弱 d. 卤化氢的稳定性依次减弱
(4)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式____________。