下列说法正确的是
| A.熔点:Na-K合金<Na<氯化钠 |
| B.非金属氢化物的稳定性顺序:H2O>H2S>H2Se,HCl<H2S<PH3 |
| C.CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应只生成Na2SO3和O2 |
| D.同一原子中,2p、3p、4p能级的轨道数依次增多 |
X、Y、Z三种元素的原子,其最外层电子排布分别为3s1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式为( )
| A.X2YZ3 | B.XYZ2 | C.X2YZ2 | D.XYZ3 |
A、B、C、D均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为19。下列说法正确的是( )
A.单质的沸点:A>B B.B与C不能存在于同一离子化合物中
C.氧化物的水化物的酸性:C<D D.阴离子的半径:C>D
下列有关性质的比较,不能用元素周期律解释的是( )
| A.热稳定性:Na2CO3>NaHCO3 | B.非金属性:Cl>Br |
| C.碱性:NaOH>Mg(OH)2 | D.酸性:H2SO4>H3PO4 |
根据电子排布的特点,Cu在周期表属于
| A.s区 | B.p区 | C.d 区 | D.ds区 |
原子结构为 的元素,位于元素周期表的
的元素,位于元素周期表的
| A.第六周期第IV族 | B.第四周期第VI族 |
| C.第六周期第A族 | D.第四周期第VIA族 |
有A、B、C、D四种元素的离子A+、B2+、C- 、D2-,它们具有相同的电子数,下列判断中,正确的是
A.A、B、C、D四种元素可能属于同一周期
B.A、B、C、D四种元素一定属于短周期元素
C.原子序数由大到小的顺序是B>A>C>D
D.离子半径由大到小的顺序是、B2+>A+>C- >D2-
关于氟、钠、镁、氯四种元素的性质递变规律,描述正确的是
| A.原子半径:Na<Cl | B.热稳定性:HCl<HF |
| C.离子半径:F-<Mg2+ | D.碱性:NaOH<Mg(OH)2 |
下列各组微粒中,互为同素异形体的是
| A.H和D | B.O2和O3 |
| C.CH3CH2CH2CH3和(CH3)3CH | D.H2O和D2O |
利用周期表中同族元素的相似性,可预测元素的性质。
(1)P元素的基态原子有_______个未成对电子,白磷的分子式为P4,其结构如下图所示。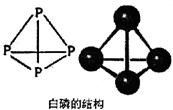
科学家目前合成了N4分子,N原子的杂化轨道类型是________,N -N键的键角为________;N4分解后能产生N2并释放出大量能量,推测其用途为________。
(2) N、P、As原子的第一电离能由大到小的顺序为________。
(3)立方氮化硼晶体的结构如下图所示:
该晶体中,B原子填充在N原子的________空隙,且占据此类空隙的比例为________ (填百分数)。
(4) N与As是同族元素,B与Ga是同族元素,立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是________;立方砷化镓晶体的晶胞边长为a pm,则其密度为________g·cm-3 (用含a的式子表示,设NA为阿伏加德罗常数的值)。
钴(Co)是人体必需的微量元素。含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用。请回答下列问题:
(1)Co基态原子的电子排布式为 ;
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学疗法中的光敏剂、催化剂等方面得到了广泛的应用。其结构如图所示,中心离子为钴离子。
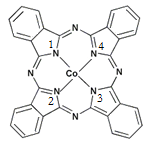
①酞菁钴中三种非金属原子的电负性由大到小的顺序为 ;
(用相应的元素符号作答);碳原子的杂化轨道类型为 ;
②与钴离子通过配位键结合的氮原子的编号是 ;
(3)CoCl2中结晶水数目不同呈现不同的颜色。
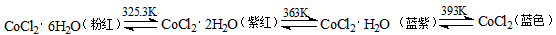
CoCl2可添加到硅胶(一种干燥剂,烘干后可再生反复使用)中制成变色硅胶。简述硅胶中添加CoCl2的作用: ;
(4)用KCN处理含Co2+的盐溶液,有红色的Co(CN)2析出,将它溶于过 量的KCN溶液后,可生成紫色的[Co(CN)6]4-,该配离子具有强还原性,在加热时能与水反应生成淡黄色[Co(CN)6]3-,写出该反应的离子方程式: ;
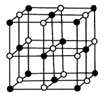
(5)Co的一种氧化物的晶胞如右图所示,在该晶体中与一个钴原子等距离且最近的钴原子有________个;筑波材料科学国家实验室一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是 。
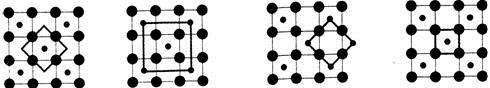
A. B. C. D.
下列说法正确的是
| A.用核磁共振氢谱不能鉴别1-丙醇和2-丙醇 |
B.实验证实 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 |
C. 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 |
D. 的单体是CH3-C≡C-CH3和CH2=CH-CN 的单体是CH3-C≡C-CH3和CH2=CH-CN |
填空题
(1)碳原子最外电子层含有__________个电子,一个碳原子可以跟其他非金属原子形成__________共价键。
(2)在有机合成过程中,引入碳碳双键的三种方法是_____________、________________、_____________。
(3)根据官能团不同,单糖可分为_______________和________________________。
(4)核酸分为DNA和RNA,DNA的主要功能是________________;RNA的主要功能是____________。