实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
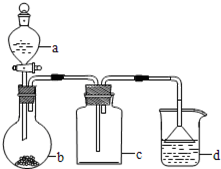
| 选项 |
a中的物质 |
b中的物质 |
c中的物质 |
d中的物质 |
| A |
浓氨水 |
CaO |
NH3 |
H2O |
| B |
浓硫酸 |
Na2SO3 |
SO2 |
NaOH溶液 |
| C |
稀硝酸 |
Cu |
NO2 |
H2O |
| D |
浓盐酸 |
MnO2 |
Cl2 |
NaOH溶液 |
将足量的CO2不断通入NaOH、Ba(OH)2、NaAlO2的混合溶液中,生成沉淀的物质的量与通入CO2的体积之间的关系可表示为( )

做实验时不小心使皮肤上沾上了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸(乙二酸)的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为:MnO4-+C2O42-+H+=CO2↑+Mn2++__。下列有关叙述正确的是( )
| A.发生还原反应的是C2O42- |
| B.该离子方程式右侧横线上的产物是OH- |
| C.10molH+参加反应时,电子转移5mol |
| D.该反应的氧化剂为KMnO4 |
下列溶液中物质的量浓度肯定是1mol/L的是( )
| A.将40gNaOH固体溶解于1L水中 |
| B.将22.4L氯化氢气体溶于水配成1L溶液 |
| C.将1L10mol/L浓盐酸与10L水混合 |
| D.10gNaOH固体溶解在水中配成250mL溶液 |
一定温度下,在容积固定的VL密闭容器中加入nmolA、2nmolB,发生反应:A(g)+2B(g)  2C(g) △H<0,反应达到平衡后测得平衡常数为K,此时A的转化率为x。
2C(g) △H<0,反应达到平衡后测得平衡常数为K,此时A的转化率为x。
(1)一段时间后上述反应达到平衡,则下列说法中正确的是_______________(填字母)。
A.物质A、B的转化率之比为1:2
B.起始时刻和达到平衡后容器中的压强之比为3n:(3n-nx)
C.充入惰性气体(如Ar),平衡向正反应方向移动
D.当2v正(A)=v逆(B)时,反应一定达到平衡状态
(2)K和x的关系满足K=__________(用含V、n、x的表达式表示)。
(3)该反应的逆反应速率与时间的关系如图所示:

①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都仅改变了一种条件,试判断改变的条件:
t2时____________;t8时____________。
②t2时平衡向_________(填“正反应”或“逆反应”)方向移动。
③若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率随时间变化的曲线。
盖斯定律和中和反应原理在生产和科学研究中有很重要的意义。
(1)已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l) △H=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ/mol
反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的△H=__________。
(2)用O2将HCl转化为Cl2,可提高效益,减少污染,传统上该转化通过如图所示的催化剂循环实现
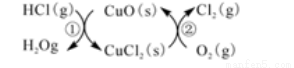
其中,反应①的热化学反应方程式为:2HCl(g)+ CuO(s) H2O(g)+CuCl2(s) △H1
H2O(g)+CuCl2(s) △H1
反应②生成1molCl2(g)的反应热为△H2,则总反应的热化学方程式为_________________(反应热用△H1和△H2表示)。
(3)25℃时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取aL该盐酸与bL该氢氧化钠溶液反应,恰好完全中和,则两溶液的pH的关系式为x+y=________(填表达式)。
某学习小组利用下图所示装置制备氨气,并探究氨气的性质(部分仪器略去)。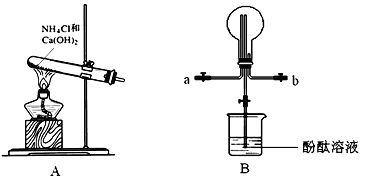
请回答下列问题:
(1)写出以A装置制备氨气的化学方程式:__________________
(2)用B装置收集氨气时,氨气的进气口是__________(填“a”或“b”)。
(3)B装置中烧瓶已收集满氨气,若要使之形成喷泉,操作方法是__________。若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是_________。
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是_________(填序号)。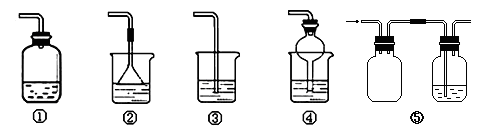
(5)氨气在催化剂并且加热时会被空气氧化,这是工业制硝酸的第一步反应,写出该反应的化学方程式:_________。
室温下,将0.4mol/L一元酸HA溶液和0.2mol/LNaOH溶液等体积混合(忽略混合时溶液体积的变化),测得混合液的pH=5,则下列说法或粒子浓度关系式正确的是( )
A.混合液中由水电离出的c(H+)=1×10-8mol/L
B.c(A-)+c(HA)=2c(Na+)=0.4mol/L
C.HA溶液中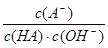 与混合液中
与混合液中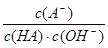 相等
相等
D.c(A-)-c(HA)=2c(OH-)-2c(H+)
在恒容密闭容器中,由CO合成甲醇:CO(g)+2H2(g) CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示。下列说法正确的是( )
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示。下列说法正确的是( )

| A.CO合成甲醇的反应为吸热反应 |
| B.该反应在T1时的平衡常数比T2时的大 |
C.平衡常数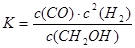 |
D.处于A点的反应体系从T1变到T2,达到平衡时 减小 减小 |
一定温度下,10mL0.4mol/LH2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表:( )
| t/min |
0 |
2 |
4 |
6 |
8 |
10 |
| V(O2)/mL |
0.0 |
9.9 |
17.2 |
22.4 |
26.5 |
29.9 |
下列叙述错误的是(溶液体积变化忽略不计)
A.反应至6min时,c(H2O2)=0.20mol/L
B.反应至6min时,H2O2分解了40%
C.0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L·min)
D.6~10min的平均反应速率:v(H2O2)<3.3×10-2mol/(L·min)
小王同学在一次实验中发现:把新制氯水逐滴加到含有酚酞的氢氧化钠溶液中,当加到最后一滴时溶液的红色突然消失。
(1)知识储备:将氯气通入水中的化学方程式为 ;氯水中具有强氧化性的分子有 、 。
(2)探究“溶液的红色突然消失”的原因:
①猜想:a.是氯水中的盐酸中和了NaOH,使酚酞由红色变成无色;
b.是 。
②设计实验:往已褪色的溶液中连续滴加NaOH溶液至过量,若现象为 ,则证明“猜想a”正确;若现象为 ,则“猜想b”正确。
(1)地壳中含量最高的金属是 ,NaHCO3俗称 ,制造计算机芯片的半导体材料是 ,水晶项链的主要成分是 。
(2)在反应3Cu+8 HNO3(稀)="=" 3Cu(NO3)2+2NO↑+4H2O中,失去电子的是_________(填元素符号),被还原的是_______(填元素符号)。当产生标况下4.48 L气体时消耗单质铜 g,此时转移了_______ mol电子。
2007年诺贝尔化学奖授予善于做“表面文章”的德国科学家格哈德·埃特尔。他的成就之一是证实了气体在固体催化剂表面进行的反应,开创了表面化学的方法论。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示。下列说法正确的是 
| A.NO2是该过程的最终产物 |
| B.NO和O2必须在催化剂表面才能反应 |
| C.汽车尾气的主要污染成分是CO2和NO |
D.该催化转化的总反应方程式为:2NO +O2 +4CO 4CO2+N2 4CO2+N2 |
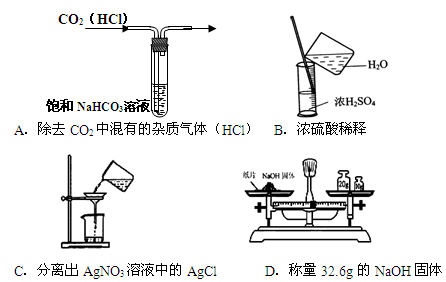
实验是研究化学的基础,下图中所示的实验方法、装置或操作均正确的是