在一定温度下,将气体X和Y各0.16mol充入10L恒容密闭容器中,发生反应发生反应X(g)+Y(g) 2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表所示:
2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表所示:
| t/min |
2 |
4 |
7 |
9 |
| n(Y)/mol |
0.12 |
0.11 |
0.10 |
0.10 |
计算该温度下此反应的化学平衡常数为多少?
某学生用0.1000mol/L盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应)。实验步骤如下:
(1)配制待测液:用2.50g含有少量杂质的固体烧碱样品配制500mL溶液。需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要___________。
(2)滴定:
Ⅰ.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“0”刻度线以上。
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”刻度线以下,并记录读数。
Ⅲ.移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液。
Ⅳ.用标准液滴定至终点,记录滴定管液面读数。
①上述滴定步骤中有错误的是(填编号)____________。该错误操作会导致测定结果___________(填“偏大”、“偏小”或“无影响”)。
②排去碱式滴定管中气泡的方法应采用右图的___________操作。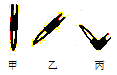
③步骤Ⅳ中滴定时眼睛应____________;判断滴定终点的现象是_____________。
④若步骤Ⅱ中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果___________(填“偏大”、“偏小”或“无影响”)
(3)按正确操作测得有关数据记录如下:按正确操作测得有关数据记录如下:
| 滴定次数 |
待测液体积 |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
20.00 |
0.20 |
20.38 |
| 第二次 |
20.00 |
4.00 |
24.20 |
| 第三次 |
20.00 |
2.38 |
a |
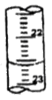
①a的读数如图所示,则a=___________;②烧碱样品的纯度为_________ %
室温下,用0.10mol/LKOH溶液滴定10.00mL0.10mol/LH2C2O4(二元弱酸)溶液,所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答: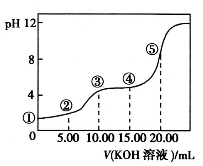
(1)点①所示溶液中,Kw=_____________。
(2)点②所示溶液中的电荷守恒式为_____________________。
(3)点③所示溶液中所有离子的浓度由大到小的顺序为___________________。
(4)点④所示溶液中的物料守恒式为0.10mol/L=___________。
(1)Na2CO3溶液显_______________性,用离子方程式表示其原因为_________________。
(2)常温下,pH=11的NaHCO3溶液中,水电离出来的c(OH-)=_______________mol/L,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=_________mol/L。
(3)已知纯水中存在如下平衡:H2O H++OH-。现欲使平衡逆向移动,且所得溶液显酸性,可选择的方法是__________(填字母序号)。
H++OH-。现欲使平衡逆向移动,且所得溶液显酸性,可选择的方法是__________(填字母序号)。
| A.向水中加入NaHCO3固体 | B.向水中加入NaHSO4固体 |
| C.加热至100℃ | D.向水中加入(NH4)2SO4固体 |
(4)若将等pH、等体积的NaOH溶液和NH3·H2O溶液分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m_______n(填“<”“>”或“=”)。
(5)等物质的量浓度的下列溶液:①NaCl; ②NaOH; ③CH3COOH; ④HCl; ⑤CH3COONa ;⑥NaHCO3;⑦Ba(OH)2;⑧Na2CO3,pH由大到小的顺序为_________(填序号)。
研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:1molCO(g)与适量的SO2(g)反应生成S(s)和CO2(g)时,放出135kJ的热量,则此反应的热化学方程式为______________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体,用CO(g)处理NO2(g)的能量转化关系如图所示。

标准状况下,22.4LCO和NO2发生上述反应。整个过程中,转移电子的物质的量为___________mol,放出的热量为___________kJ(用含有a的代数式表示)。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1="-574kJ/mol"
② CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2
若1molCH4(g)直接将NO2(g)还原至N2(g),整个过程中放出的热量为867kJ,则△H2=_____________。
右图是某同学设计的验证原电池和电解池的实验装置,下列说法不正确的是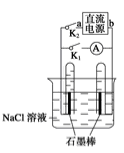
| A.若关闭K2、打开K1,一段时间后,发现左侧试管收集到的气体比右侧略多,则a为正极,b为负极 |
| B.关闭K2,打开K1,一段时间后,用拇指堵住试管移出烧杯,向试管内滴入酚酞,发现左侧试管内溶液变红色,则 a为负极,b为正极 |
| C.若直流电源a为负极,b为正极,关闭K2,打开K1,一段时间后,再关闭K1,打开K2,则电路中电流方向为从右侧石墨棒沿导线到左侧石墨棒 |
| D.若直流电源a为负极,b为正极,关闭K2,打开K1,一段时间后,左侧产生的是氢气,右侧产生的是氯气,再关闭K1,打开K2,构成原电池,则左侧是正极,右侧是负极,在左侧石墨棒上发生还原反应,发生的电极反应为H2-2e-+2OH-=2H2O,正确。 |
近年来科学家研制了一种新型的乙醇电池(DEFC),它用磺酸类质子作溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更加安全.电池总反应式为:C2H5OH+3O 2 →2CO 2+ 3H2O.下列说法不正确的是( )
A.1mol乙醇被氧化转移6mol电子
B.C2H5OH在电池的负极上参加反应
C.在外电路中电子由负极沿导线流向正极
D.电池正极的电极反应式为4H++O2+4e-=2H2O
已知25℃时,几种难溶电解质的溶度积常数Ksp如下表所示:
下列叙述不正确的是
| A.由溶度积常数不能判断相应物质的溶解性大小 |
| B.将等体积的4×10-3 mol/L的AgNO3溶液和4×10-3mol/L K2CrO4溶液混合,有Ag2CrO4沉淀产生 |
| C.向AgCl的悬浊液中滴加饱和NaBr溶液不能得到黄色AgBr |
| D.向100 mL 0.02mol/L的NaSO4溶液中加入100mL0.02mol/L的AgNO3溶液,有白色沉淀生成 |
如图是温度和压强对反应X+Y 2Z影响的示意图。下列叙述正确的是( )
2Z影响的示意图。下列叙述正确的是( )

| A.上述可逆反应的正反应为放热反应 |
| B.X、Y、Z均为气态 |
| C.X和Y中只有一种是气态,Z为气态 |
| D.上述反应的正反应的△H>0 |
符合图1、图2的反应是
A.X(g)+3Y(g) 2Z(g);ΔH>0 2Z(g);ΔH>0 |
B.X(g)+3Y(g) 2Z(g);ΔH<0 2Z(g);ΔH<0 |
C.X(g)+2Y(g) 3Z(g);ΔH<0 3Z(g);ΔH<0 |
D.5X(g)+3Y(g) 4Z(g);ΔH<0 4Z(g);ΔH<0 |
常温下,下列溶液中离子浓度关系表达正确的是
| A.Na2CO3溶液中:c(H+)+c(Na+)=c(OH-)+c(CO32-)+c(HCO3-) |
| B.0.1mol/L的Na2CO3溶液中:c(Na+)> c(CO32-) > c(OH-)>c(HCO3-) |
| C.pH=5.3的NaHSO3溶液:c(Na+)>c(HSO3-)>c(H2SO3)>c(SO32-) |
| D.pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后:c(Na+)>c(CH3COO-)+c(OH-)+c(H+) |
常温下,下列各组离子在相应的条件下可能大量共存的是
| A.能使pH试纸变红的溶液中:CO32-、K+、Cl-、Na+ |
B.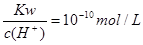 的溶液中:Na+、HCO3-、Cl-、K+ 的溶液中:Na+、HCO3-、Cl-、K+ |
| C.在c(OH-)/c(H+)=1×1012的溶液中:NH4+、Fe2+、Cl-、NO3- |
| D.由水电离产生的c(OH-)=1×10-12mol/L的溶液中:NO3-、Mg2+、Na+、SO42- |
已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是下列三种酸的电离常数,若已知下列反应可以发生:NaCl+HNO2=HCN+NaNO2,NaNO2+HF=HNO2+NaF。据此判断,下列叙述不正确的是
| A.K(HF)=7.2×10-4 | B.K(HNO2)=4.9×10-10 |
| C.反应NaCN+HF=HCN+NaF可以发生 | D.K(HCN)<K(HNO2)<K(HF) |
室温时,将浓度和体积分别为c1,V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是
| A.当pH=7时,若V1=V2,则一定是c2>c1 |
| B.在任何情况下都满足c(Na+)+ c(H+)=c(CH3COO-)+c(OH-) |
| C.若pH>7,则一定是c1V1>c2V2 |
| D.若V1=V2,c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+) |
将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g) 2Z(g) ∆H< 0。当改变某个条件并达到新平衡后,下列叙述正确的是( )
2Z(g) ∆H< 0。当改变某个条件并达到新平衡后,下列叙述正确的是( )
| A.升高温度,X的物质的量减小 |
| B.增大压强(缩小容器体积),Z的浓度不变 |
| C.保持容器体积不变,充入一定量的惰性气体,Y的浓度不变 |
| D.保持容器体积不变,充入一定量的Z,重新平衡时,Y的体积分数增大 |