下列实验能达到预期目的的是( )
| A.检验溶液中是否含有CO32-:滴加稀盐酸,将产生的气体通入澄清石灰水 |
| B.检验溶液中是否含有NH4+:先滴加浓NaOH溶液并加热,再用湿润的红色石蕊试纸 |
| C.检验溶液中是否含有Fe2+:先滴加氯水,再滴加KSCN溶液 |
| D.检验溶液中是否含有SO42-:先滴加氯化钡溶液,再滴加稀盐酸 |
以下实验:①为检验RX是碘代烷,将RX与NaOH水溶液混合后再加入AgNO3溶液;②实验室里用无水乙醇和浓硫酸共热至140℃制乙烯;③用锌和稀硝酸反应制取氢气,用排水法收集氢气;④在试管中加入2mL10%的CuSO4溶液,滴入2%的NaOH溶液4~6滴,振荡后加入乙醛溶液0.5mL,加热至沸腾来检验醛基;⑤为检验淀粉已水解,将淀粉与少量稀硫酸加热一段时间后再加入银氨溶液,水浴加热。其中可能失败的实验是( )
| A.①②③④⑤ | B.①④⑤ | C.③④⑤ | D.③⑤ |
已知某待测液由Ag+、Mg2+、K+、Ba2+、NO3-中的若干种离子组成,进行如下实验:
第一步:加入过量的稀盐酸,有白色沉淀生成。
第二步:过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
第三步:再过滤,取少量滤液,滴入NaOH溶液至溶液呈碱性,在此过程中溶液无明显现象。
根据实验现象回答:
(1)分别写出第二步和第三步中所涉及的反应的离子方程式:
第二步: 第三步: ;
(2)待测液中一定含有 和NO3-离子,一定不含有 离子,还有一种离子不能确定其是否存在,要检验这种离子的实验方法是(填写实验名称和观察到的现象及结论,不要求写实验操作过程):实验名称 ,现象及结论 。
下列实验操作能达到预期目的是( )
| A.向某无色溶液中加BaCl2溶液产生不溶于稀HNO3的白色沉淀,说明原溶液中一定有SO42- |
| B.向某无色溶液中加入盐酸,有无色无味的气体产生,则说明原溶液中一定有CO32- |
| C.向某溶液中滴加KSCN溶液,溶液不变红,再滴加氯水,变红,说明原溶液一定有Fe2+ |
| D.向某无色溶液中加浓NaOH溶液并加热,产生能使湿润的蓝色石蕊试纸变红的气体,则说明原溶液中一定有NH4+ |
下列关于离子检验的叙述正确的是( )
| A.向FeCl2、NaI的混合溶液中加入硫氰化钾溶液,再滴加少量氯水,溶液没有变为红色,说明还原性:Fe2+<I- |
| B.检验AlNH4(SO4)2溶液中的NH4+:取样于试管中,向溶液中加入少量NaOH溶液,加热,用湿润的红色石蕊试纸检验产生的气体 |
| C.检验Na2SO3和Na2SO4的混合溶液中的SO42-:先加足量稀硝酸,再加氯化钡溶液 |
| D.验证碳酸钠溶液显碱性是CO32-导致的:先加酚酞试液,溶液变红,再加硫酸溶液,红色褪去 |
除去下列物质中的杂质(括号内为杂质),所选用的试剂及操作方法不正确的是( )
| 选项 |
待提纯的物质 |
选用试剂 |
操作的方法 |
| A |
FeCl2溶液(FeCl3溶液) |
铁粉 |
过滤 |
| B |
Al2O3(Fe2O3) |
NaOH溶液和CO2 |
溶解、过滤、过滤 |
| C |
Cl2(HCl) |
饱和食盐水 |
洗气 |
| D |
Na2CO3固体(NaHCO3固体) |
—— |
加热至质量不再变化 |
Ⅰ.铁是人体必需的微量元素,绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。
(1)测定绿矾样品含量的实验步骤:
A.称取5.7 g样品,溶解配成 250 mL溶液
B.量取25 mL待测液于锥形瓶中
C.用硫酸酸化的0.01 mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积为40 mL。
根据上述步骤回答下列问题:
①用硫酸酸化的KMnO4溶液滴定终点的标志是____________________。
②计算上述样品中 FeSO4·7H2O的质量分数为____________________。
Ⅱ.硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,常用于代替硫酸亚铁。
(2) 为检验分解产物的成分,设计如下实验装置进行实验,加热A中硫酸亚铁铵至分解完全。
①A中固体充分加热较长时间后,通入氮气,目的是_________________。
②装置B中BaCl2溶液的作用是检验分解产物中是否有SO3气体生成,若含有该气体,观察到的现象为________________。
③实验中观察到C中有白色沉淀生成,则C中发生的反应为______________(用离子方程式表示)。
下列除杂试剂的选择或除杂操作不正确的是
| |
括号内为杂质 |
除杂试剂 |
除杂操作 |
| A |
Na2O2(Na2O)固体 |
O2 |
在纯氧气中加热 |
| B |
Na2CO3 (NaHCO3)溶液 |
CO2 |
通入过量的 CO2 |
| C |
FeCl3(FeCl2)溶液 |
Cl2 |
通入过量的 Cl2 |
| D |
FeSO4(CuSO4)溶液 |
Fe |
加入过量的 Fe 粉,充分反应后过滤 |
榴石矿石可以看作由CaO、FeO、Fe2O3、Al2O3、SiO2组成。工业上对其进行综合利用的流程如下: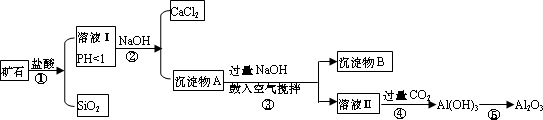
(1)溶液Ⅰ中除了Ca2+外,还可能含有的金属阳离子有__________________;
(2)步骤③中NaOH参加反应的离子方程式____________________________,鼓入空气并充分搅拌的目的是(用化学方程式表示)____________________;
(3)在工业生产中,步骤④通入过量CO2而不加入盐酸的原因是_____________________。
下列除杂方案错误的是
| 选项 |
被提纯的物质 |
杂质 |
除杂试剂 |
| A |
FeCl3(aq) |
Al3+(aq) |
NaOH溶液、盐酸 |
| B |
AlCl3(aq) |
Cu2+ |
Al粉 |
| C |
NaHCO3(aq) |
Na2CO3(aq) |
CO2气体 |
| D |
FeCl3(aq) |
Cu2+ |
Fe粉 |