在实验室用电解水的实验来测定水的组成,负极产生的气体体积是正极产生气体体积的2倍,化学反应的文字表达式为 ,由此可得出的结论是 。过氧化氢溶液在常温下 (填“能”或“不能”)产生氧气;只给氯酸钾加热 (填“能”或“不能”)产生氧气。
下图是实验室制取气体的常用装置。
(1)仪器①的名称是 。
(2)用高锰酸钾制取氧气的化学方程式为 ;实验时应在试管口放一团棉花,其作用是 ;用排水法收集氧气的合适时机是 。用右图所示装置收集氧气,氧气应从 (填“a”或“b”)端导入。
(3)用双氧水制取氧气应选用的发生装置是(填装置字母) ;发生反应的化学方程式为 。
下图是一组用于研究可燃物燃烧条件的对比实验,请回答有关问题:(1)仅由实验1就可得出可燃物燃烧的条件是:
① ;② 。
(2)通过实验2可以进一步得出燃烧所需要的条件,实验中发生反应的化学方程式为 。
(3)一旦室内起火时,如果打开门窗,火反而会烧得更旺,原因是 。
扑灭森林火灾的有效方法之一,是将大火蔓延路线前的一片树木砍掉,其灭火原理
是 。
通过一年的化学学习,同学们对身边的常见物质有所认识,并能用所学的知识解释一些问题。请按要求回答下列问题:
(1)服用含Al(OH)3的药物来治疗胃酸过多,其反应的化学方程式为 。
(2)鉴别铵态氮肥(含有铵根离子)、磷肥、钾肥三种化肥,首先看外观,
的是磷肥,然后将另两种化肥各取少许,分别和少量的熟石灰粉末混合、研磨,能嗅到气味的是 。
(3)三支试管中分别装有少量白色固体,它们分别是氯化钠、氢氧化钠、碳酸钙中的一种,只要加入足量的 就能将它们一次性鉴别出来;
(4)将稀盐酸、Na2CO3溶液、Ca(OH)2溶液倒入同一烧杯中,充分反应后过滤,得到固体A和滤液B。滤液B中一定含有的溶质是 。
(10分)用化学方程式解释下列问题:
(1)工业上用稀硫酸除去铁制品表面的铁锈 ;
(2)食品包装常用生石灰作干燥剂 ;
(3)二氧化碳通入足量的氢氧化钠溶液
(4)纯碱和稀盐酸反应
(5)铜丝插入硝酸银溶液反应
(4分)生产、生活中使用的金属材料很多。
(1)生铁属于 (填写物质类别),为了防止铁制品生锈,经常在其表面涂上一层活动性较强的金属粉末铝的原因是什么?
(2)如图所示,某同学对实验室药品柜里的氧化铜瓶塞上的蓝色物质产生了探究欲望,经过查阅资料知道,该物质是氧化铜与空气中的二氧化碳和 缓慢氧化生成的铜绿〔化学式为Cu2(OH)2CO3)〕。请写出化学方程式。
按要求写出下列反应的化学方程式。
(1)铁丝在氧气中燃烧:
(2)加热氯酸钾和二氧化锰的混合物制取氧气:
(3)木炭粉和氧化铜在高温下反应:
(4)小苏打与稀盐酸反应:
某校化学课外小组的同学,利用塑料瓶(质软)设计了下图所示的实验。请你根据生活经验及所学的知识,结合实验回答下列问题:
(1)请你分析并推测振荡后塑料瓶将发生什么变化?
(2)发生该变化的原因是什么?
(3)由此实验你可得出什么结论?
科学地利用和控制燃烧非常重要。同种可燃物燃烧的剧烈程度和什么因素有关?请写出其中的一种因素并举出实例加以论证。
实验室有一包粉末状物质。可能是氯化钠、硫酸钠、碳酸钠,氯化铁中的一种或几种组成,为了确定原粉末的成分,某校化学兴趣小组的同学按下图所示进行试验: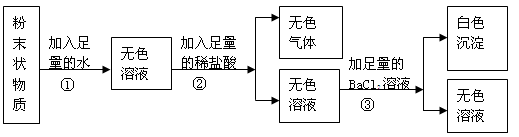
(1)该粉末中一定不含有的物质是 ,可能含有的物质是 。
(2)写出步骤③的化学方程式: 。
实验室里有稀硫酸、氧化铜、铁粉三种物质,请你设计两种方案制取铜(用化学方程式表示).
方案一:;
方案二:.
碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)是生活中常见的盐,有着广泛的用途,根据所学知识回答:
⑴碳酸钠和碳酸氢钠中阴离子对应的酸都是 (填化学式);
⑵碳酸钠常作食用碱,水溶液PH 7(填“>”“=”“<”)
⑶碳酸氢钠俗名 ,在医疗上用作治疗胃酸过多,反应的化学方程式为 ;
⑷碳酸钠固体中混有少量的碳酸氢钠,常用加热的方法除去碳酸氢钠,反应的化学方程式为2NaHCO3 Na2CO3+
Na2CO3+ ↑+H2O,则“
↑+H2O,则“ ”中的化学式为 ;
”中的化学式为 ;
⑸干粉灭火器利用碳酸氢钠来灭火,其灭火原理是 。
根据初中化学所学知识回答下列问题:
(1)判断稀盐酸与下表中的四种化合物溶液之间能否发生反应.请仿照示例,在表格内②③④处填写("能"或"不能"),并根据复分解反应发生的具体条件在对应的表格中填写判断依据.
| 氢氧化钠溶液 |
氯化钠溶液 |
碳酸钾溶液 |
硝酸银溶液 |
|
| 稀盐酸 |
示例:① 反应 |
② 反应 |
③ 反应 |
④ 反应 |
| 判断依据 |
示例: |
⑵某工厂化验室用20%的氢氧化钠溶液洗涤一定量石油产品中残余的硫酸,共消耗氢氧化钠溶液80.0g,洗涤后的溶液呈中性,这一定量石油产品中含H2SO4的质量是多少?
某同学在实验室发现了一块绿色的孔雀石标本,他查阅资料知其主要成分是
.他以
为原料制取铜,实验流程如下图所示(部分生成物已省略)

(1)
溶液中所含的溶质是。
(2)固体
中所含的物质是。
(3)
与稀硫酸发生的化学方程式为。
硫酸产量标志着一个国家化工业发展的水平。工业生产硫酸的主要流程为:
①煅烧黄铁矿4FeS2+11O2 2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
②SO2转化为SO3 ③用浓H2SO4吸收SO3 请回答相关问题:
(1)如何利用流程①中形成的固体剩余物: 。
(2)SO2具有与CO2相似的化学性质。有人设计用熟石灰吸收尾气中的SO2,请写出此反应的化学方程式 。
(3)第②步反应是一个化合反应,请判断实现此反应的另一反应物是 。
(4)将SO2和Cl2通入水中至恰好完全反应,生成两种常见的酸,请完成下列化学方程式:Cl2+SO2+2H2O=== +2HCl
(5)实验室稀释浓硫酸的方法是:
。