有一包固体粉末可能含有Na 2CO 3、FeCl 3、CaCl 2、NaOH中的一种或几种,为了探究它们的成分,进行如下实验:①取少量该固体粉末加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;②向滤液中滴加酚酞溶液,溶液变红.根据上述实验回答下列问题:
(1)粉末中一定不含 ,一定含有 .
(2)为了确定可能含有的物质,取少量②中红色溶液于试管中,加入过量的 溶液,若溶液仍为红色,则证明该物质一定存在.
铁是目前世界年产量最多的金属

(1)如图是一氧化碳还原氧化铁实验装置图,回答下列问题:
①写出甲处玻璃管中的化学反应方程式 ;
②下列关于该实验的说法正确的是 (填字母)。
A.装置甲处玻璃管内黑色粉末变红
B.实验结束后,应先熄灭甲处的酒精喷灯
C.一氧化碳发生了还原反应
(2)每年因腐蚀而浪费掉的金属材料数量惊人,铁栅栏常采取的防锈措施是 ,除防止金属腐蚀外,保护金属资源的有效途径还有 (答一点即可)。
有一工业过程:

按要求回答下列问题:
(1)请将电石与水反应的化学方程式补充完整:
CaC 2+2H 2O═Ca(OH) 2+ ↑.
(2)有关物质常温下的溶解度如表:
| 物质 |
Ca(ClO 3) 2 |
CaCl 2 |
KClO 3 |
KCl |
| 溶解度/g |
209.0 |
74.5 |
7.3 |
34.2 |
上述流程中加入了KCl粉末,KCl与 (填化学式)发生了复分解反应得KClO 3晶体,该过程得到KClO 3晶体的原因是 .
(3)写出向CaCl 2溶液中通入两种气体生成CaCO 3的化学方程式: .
稀盐酸是实验室常用的试剂,有关稀盐酸的性质实验如下。
①若需检验某盐酸样品中是否含有硫酸,应选用的试剂是 。
②向放有锌粒的试管中滴加稀盐酸,有气泡产生,该反应的基本类型是 。
③向滴有酚酞的氢氧化钠溶液中滴加稀盐酸至过量,观察到的现象是 ,反应的化学方程式是 。
④镓(Ga)是一种活泼金属,能与稀盐酸反应。反应中,反应物Ga与生成物H 2的物质的量关系如图所示,请写出该反应的化学方程式 。

实验室制取氧气并进行相关性质实验。

①写出仪器甲的名称 。
②以氯酸钾和二氧化锰为原料制氧气的化学方程式是 ,应选用的发生装置是 (选填编号),用向上排空气法收集氧气应选用的装置是 (选填编号)。
③用排水法收集氧气时,集气瓶内的水全部排出后,将导管移出集气瓶,再进行如下操作:a.从水槽中取出集气瓶;b.瓶口向上放置;c.在集气瓶口盖好毛玻璃片。正确的操作顺序是 (用编号排序)。
④硫在氧气中燃烧生成二氧化硫,火焰呈 色;二氧化硫若大量排放到空气中造成的后果是 。铁丝在氧气中燃烧的化学方程式是 ,实验时应预先在集气瓶底部放少量细沙,细沙的作用是 。
(1)倾倒液体时,细口瓶标签的一面朝向 处,细口瓶的塞子要 在桌面上。
(2)量液体时,量筒必须放平,视线要与量筒内液体 液面的最低处保持水平,再读出液体的体积。
现有甲、乙、丙、丁四种无色溶液,它们分别是稀HCl、稀H 2SO 4、BaCl 2溶液、Na 2CO 3溶液中的一种,已知甲+乙→无明显现象,乙+丙→白色沉淀,丙+丁→白色沉淀,甲+丁→无色气体;BaCO 3、BaSO 4难溶于水。试回答:
(1)丁物质中的溶质是 (填化学式)
(2)写出乙和丙反应的化学方程式 。
(3)写出甲和丁反应的化学方程式 。
某同学将甲乙固体各30克分别加入100克水中后,进行了如图1所示的实验。甲乙两种固体的溶解度曲线如图2所示。

请回答:
(1)10℃时,甲乙两种物质的溶解度大小关系:甲 乙(填"<"">"或"=")。
(2)m的取值范围 。
(3)40℃时,取等质量的甲乙两种物质的饱和溶液分别蒸发等量的水后,恢复到40℃.下列说法正确的是 (填字母)。
A.恢复到原温度后,溶液中溶剂的质量:甲=乙
B.恢复到原温度后,析出晶体的质量:乙>甲
C.若再降温到20℃时,溶液的质量:甲>乙
D.若再降温到20℃时,溶液的溶质质量分数:甲=乙
古往今来,金属材料和制品在我们的社会生活中一直起着非常重要的作用。
(1)考古工作者发现铁质的出土文物往往锈蚀严重,铁生锈的条件是 。在实验室常用稀盐酸清除铁锈,化学方程式为 。
(2)近年来,我国高铁建设促进了经济、社会的快速发展。制造铁轨的材料是合金钢,主要原因是合金钢具有 的优越性能(要求只答一条)。
(3)某同学在实验室进行了两个有关金属性质的实验:
实验Ⅰ:硫酸铝溶液和铁粉混合
实验Ⅱ:硫酸铜溶液与铁粉混合
在上述两个实验结束后,该同学将实验Ⅰ和Ⅱ的物质全部倒入同一个烧杯中,发现烧杯内的红色固体明显增多,原因是 (用文字说明)。一段时间后过滤,向滤渣中滴加盐酸,结果没有气泡产生。那么,滤液中所含金属离子的情况可能是 [填写序号)。
①Al 3+
②Al 3+、Fe 2+
③Al 3+、Fe 3+
④Fe 2+、Cu 2+
⑤Al 3+、Fe 2+、Cu 2+
已知A、B、C、D、X是初中化学常见的五种物质,它们在一定条件下能发生如图所示的转化关系,其中X为大气循环的气体。

(1)若反应①为置换反应,则X是 :反应①的化学方程式是
(2)若反应①为复分解反应,则X是 :反应③的化学方程式是
阅读科普短文
稀土材料
稀土元素是指元素周期表中ⅢB族的钪(Se)、钇(Y)以及铜系元素。这些元素的氧化物都不溶于水,外形像泥土,而且又稀少,因而人们喜欢称它们为"稀土元素"。稀土元素的化学性质较为活泼,若与其他元素结合,便可组成种类繁多、功能多样、用途广泛的新型材料,且性能会有较大提高,被称作当代的"工业味精"稀土元素的镧(La)、铈(Ce)、镨(Pr)、钕(Nd)。在元素周期表中的位置如图所示。
稀土元素的化合物还是生产特种玻璃和陶瓷的重要原料。如将三氧化二铈(Ce 2O 3)加入玻璃中,可制成低散射、高折射的光学玻璃,用于生产精密的光学器材。
根据短文内容,回答下列问题
(1)从材料中可得出,稀土元素的化学性质 。
(2)铈元素的质子数是 。
(3)三氧化二铈(Ce 2O 3)中Ce元素的化合价是 价。
(4)三氧化二铈(Ce 2O 3)的用途是 。
质量守恒定律的发现,对化学的发展做出了重要贡献。

(1)通过分别称量下列两组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是 (填标号)a.大理石和稀盐酸 b.NaOH溶液和Na 2SO 4溶液
(2)在足量氧气中点燃镁条的实验过程中,固体质量变化如图一。
①从燃烧条件分析,固体质量在t 1前没有发生变化的原因是
②该反应的化学方程式为
③参加反应的氧气质量为 g
(3)在一定条件下,A和B反应生成C,微观示意图如图二。回答下列问题:
①一个A分子由 个原子构成
②C分子中原子的质量比N:O=
③该反应的化学基本反应类型为
④上述反应中一定发生改变的是 (填标号)
a.元素种类 b.原子种类 c.分子种类
图1是元素周期表的部分信息,请根据下表回答有关问题:

(1)具有相似化学性质的一组元素是 。
| A. |
Na、Cl |
B. |
C、Be |
C. |
F、Cl |
D. |
Cl、Ar |
(2)由第7号元素和第12号元素的原子形成化合物的化学式为 。
(3)某粒子的结构示意图如图2,当x﹣y=8时,该粒子的符号为 。
(4)钠、氯、氧三种元素可形成原子个数比为1:1:4的化合物,则此化合物中氯元素的化合价为 。
(5)具有相同原子数和电子数的分子或离子叫等电子体。下列各组粒子中属于等电子体的是 。
| A. |
NO和O 2 |
B. |
CO和N 2 |
C. |
SO 2和CO 2 |
D. |
NH 4 +和H 2O |
(1)图1装置中既能制O 2又能制CO 2的是 (填序号).
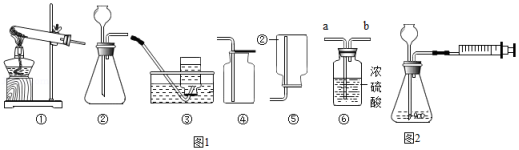
请写出实验室用你所选装置制两种气体的化学方程式.
制O 2:
制CO 2:
(2)用推拉注射器活塞的方法来检查装置气密性,如图2,当缓慢拉动活塞时,如果装置气密性良好,则能观察到 .
(3)将制得的CO 2通入到盛有NaHCO 3溶液的装置⑥中,目的是 (请用化学方程式表达).