高温分解贝壳(主要成分是碳酸钙)可以生成氧化钙和二氧化碳。现高温分解50t含碳酸钙80%的贝壳,最多可得到氧化钙多少t(反应方程式为:CaCO3 CaO+CO2↑)
CaO+CO2↑)
帕拉米韦氯化钠注射液是治疗H7N9亚型禽流感的有效药物之一,帕拉米韦的化学
式为C15H28NXO4.试计算:
(1)帕拉米韦中氢元素与氧元素的质量比为 ;
(2)帕拉米韦的相对分子质量为328,则x的数值为 ;
(4)32.8g的帕拉米韦中氧元素的质量为 g。
实验室里有一瓶固体烧碱因吸收了空气中的二氧化碳而部分变质。为测定这瓶烧碱的纯度,称取该样品20g,溶于水配成溶液,向其中逐滴加入氯化钡溶液至沉淀完全,反应过程中生成沉淀的质量与所用氯化钡溶液质量关系如图所示。
(1)从图中可以看出,反应产生的沉淀最多是 g。
(2)该烧碱样品中碳酸钠的质量是多少g?
向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图。据图回答:
(1)在滴加NaOH溶液过程中,原溶液中 离子个数不变。(填离子符号)
(2)P点溶液中的溶质是 。
(3)m1的值为 。
(4)M点溶液中的溶质质量分数是多少?
圆梦中学现有20%的硝酸钾溶液、蒸馏水、硝酸钾固体,现需要100g质量分数为15%的硝酸钾溶液,请根据下列要求计算:
(1)若选用硝酸钾固体和蒸馏水来配制,各需多少?
(2)若选用20%的硝酸钾溶液与蒸馏水来配制,各需多少?
为了消除碘缺乏病,我国政府规定居民的食用盐必须加碘,简称碘盐.
(1)碘酸钾的化学式为KIO3,则碘酸钾的相对分子质量为 ,碘酸钾中钾、碘、氧元素的质量比为 .
(2)若1kg碘盐中含30mg碘。已知成年人每天约需要0.15mg碘,假设这些碘主要从碘盐中摄取的,则成人每天需要食用碘盐 g?
(3)多少克碘酸钾中含碘元素20mg?
已知硫酸铵的化学式(NH4)2SO4,试计算:
(1)硫酸铵的相对分子质量?
(2)硫酸铵中各元素的质量比?
(3)264千克含硫酸铵90%的硫铵化肥中含氮元素多少千克?
某保健品主要成分为碳酸钙,请完成下列问题:
(1)碳酸钙的化学式为CaCO3,其相对分子质量为 钙、碳、氧元素的质量比为
(2)碳酸钙中钙元素的质量分数是
(3)某儿童现需要补充钙元素200mg,则该儿童需食用该碳酸钙 克
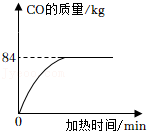
我国明代科技著作《天工开物》中有利用炉甘石(主要成分是ZnCO3)火法炼锌的工艺记载,主要反应原理为ZnCO3+2C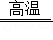 Zn+3CO↑,现用200kg炉甘石与足量碳充分反应,产生CO的质量与加热时间的关系如图所示。
Zn+3CO↑,现用200kg炉甘石与足量碳充分反应,产生CO的质量与加热时间的关系如图所示。
(1)此过程中产生CO的质量是 kg。
(2)列式计算此炉甘石中ZnCO3的质量分数。
某钢铁厂每天需消耗1000t含氧化铁80%的赤铁矿石,该厂理论上可以炼出含铁96%的生铁的质量是多少?
(6分)2013年11月,某快递公司违反国家规定快递有毒化学品,因化学品泄漏,导致多人伤亡,被称为“夺命快递”。“夺命快递”中的化学品是氟乙酸甲酯(化学式为C3H5FO2),是有毒液体,在染料、医药、农药等工业领域有着广泛的用途。
(1)氟乙酸甲酯中碳、氢、氟、氧的原子个数比是
(2)一般成人接触400mg氟乙酸甲酯就会急性中毒。如果检测到被氟乙酸甲酯污染的某物品上含有氟元素57mg(氟元素都来自氟乙酸甲酯),通过计算说明接触该污染物品的成年人会不会急性中毒。
汽车尾气排放出的气体主要有NO和NO2,它们污染环境,可用氨气(NH3)除去。反应的化学方程式为:2NH3+NO+NO2催化剂2N2+3H2O。若反应后得到56gN2,理论上消耗氨气多少克?
(8分)某化学兴趣小组在室温的条件下(温度为20℃),为了测定H2SO4与NaOH发生中和反应时放出的热量,在左下图的小烧杯中加入8mL溶质质量分数为10%的NaOH溶液(密度1 g/mL),并滴入3滴酚酞,测量其温度;另取过量的稀硫酸(密度1.12g/mL),测量其温度后逐量缓慢地加入到小烧杯中,边加边用环形玻璃棒搅拌;测得烧杯中溶液温度的变化与加入稀硫酸体积之间关系如右下图所示。
(1)当加入5 mL稀硫酸时,溶液中的溶质有 (填写溶质化学式)。
(2)当加入约为 mL稀硫酸时,烧杯中溶液的温度达到最高。此时烧杯中溶液的温度约为(填写整数) ℃,烧杯中溶液颜色 。
(3)当加入稀硫酸的体积大于10mL时,溶液温度下降的原因是 。
(4)当溶液温度升到最高时,此时溶液中溶质质量分数是多少?(写出计算过程,共3分)