向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图。据图回答: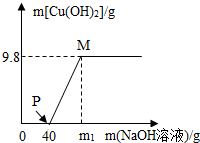
(1)在滴加NaOH溶液过程中,原溶液中 离子个数不变。(填离子符号)
(2)P点溶液中的溶质是 。
(3)m1的值为 。
(4)M点溶液中的溶质质量分数是多少?
向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图。据图回答:
(1)在滴加NaOH溶液过程中,原溶液中 离子个数不变。(填离子符号)
(2)P点溶液中的溶质是 。
(3)m1的值为 。
(4)M点溶液中的溶质质量分数是多少?