为测定某赤铁矿石中氧化铁的质量分数,某化学兴趣小组的同学用过量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用100g氢氧化钠溶液恰好完全吸收,形成不饱和溶液.该溶液总质量与反应时间的变化关系如图.试分析解答: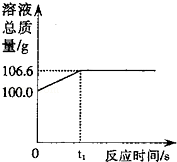
(1)赤铁矿石中所含主要物质的颜色为: .
(2)实验中多余的一氧化碳能否用水吸收? .
(3)上述反应中产生二氧化碳的质量为 g.
(4)计算实验结束后所得不饱和溶液中所含溶质的质量.
为测定某赤铁矿石中氧化铁的质量分数,某化学兴趣小组的同学用过量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用100g氢氧化钠溶液恰好完全吸收,形成不饱和溶液.该溶液总质量与反应时间的变化关系如图.试分析解答:
(1)赤铁矿石中所含主要物质的颜色为: .
(2)实验中多余的一氧化碳能否用水吸收? .
(3)上述反应中产生二氧化碳的质量为 g.
(4)计算实验结束后所得不饱和溶液中所含溶质的质量.