酸、碱、盐在生活、生产中应用广泛,使用时必须十分小心,氢氧化钠具有强烈的,实验时最好戴防护眼镜,为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请你根据要求完成下列问题:

(1)小丽同学发现,以前取用氢氧化钠溶液时试剂瓶忘记盖瓶塞,依据反应③说明
必须密封保存,否则在空气中要变质,如果该溶液变质,则发生反应的化学方程式为;
(2)要检验该氢氧化钠溶液已变质,选择下列试剂不能达到目的是
| A. |
稀 |
B. |
酚酞试液 |
C. |
|
D. |
|
(3)为了验证反应④,小丽将无色酚酞试液分别滴入
溶液和澄清石灰水中,溶液由无色变成红色,原因是它们在水溶液中能电离出。
(4)依据反应②,
能与下列物质反应的是.
| A. |
|
B. |
|
C. |
|
D. |
|
发生反应的化学方程式为:.
(5)硫酸铵[ ]、磷酸二氢钙[ ]、亚硝酸钠( )、硝酸钾( )等属于盐,其中又属于复合肥的。
现欲探究一固体混合物A的成分,已知其中可能含有NH4Cl、Cu(OH)2、BaSO4、CaO、NH4 NO3五种物质中的两种或多种。按下图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应均恰好完全反应)
试根据实验过程和发生的现象判断:
(1)常温下,气体B的水溶液显_________(填“酸性”“中性”“碱性”之一)。
(2)滤渣D的化学式是_________________。
(3)固体混合物A中,一定存在的物质是(写化学式)___________________________。
(4)滤液C中,一定大量存在的金属离子是(写离子符号)________________________。
(5)写出过程③中可能发生的一个化学方程式: 。
(6)固体混合物A中还不能确定存在的物质是(写化学式) ,得出此结论的理由是 。
已知某固体混合物A中可能含有
、
、
、
、
五种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理(设过程中所有发生的反应都恰好完全反应)。
I.取一定质量的该固体混合物A放入一洁净烧杯中,向其中加入适量
溶液,搅拌,待烧杯中物质充分反应后,过滤,得红褐色沉淀
和滤液
。
Ⅱ.另取一定质量的该固体混合物A放入另一洁净烧杯中,向其中加入适量
溶液,搅拌,待烧杯中物质充分反应后,过滤,得白色沉淀
和滤液
。
III.将所得滤液C和滤液E充分混合,再向混合后的溶液中加入适量
溶液,待充分反应后,过滤,得白色沉淀
和滤液
。
Ⅳ.根据上述实验过程和发生的现象做出相应推理,填写以下空白:
(1)在固体混合物A里,上述五种物质巾肯定存在的物质是(写化学式)
(2)写出步骤III中生成白色沉淀F的1个化学方程式
(3)在滤液
中,含有的金属阳离子共有种,该滤液中肯定存在的酸根离子。
(4)在混合物
里,上述五种物质中肯定不存在的物质是(写化学式)。得出此结论的理由是。
(5分)氯化钾固体样品中混有少量碳酸钾和硫酸钾两种杂质,为了获得纯净的氯化钾,将样品溶解,按如图所示步骤进行提纯。已知试剂I为氯化钡溶液.B、C为固体难溶物, 每步骤加稍过量的试剂:
(1)固体难溶物B含有碳酸钡和________;
(2)检验步骤①已除去杂质的方法(操作、现象、结论)是____________________________.
(3)试剂Ⅱ中溶质的化学式:________________________,试剂III的名称是__________;
(4)由E获得氯化钾晶体的分离操作名称是________________。
某化学小组向一定量
和
混合溶液中加入一定量的
粉,充分反应后过滤得溶液
和固体
.
对滤液
所含的溶质有以下几种猜想:
①
、
、
② 、
③ 、
④只有
经过讨论大家一致认为不合理的猜想是(填标号),其理由是.
【实验探究】若猜想④成立,通过以下实验可确定固体
的成分,请将下表填写完整.
| 实验步骤 |
现 象 |
固体
的成分 |
| 有气泡产生 |
某溶液由盐酸、稀硫酸、氢氧化钾、氯化镁中的一种或几种混合而成。现向该混合溶液中滴入氢氧化钡溶液,产生沉淀质量与加入氢氧化钡溶液体积如图所示。则
(1)该溶液中一定没有的溶质是 。
(2)a点对应的溶液中一定含有的溶质是 。
食盐是一种重要的化工原料。请回答下列问题。
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。
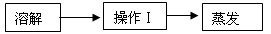
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和。
②在蒸发过程中,待时,停止加热,利用余热将滤液蒸干。
(2)由于粗盐中含有少量
,
、
等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。
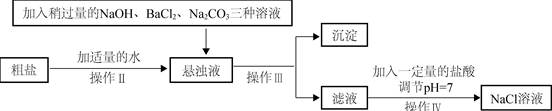
①加入稍过量的
溶液除了能除去粗盐中的
外,它还有一个作用是(用化学方程式表示)。
②通过操作Ⅲ所得滤液中的溶质有(用化学式表示)。
(3)若有溶质质量分数为10%的氯化钠不饱和溶液100 kg,要将其变成20 ℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是。已知:20 ℃时氯化钠的溶解度为36g。
(5分)通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下: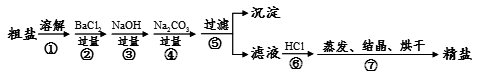
(1)用托盘天平称量粗盐时,若指针偏向右边,则表示(填下列正确选项的代码) _________ 。
| A.右盘重,砝码轻 | B.右盘轻,样品重 |
| C.左盘重,样品轻 | D.左盘轻,砝码重 |
(2)第②步操作的目的是除去粗盐中的 (填化学式,下同),第⑥步操作的目的是除去滤液中 ;
(3)第③步操作发生反应的化学方程式是_____________________________ ;
(4)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、CaCO3和__________(填化学式)。
(1)等质量的
、
两种物质分别与等质量的同浓度的稀盐酸充分反应,反应产生气体的质量与反应时间的关系如甲图所示。请回答下列问题:
①若
、
为
中的一种,则
是,反应结束后只有一种金属剩余,则剩余金属为。
②若
、
为碳酸钠粉末和碳酸钙块状固体中的一种,反应结束后,则它们消耗的酸(填"
多"、"
多"或"相等")。
反应至
点时,所得溶液的溶质为(写化学式)。
(2)如图所示,
、
、
、
、
分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,
是硝酸铜溶液。("-"相连两物质能发生反应)请回答:

①
的化学式为,
物质的一种用途:。
②
与
反应的化学方程式,基本反应类型是。
K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备K2SO4和Mn3O4的工艺流程如下:
【相关资料】(1)含水结晶盐受热时通常先失去结晶水;
(2)图2中物质B就是工业产品Mn3O4 ;
(3)Mn3O4在高温时会被氧化,且锰的化合价从+1到+7变化时逐级升高,如+2的锰先氧化到+3的锰,再从+3氧化到+4分别是对应的氧化物为三氧化二锰和二氧化锰。
【问题解答】
(1)反应II中加入的NH4HCO3中氮元素的化合价为 ;
(2)反应Ⅲ中,向(NH4)2SO4溶液中加入KCl溶液充分反应后,进行蒸发浓缩、结晶、 、洗涤、干燥等操作即得K2SO4晶体;
(3)试分析反应Ⅲ后有K2SO4析出的原因是____________________________;
(4)加热MnSO4·H2O固体时第一次质量减少的原因是 (用化学方程式表示);
(5)煅烧过程中固体锰元素的质量分数随温度的升高而增大。但当温度超过1000℃时,再冷却后,测得产物中的锰元素的质量分数反而减小。试分析产物中锰元素的质量分数减小的原因: 。
科学兴趣小组在调查一化工厂时,发现有个车间排出的废水澄清透明,呈黄色.为测定该废水中所含的物质,他们进行如下实验(假设能发生的反应均恰好完全反应):
(1)用pH试纸测试,测得pH为2.
(2)取一定量废水溶液,加入Ba(NO3)2溶液,无现象.
(3)另取一定量废水溶液,加入AgNO3溶液后,过滤,得到白色沉淀A和滤液.
(4)向滤液中加入NaOH溶液,得到红褐色沉淀B.
由此可知:该废水溶液呈 性;所得的红褐色沉淀B为 ;废水溶液中肯定含有的盐是 .
对知识的归纳和总结是学好科学的重要方法.在学习了酸碱的性质后,小红同学总结了稀盐酸和氢氧化钙的化学性质(如图),


(1)为了验证氢氧化钙与酸碱指示剂反应,小红将无色酚酞试液滴入氢氧化钙溶液中,溶液由无色变成____________色
(2)利用氢氧化钙与碳酸钠反应的性质,可以除去氢氧化钠溶液中少量的氢氧化钙杂质,请写出该化学反应的方程式______________________.
(3)利用稀盐酸的化学性质,可以去除铁锈,请写出方程式_______________________
(4)老师告诉同学们:对于酸和盐的反应,可以用厨房中的常见物品进行实验,其中能发生反应的两种物品是 和 (填名称或俗称)。
(5)工业上采用石灰浆雾滴技术除去废气中的二氧化硫,在此对石灰浆进行雾化处理的目的是________________________
实验室有一瓶无色溶液,老师告诉同学们该溶液可能是
溶液、
溶液、
溶液中的一种,请你和同学们一起来参与探究,并回答问题:
(1)取少量该溶液于试管中,滴加酚酞试液,溶液变红色,则原溶液不可能是溶液;
(2)另取少量该溶液于试管中,滴加
溶液,产生(填实验现象),则该溶液为
溶液,其反应的化学方程式为。
某白色固体由
、
、
、
中的三种组成,取样后加入足量的水,充分搅拌后,有白色沉淀生成,则原固体混合物的组成可能有(填序号)
①
、
、
②
、
、
③
、
、
④
、
、
过氧化钙晶体﹝
﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒。以贝壳为原料制备CaO2流程如下:

(1)气体
是
,其名称是;将过氧化钙晶体与溶液分离的方法是。
(2)反应
需控制温度在
,可将反应容器放在中,该反应是化合反应,反应产物是
,请写出化学方程式。获得的过氧化钙晶体中常含有
杂质,原因是。
(3)
的相对分子质量为,过氧化钙晶体﹝
﹞中
、
元素的质量比为。
(4)为测定制得的过氧化钙晶体中
的质量分数,设计的实验如下:称取晶体样品
,加热到
充分反应(方程式为
,杂质不发生变化),测得生成氧气的质量为
,请计算样品中
的质量分数(
相对分子质量为
),写出必要的计算过程。
(1)冬季,大雪覆盖路面,给交通造成很多麻烦,散撒融雪剂可以使雪很快融化,有效地清除交通雪障。除使用融雪剂外,常使用铲雪车铲雪,铲雪车的铲斗是用锰钢制造的,锰钢属于 (填写序号字母)。
| A.合成材料 | B.合金 | C.金属材料 | D.复合材料 |
(2)氯化钙是常用的融雪剂。工业上以碳酸钙(含有少量Na+、Mg2+、Fe3+等杂质)生产氯化钙的主要流程如下:
①滤渣的主要成分是 、 (填化学式);
②加盐酸酸化,其目的之一是除去未反应的氢氧化钙,写出反应的化学方程式 ,该反应属于 反应(填基本反应类型)。
(3)已知盐酸盐(金属氯化物)跟AgNO3溶液反应生成白色沉淀。某公司生产的融雪剂由NaCl、NaNO3、MgCl2、CuSO4中的两种物质组成。小明为探究其成分,设计并完成下列实验:
请你推断:融雪剂中一定不含的物质是 (填写名称),融雪剂中一定含有的物质是 (填化学式)。