盐城濒临黄海,海盐文化全国知名.某兴趣小组同学去盐场参观,带回了部分粗盐样品,并对其进行了如下探究:
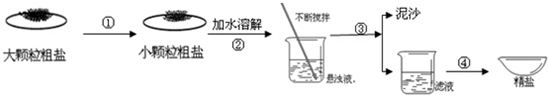
(1)操作①中必须用到的一种仪器是(填序号)
| A. | 研钵 | B. | 量筒 | C. | 烧杯 | D. | 试管 |
(2)操作③的名称是,操作④中用到玻璃棒,作用为.
(3)用提纯得到的"精盐"配制100g 7.5%的氯化钠溶液.经检测,溶质质量分数偏小,其原因可能有(填序号)
①氯化钠固体不纯
②称量时精盐与砝码放反了
③量取水时俯视读数
④装瓶时,有少量溶液洒出
(4)查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质(假定可溶性杂质只有
一种),为了得到较纯净的氯化钠,小组同学将所得的"精盐"又作了如下处理:
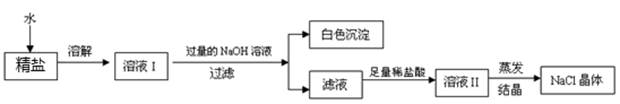
①白色沉淀的化学式为.
②在得到的滤液中加入足量的稀盐酸的目的是.
③若实验过程中不考虑损耗,最终到的
固体的质量将(填"大于"、"小于"或"等于")原精盐中
的质量.
如图所示,若将稀硫酸比作初三学生,要求在“应急演练”中按照“距离最短”的原则从楼顶入口处由上至下疏散到出口处,已知各层都有三道门(空白处为通道),稀硫酸要在每层中各打开一道门(即能与稀硫酸反应的物质)后才能到达出口处。请分别写出疏散路线上依次发生反应的化学方程式,并按要求填空。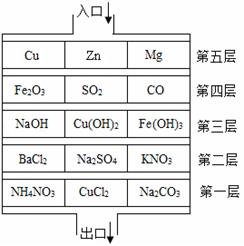
(1)第五层: ,该反应的基本反应类型是 ;
(2)第四层: ,反应前后溶液的颜色变化为 ;
(3)第三层: ,该反应属于 (选填“吸热”或“放热”)反应;
(4)第二层: ;
(5)第一层: ,该反应的基本反应类型是 。
(6)若将稀硫酸改为稀盐酸,则在疏散路线上无法通过第 层。
(11分)小明同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.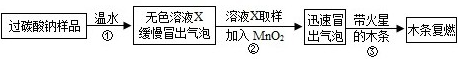
【探究一】小组同学根据所学的化学知识设计并进行了如图所示的实验.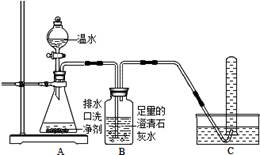
要保证实验的效果,实验装置要有良好的气密性,检查A装置气密性的方法是_________.实验中观察到如下现象:A中有气泡产生;B中的澄清石灰水变浑浊;C中收集到的气体能使燃着的木条燃烧更旺.由此同学们得出结论:生成的两种气体分别是_______、________(填化学式).
【探究二】
(1)实验过程:教师提供了一瓶过碳酸钠(Na2CO4),
小组同学进行了如下实验探究:
(2)提出问题:无色溶液X中的溶质有哪些物质?
(3)猜想与假设:根据以上实验现象,X溶液中一定存在的溶质是 _____;还可能存在Na2CO3、NaHCO3、NaOH中的一种或几种.写出上述实验探究中②反应的化学方程式__________.
(4)查找资料:
资料1:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;
氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3+CaCl2═CaCO3↓+2NaCl
资料2:NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同.
(5)实验过程:小组同学对溶液X中的溶质进行了如下实验.请将下列实验方案填写完整.
| 实验操作 |
主要实验现象 |
结论 |
| ①____________________ |
_____________ |
证明溶液中有Na2CO3 |
| ②_________________ |
______________ |
证明溶液中既无NaHCO3又无NaOH |
(6)实验反思:①根据资料,Na2CO4与水反应的化学方程式为________________.②Na2CO3、NaHCO3两种物质性质上既有共性又有差异,其差异性可用于鉴别、______等.
纳米碳酸钙是一种重要的无机化工产品,下图是某厂生产纳米碳酸钙的工艺流程。
请回答下列问题:
(1)请完成并配平该工艺中生成CaCO3固体的反应方程式:
CaCl2+_________+CO2=CaCO3↓+__________+H2O
(2)若在实验室中进行该实验,操作l的名称是___________,使用到的非玻璃实验用品有_________、________。
(3)上述过程制得的碳酸钙粗品表面可能含有的可溶性杂质有___________(写一种化学式即可)。操作2为:_________、检验和干燥,检验操作中选用的试剂为____________(选择序号)。
①NH4Cl溶液 ②AgNO3溶液 ③CaCl2溶液 ④Ba(NO3)溶液
(4)上述流程中的副产品可用作_______________________________(写一种用途)。
海水是巨大的资源宝库,利用海水为原料获得许多化工产品的流程如下图: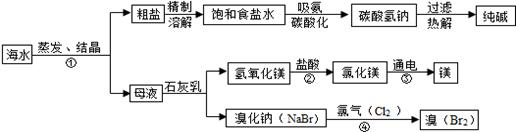
(1)实验室去除粗盐中难溶性杂质的一般步骤是:溶解、过滤、 、计算产率;
(2)步骤①中选用蒸发结晶而不用降温结晶的理由是 。
(3)由上述流程图看出碳酸氢钠的热稳定性 (填“大于、小于或等于)纯碱的热稳定性。
(4)步骤②发生的反应属于 反应(填一种基本反应类型)。用镁制造的一种镁铝合金常用作生产飞机外壳的材料,该材料具有的优良性能有 (任答一点)。
(5)步骤④发生的反应为置换反应(类似于金属与盐溶液之间的反应),
反应后溴元素的化合价比反应前 (填“升高”或“降低”或“不变”)。
(6)通过海水为原料制取纯碱中会含有杂质氯化钠,为了测定纯碱中杂质氯化钠的质量分数,小阳同学进行了三次实验,实验数据如下表:
| 编 号 |
第 1 次 |
第 2次 |
第 3次 |
| 所取固体样品的质量/g |
13 |
10 |
10 |
| 样品用98g水溶解后,加入CaCl2溶液的质量/g |
100 |
100 |
125 |
| 反应后生成沉淀的质量/g |
8 |
8 |
8 |
完成下列计算:
①固体样品中氯化钠的质量分数是 ;
②第 2 次反应结束后溶液中溶质质量分数是多少?(写出必要的计算题过程)
化工生产中需要对原料提纯,以利于提高产品质量。经测定某氯化钠样品中混有硫酸钠,为了除去杂质并制得纯净的氯化钠固体,在实验室研究中某学生设计方案如下:
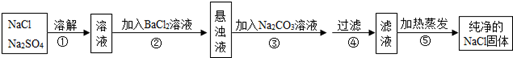
回答下列问题
(1)操作②能否用硝酸钡溶液?说明理由;
(2)进行操作②后,如何判断硫酸钠已除尽,方法是;
(3)操作③的目的是,③、④操作顺序能否交换,其理由是;
(4)此设计方案是否严密,说明理由.
以下是我们日常生活中常用各种清洗剂。
| 名称 |
洗涤灵 |
洁厕灵 |
炉具清洁剂 |
活氧彩漂 |
污渍爆炸盐 |
| 产品样式 |
 |
 |
 |
 |
 |
| 有效成分 或功能 |
清洗油污 |
盐酸 |
氢氧化钠 |
过氧化氢 |
过碳酸钠 |
(1)我们使用洗涤灵清洗餐具上的油污,这是因为它具有 的功能。
(2)清除以下物质,可以使用洁厕灵的是 填字母序号)。
A.铁锈 B.水垢(主要成分为碳酸钙和氢氧化镁)
C.油渍 D.氢气还原氧化铜实验后,试管内壁残留的红色固体
(3)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2。将爆炸盐溶于水后,再加入足量的洁厕灵,产生能使澄清石灰水变浑浊的气体,这一反应了体现右图中 (选填①②③④)性质关系。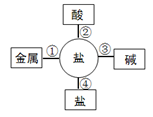
(4)将洁厕灵滴入炉具清洁剂中,如图甲所示。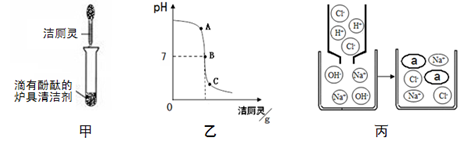
①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外) ;此时溶液可用图乙中 点处(选填A、B、C)表示。
②若反应后溶液pH为7,图丙中a微粒的化学式为 。
(5)①“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(—O—O—)。据此推测,下列物质中,可用作杀菌消毒剂的是 (填序号)。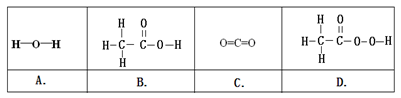
②氧化氢溶液常用于医用消毒,某兴趣小组为测定一瓶久置的医用过氧化氢溶液中溶质质量分数。他们取该溶液51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示。试计算该过氧化氢溶液中溶质的质量分数。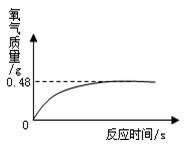
(写出计算过程)