湖南省郴州市初三初中毕业学业考试适应考试化学试卷
水是一种重要的资源。下列说法正确的是
| A.硬水中加入肥皂水容易起浮渣 |
| B.通过沉淀、过滤、吸附、消毒可将海水淡化 |
| C.澄清的泉水是纯净水 |
| D.过量地使用化肥不会导致水体污染 |
“加多宝凉茶”、“百事可乐”、“神农谷矿泉水”等这些生活中常见的饮料属于
| A.酸 | B.盐 | C.氧化物 | D.混合物 |
焊接金属时,能用作保护气的一组气体是
| A.氮气、氩气 | B.氮气、氧气 | C.二氧化碳、氧气 | D.氢气、氮气 |
下列说法错误的是
| A.“酒香不怕巷子深”说明分子是不断运动的 |
| B.分子是保持物质性质的最小粒子 |
| C.原子是化学变化中的最小粒子 |
| D.分子可以化分成原子,原子可以构成分子 |
下列是生活中常用的物质,其中属于天然有机高分子材料的是
| A.纯棉袜子 | B.不锈钢保温杯 |
| C.一次性尼龙袜子 | D.一次性塑料杯 |
化学反应前后各元素化合价肯定不发生改变的是
| A.化合反应 | B.复分解反应 | C.置换反应 | D.分解反应 |
(NH4)2SO4是一种常见的化学肥料,该物质中氮元素的化合价是
| A.+3 | B.-3 | C.+5 | D.-5 |
钛和钛合金被认为是21世纪最重要的金属材料,它具有熔点高、密度小、抗腐蚀性强等优良性能,广泛应用于军事、船泊、化工等。已知钛原子的质子数是22,中子数是24,则钛原子的核外电子数、相对原子质量分别是
| A.22 46 | B.22 24 | C.24 22 | D.24 46 |
蚂蚁会分泌一种信息素(C10H18O),下列关于该信息素的说法正确的是
①由碳、氢、氧元素组成 ②由多种原子构成的化合物
③碳、氢、氧元素的质量比为10∶18∶1 ④一个信息素分子中含有29个原子
| A.①③ | B.②③ | C.①④ | D.②④ |
下列是我们生活中经常用到的一些日用品,它们的水溶液的pH分别列于下表,其中属于酸性物质的是
| 牙膏 |
肥皂 |
食醋 |
食盐 |
| 10 |
12 |
4 |
7 |
A、牙膏 B、肥皂 C、食醋 D、食盐
下列对溶液的叙述,不正确的是
| A.无色透明的液体一定是溶液 |
| B.水是常见的溶剂 |
| C.溶液中可能有多种溶质 |
| D.饱和溶液降温后,不一定有晶体析出 |
某同学为探究镁、锌、铜、银的活动性顺序,设计如图试验流程。依据流程设计,下面对物质①②的选择合理的是
| A.①稀硫酸 ②硝酸银 |
| B.①稀盐酸 ②硫酸锌 |
| C.①稀盐酸 ②硫酸亚铁 |
| D.①稀硫酸 ②氯化镁 |
向一定量硫酸和硫酸铜的混合溶液中,逐滴加入一定质量分数的氢氧化钠溶液,直至过量。某同学依据实验事实绘制了如图所示的曲线,下列说法正确的是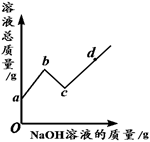
| A.a至b段对应溶液的pH逐渐减小 |
| B.b点对应溶液中的溶质为硫酸钠 |
| C.c点对应溶液中的溶质种类最少 |
| D.a至d段硫酸钠的质量逐渐增大 |
实验室常用二氧化锰与浓盐酸反应制取氯气,其反应化学方程式为:
MnO2+4HCl(浓) MnCl2+Cl2↑+2X根据上述已配平的化学方程式,可知X的化学式为
MnCl2+Cl2↑+2X根据上述已配平的化学方程式,可知X的化学式为
| A.H2O | B.H2 | C.H2O2 | D.HClO |
下列对一些事实的解释不正确的是
| |
事 实 |
解 释 |
| A. |
用碳素墨水书写档案 |
常温下单质碳的化学性质稳定 |
| B. |
石墨能够做电池的电极材料 |
石墨较软 |
| C. |
焦炭可以把铁从它的氧化物矿石里还原出来 |
焦炭具有还原性 |
| D. |
制糖工业中用活性炭来脱色以制白糖 |
活性炭具有吸附性 |
某固体混合物由Mg和MgO组成,取该混合物6.4g与一定量稀硫酸恰好完全反应(反应后溶液中无晶体析出),所得溶液中溶质的质量为24g,则原混合物中氧元素的质量为
| A.4.8g | B.3.2g | C.2.56g | D.1.6g |
请用化学用语表示:
(1)2个氢原子 ;
(2)-1价的氢氧根 ;
(3)钙离子 ;
(4)10个水分子 .
化学与我们生活息息相关。用下列生活中常见物质来完成以下各题:(用序号填空)
①甲烷 ②生石灰 ③熟石灰 ④小苏打 ⑤水银
(1)属于最简单的有机物的是 ;
(2)属于盐的是 ;
(3)属于碱的是 ;
(4)属于单质的是 。
(5)属于氧化物的是 ;
下图是A、B、C三种物质的溶解度曲线,根据此图回答下列问题:
(1) ℃时,物质A和C的溶解度相等。
(2)t2℃时,A物质的溶解度是 g。
(3)等质量的A、B、C三种物质的饱和溶液同时从t2℃降温到t1℃,其中溶质质量分数没有发生改变的是
(4)t2℃时,小红向100g的水中加入45.8gA物质,她发现A物质全部溶解,一段时间后,她意外地发现又有部分A物质的晶体析出。我认为A物质“全部溶解”的原因是因为A物质溶解时 (填“吸热”或“放热”)引起;析出晶体的原因是
下图是元素周期表中1-3周期的原子结构简图,据图回答相关问题。
(1)请画出8号元素原子结构示意图 ;该元素在化学反应中容易 (填“得到”或“失去”)电子,12号元素、8号元素和1号元素一起形成的化合物的化学式为 ;
(2)已知,Al(OH)3 既可以与盐酸等强酸反应,也可以与强碱NaOH反应生成偏铝酸钠(NaAlO2)和水,写出Al(OH)3与NaOH反应的化学方程式 ;
(3)归纳第2周期元素原子结构中核外电子排列的规律: (任写一条)。
化石燃料为人类社会的进步起到了不可估量的作用。
(1)煤、石油和 并称三大化石燃料, 后者燃烧的化学方程式是
(2)化石燃料属于(填“可再生”或“不可再生”)__________能源。煤燃烧会产生二氧化碳、二氧化硫、一氧化碳等气体,这些气体中,溶于雨水会形成酸雨的是 。
(3)随着全球经济的不断增长,人类对能源的需求更高,为此,人类正努力开发新能源。目前正在开发和使用的新能源有潮汐能、氢气、 (填一种)等。氢气作为21世纪极具开发前景的新能源之一,理由是 (任填一个);
(1)冬季,大雪覆盖路面,给交通造成很多麻烦,散撒融雪剂可以使雪很快融化,有效地清除交通雪障。除使用融雪剂外,常使用铲雪车铲雪,铲雪车的铲斗是用锰钢制造的,锰钢属于 (填写序号字母)。
| A.合成材料 | B.合金 | C.金属材料 | D.复合材料 |
(2)氯化钙是常用的融雪剂。工业上以碳酸钙(含有少量Na+、Mg2+、Fe3+等杂质)生产氯化钙的主要流程如下:
①滤渣的主要成分是 、 (填化学式);
②加盐酸酸化,其目的之一是除去未反应的氢氧化钙,写出反应的化学方程式 ,该反应属于 反应(填基本反应类型)。
(3)已知盐酸盐(金属氯化物)跟AgNO3溶液反应生成白色沉淀。某公司生产的融雪剂由NaCl、NaNO3、MgCl2、CuSO4中的两种物质组成。小明为探究其成分,设计并完成下列实验:
请你推断:融雪剂中一定不含的物质是 (填写名称),融雪剂中一定含有的物质是 (填化学式)。
实验室提供了下图所示的仪器。回答下列问题:
(1)写出图中标示仪器的名称:A ,F
(2)用大理石和稀盐酸反应制取二氧化碳,应选用的仪器是 (填写字母序号),药品加入的先后顺序是 ,该反应的化学方程式为 ,实验室检验二氧化碳的方法是 。
(3)实验中要节约药品,应该严格按照实验规定的用量取用。如果没有说明药品的取用量,液体一般按 取用。
一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如下图所示。
要求同学们进行探究:
确认这瓶溶液到底是什么溶液?
提出猜想:王老师提示:这瓶无色溶液只能是以下四种溶液中的一种:
①硫酸镁溶液、 ②硫酸钠溶液、
③硫酸溶液、 ④硫酸铵溶液。
查阅资料:
A:常温下,相关物质的溶解度如下
| 物质 |
MgSO4 |
Na2SO4 |
(NH4)2SO4 |
H2SO4 |
| 溶解度 |
35.1g |
19.5g |
75.4g |
与水任意比互溶 |
B:(NH4)2SO4的水溶液显酸性
【实验探究】
(1)通过查阅资料,小明同学认为猜想 (填序号)不成立,原因是 。
(2)为确定其它几种猜想是否正确,小明同学继续进行探究:
| 实验步骤 |
实验现象 |
实验结论 |
| a取该溶液少许于试管中,向其中滴加几滴氢氧化钠溶液 |
溶液中有白色沉淀生成 |
猜想①成立 |
| b取该溶液少许于试管中,向其中滴加几滴紫色石蕊溶液 |
|
猜想③成立 |
小芳同学认为小明实验步骤b的结论不正确,她的理由是 ;
(3)请你设计实验方案,确认该溶液是硫酸铵溶液并完成实验报告:
| 实验操作 |
实验现象 |
实验结论 |
| 取该溶液少许于试管中,再往该溶液加入 溶液,加热。 |
|
猜想④成立,该反应的化学方程式为 |
甘油是重要的化工原料,可以用来制造塑料,合成纤维、炸药等。甘油化学式是C3H8O3。请按要求计算:
(1)甘油中碳、氢、氧的原子个数比是 。
(2)甘油的相对分子质量是 。
(3)3.68g甘油中氧元素质量是 克。
某硫酸厂废水中含有少量硫酸,为达标排放,技术员小张对废水中硫酸的含量进行检测。
(1)配制溶液:欲配制溶质质量分数为4%的NaOH溶液100g,需要NaOH固体 g,水 ml(水的密度为1g/cm3);
(2)检测分析:取废水样品100g,向其中逐滴加入NaOH溶液至恰好完全反应时,消耗4%的NaOH溶液20g(假设废水中其它成分均不和NaOH反应)。 试计算废水中硫酸的质量分数?
课外化学兴趣小组的同学利用某化工厂的废碱液(主要成分为Na2CO3、还含有少量NaCl)和石灰乳(氢氧化钙的悬浊液)为原料制备烧碱,并对所得的烧碱粗产品的成分进行分析和测定。
【查阅资料】①碱石灰是CaO与NaOH的固体混合物,可吸收二氧化碳和水;
②CO2+Ba(OH)2 ═ BaCO3↓+H2O。
【粗产品制备】
(1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为 。
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品。
【粗产品成分分析】
(1)取适量粗产品溶于水得澄清溶液,加入Ba(NO3)2溶液出现白色沉淀,由此该粗产品中一定不含有 ,理由是
(2)该小组同学通过对粗产品成分的实验分析,确定该粗产品中含有三种物质。
【含量测定】Na2CO3含量的测定:
该兴趣小组的同学设计了下图所示的实验装置。取20.0g粗产品,进行实验。
(1)实验过程中需持续缓缓通入空气,其目的是 。
(2)下列各项措施中,不影响测定准确度的是______(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.取消上图中D装置
(3)实验中准确称取20.0g粗产品,进行测定,测得BaCO3质量为1.97g。则粗产品中碳酸钠的质量分数为 。
(4)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是 。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号