某中学进行的实验操作考查,制定了四个考签:a.O2的制取;b.CO2的制取;c.配制50g10%的NaCl溶液;d.粗盐提纯。每个同学抽取一个考签进行实验。
①甲同学抽签后来到实验室,发现本组实验桌上主要准备了下列仪器和药品:
上图中仪器E的名称为(6),甲同学抽到的考签应该是(7)(填实验名称),该实验的原理为(8)(用化学方程式表示),应选用的仪器有(9)(填字母代号)。
②乙同学在完成“配制50g 10%的NaCl溶液”实验过程中,需称量NaCl(10)g,溶解NaCl时用到的玻璃棒,其作用是(11)。
③丙同学抽到的考签为用氯酸钾制氧气,其反应的化学方程式为(12),制取过程中所用二氧化锰起(13)作用,氧气的收集方法是(14)。
为了除去氯化钠样品中的碳酸钠杂质,某兴趣小组将样品溶解后进行如下实验: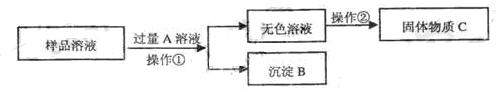
(1)A溶液中溶质可能为____________(只写一种);
(2)将无色溶液与沉淀B分离的操作①的方法名称是_____________;
(3)从无色溶液得到固体物质C的操作②的方法名称是____________;
(4)因为A溶液过量,此方案得到的固体物质C中混有新的杂质,为了既能除去杂质碳酸钠,又能有效地防止新杂质的引入,可向样品溶液中加入过量的_____________后,直接进行操作②即可得到纯净的氯化钠固体。
研究性学习小组选择下列某些仪器制取气体。
(1)写出仪器名称a b
(2)该小组同学要制取二氧化碳气体,写出该反应的化学方程式:______ _ ____ _______ ,此时发生装置应该选用上图中的________,收集二氧化碳的装置可以用________ 。
(3)实验室用A装置制取氧气的化学反应方程式:___________________________________
(4)某化学兴趣小组按照课本实验方法(如图),
做木炭与氧化铜反应实验,证明该反应的现象_________________,该反应的化学方
程式为__________________________________,其中单质碳具有__________性(填“氧化性”或”还原性”)
请根据下图实验装置图回答问题:
(1)写出仪器a,b的名称:a是 ,b是 .
(2)用A装置制取氧气的化学方程式是 ,可选用的收集装置是 (填序号).
(3)实验室用B、E装置制取CO2的化学方程式为 ,请写出用澄清石灰水检验二氧化碳时发生反应的化学方程式: 。若将发生装置由B改为F,其优点是 。
(4)将一瓶二氧化碳气体正立于烧杯中(装置见下图),敞口一会儿,集气瓶外壁上湿润的蓝色石蕊试纸自上面而下变红色,该现象说明分子具有 的性质,还说明二氧化碳气体 .
(5)某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验。实验装置如图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止。测得反应前后的有关质量如表:

①计算石灰石样品中CaCO3的质量分数。
②若在上述实验过程中石灰石样品和所加酸液均无抛洒,根据图中装置判断,该实验结果可能 (填“偏大”、“偏小”或“准确”),原因是 。
如图所示的是实验室常用的制备气体的实验装置,根据要求回答下列问题。
(1)如何检查A装置的气密性
(2)实验室用高锰酸钾制取氧气应选用的装置是 (填字母),
反应的化学方程式为 。
(3)实验室可用氧化钙固体与浓氨水在常温下混合制取少量氨气,为了得到平稳的氨气流,应选择的发生装置是 (填字母)
(4)收集某气体的方法,主要取决于这种气体的性质。在标况下,氨气的密度为0.771g/L,且氨气极易溶于水,所以收集氨气是应选用的装置是 。(填字母)
三瓶失去标签的无色溶液分别是盐酸、氢氧化钙溶液、碳酸钠溶液,某同学将其编号为A、B、C,且各取少量进行分析,得到以下实验结果:
| 实验 |
A+B |
A+C |
B+C |
| 现象 |
产生沉淀 |
产生气泡 |
无明显现象 |
(1)A是__________,B是__________,C是__________;(填物质化学式)
(2)写出A+B反应的化学方程式为____________________;B+C反应的化学方程式为____________________。
海水是一种重要的自然资源。以下是我市对海水资源的部分利用。
(1)从海水中获取淡水。常用的操作方法是 (填一种即可);
(2)从海水中获得氯化钠。将海水进行 可得到粗盐;
(3)从海水中得到金属镁。下图是从海水中提取镁的简单流程。
上述过程中,试剂A可由生石灰和水反应得到,此反应为反应 (填“放热”或“吸热”) ;可通过 (填操作名称)得到沉淀B。
海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:
。
小明用图A所示装置测定空气中氧气的含量.

(1)实验时,取下橡胶塞,点燃红磷后迅速伸入集气瓶中并旋紧橡胶塞,这时看到的现象是 ,该反应的文字表达式为 ;
(2)小明又设计了如图B所示的改进装置,其优点是___________________(只需写一点)。从理论上分析,玻璃管内液面最终将上升至________处(填“1”、“2”、“3”、“4”),但实测结果液面往往偏低,其原因可能是______________________________(只需写一条);
(3)他在一本参考书上发现,镁居然能在氮气中燃烧.于是他用镁代替红磷做起了这个实验,实验完毕,你认为进入集气瓶中水的体积_________(填大于、小于或等于)总容积的1/5。
精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
【物质制备】利用绿矾制备精还原铁粉的工艺流程如下: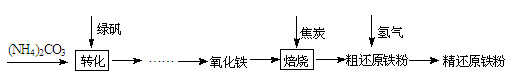
粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为: 、
、 。
。
(1)写出焙烧中氧化铁与CO反应的化学方程式 。
(2)焙烧中加焦炭的作用除了可以作燃料提供反应所需高温外,还能 。
【含量测定】甲同学为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按如下装置进行实验。已知:3CH4+4Fe2O3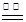 3CO2+6H2O+8Fe ,浓硫酸有吸水性,碱石灰不仅能吸收水而且能吸收CO2。(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响)。
3CO2+6H2O+8Fe ,浓硫酸有吸水性,碱石灰不仅能吸收水而且能吸收CO2。(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响)。
(3)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;
③点燃C处酒精灯;
④点燃A 处酒精灯;
⑤分别熄灭A、C处酒精灯;
⑥ ;
⑦再次称量必要装置的质量。
(4)步骤②的目的是 ,验证该步骤目的达到的实验方法是 。
(5)反应后C装置中的现象是 。
(6)装置F的作用是 。
(7)若缺少装置D,则所测氧元素的质量分数将 (“偏大”、“偏小”或“不变”)。
(8)实验后,甲同学根据装置 (填A、B、C、D、E、F)的增重分别算得样品中氧和碳元素的质量分数。
(9)乙同学将10.0克粗还原铁粉样品与足量稀盐酸充分反应,经测定共产生0.3克气体。计算该粗还原铁粉样品中铁单质的质量分数。(要求写出计算过程)
利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如下(反应条件已略去): 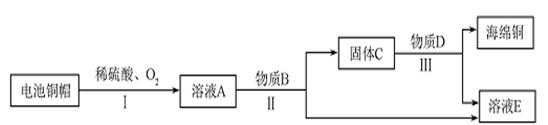
已知:2Cu+2H2SO4+O2 2CuSO4+2H2O 、Zn+CuSO4= ZnSO4+Cu
2CuSO4+2H2O 、Zn+CuSO4= ZnSO4+Cu
(1)过程中I中稀硫酸过量的目的是 。
(2)过程Ⅱ中分离操作的名称是 ,在操作过程中使用到的玻璃仪器有烧杯、玻璃棒和 ,其中玻璃棒的作用是 。
(3)过程Ⅲ中有气体产生,该气体是 (填化学式)。
(4)A~E 中含铜、锌两种元素的物质有 (填字母序号)。
(5)为了得到纯净的海绵铜,过程Ⅲ中过滤后应 、干燥。
用集气瓶可以完成多种实验。请根据如下实验示意图,回答有关问题。
(1)实验Ⅰ完成的实验是 ,实验Ⅱ的广口瓶中装入的试剂是 ,
(2)实验室利用Ⅰ和Ⅲ的装置制取氧气的化学方程式是 ;
(3)实验Ⅳ的集气瓶中预先加入了少量水,其作用是 ;
(4)实验Ⅴ观察到的现象是 ;
(5)下图装置可用于气体的收集、检验、除杂和体积的测量等,不能完成的实验是 (填序号)。
| A.气体从a端通入,收集氧气 |
| B.瓶内装有润湿的红色石蕊试纸,气体从a端通入,检验氢气中是否混有氨气 |
| C.瓶内装有氢氧化钠溶液,气体从b端通入,吸收一氧化碳中混有的二氧化碳 |
| D.在b端接量筒,瓶内装满水,测量气体的体积 |
某同学对一瓶失去标签的溶液进行鉴定,并测定其溶质的质量分数,他进行了如下实验:
(1)取少量该溶液,倒入一洁净的试管中,加入少量稀硫酸和稀硝酸的混合溶液出现白色沉淀,他由此得出的结论是原溶液中含有 离子;
(2)从试剂瓶中取5克溶液,倒入一洁净的烧杯里,加入0.5毫升的稀硝酸,然后用滴管滴入AgNO3溶液,出现白色沉淀。他由此得出的结论是原溶液是 溶液,继续滴加AgNO3溶液至不再生成沉淀为止;
(3)将(2)中得到的液体进行过滤,在此玻璃棒的作用是 ;
(4)将(3)中得到的沉淀物取出充分干燥后称量其质量为0.1克,若沉淀的相对分子质量为n,原溶液中溶质的相对分子质量为m,则原溶液中的溶质质量分数为 ;
(5)在上述实验中,有一处错误操作是 。这一错误操作对所测溶液的溶质质量分数的影响是 。(填“偏大”或“偏小”)
下图是某同学做“净化黄泥水”实验时的过滤装置图:
(1)图中还缺少的一种仪器是 ,其作用是 。
(2)指出图中另外还有一处明显错误: ,此处错误导致的后果是 。
蔬菜的搭配饮食很有讲究,某同学对“菠菜中富含可溶性草酸盐和碳酸盐,与豆腐同食会引起结石”的说法很感兴趣,于是对这一问题进行了探究。
探究:菠菜里是否含有可溶性草酸盐和碳酸盐?
【查阅资料】
①可溶的草酸盐、碳酸盐能与CaCl2溶液反应生成难溶于水的草酸钙(CaC2O4)、碳酸钙。
②醋酸(化学式用HAc表示)不与草酸钙反应,但能与碳酸钙反应生成可溶性盐。
【实验流程】
根据流程回答问题:
(1)操作①的名称是 。
(2)加入足量CaCl2溶液的目的是 。
(3)已知气体D能使澄清石灰水变浑浊,步骤③中发生反应的化学方程式为: 。
【实验结论】菠菜里含有可溶性草酸盐和碳酸盐。
【问题讨论】菠菜中含有大量的草酸盐,而普通豆腐中含有大量的钙,菠菜和豆腐一起吃可形成不溶性的沉淀,从而导致结石。但豆腐中富含钙和蛋白质,菠菜中也含有大量的营养成分,如七大营养素中不能被直接消化和吸收的 等都是人体必需的。所以,合理搭配饮食非常重要。