浙江省杭州市余杭区初中联盟学校初三上学期期中化学试卷
一辆满载浓硫酸的槽罐车在路上因车祸翻倒,浓硫酸大量泄漏,为了不污染旁边的水源,下列采取的措施适宜的是
| A.用水冲洗泄漏的浓硫酸 | B.将熟石灰撒在泄漏出的浓硫酸上 |
| C.将氯化钡撒在泄漏出的浓硫酸上 | D.用土将泄漏出的浓硫酸掩埋 |
如图,实验室中用碳酸钙与盐酸反应制取CO2气体,此CO2气体中常含有水蒸气和氯化氢气体若要除去这两种气体杂质,可将生成的气体通过甲、乙两个洗气瓶,通过导管的正确顺序是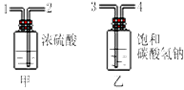
| A.①②③④ | B.②①③④ |
| C.④③②① | D.③④②① |
分类是学化学的方法之一,下列物质是按氧化物、盐、混合物顺序排列的是
| A.蒸馏水、大理石、澄清石灰水 | B.酒精、硫酸钠、泥浆水 |
| C.氧化铜、高锰酸钾、冰水混合物 | D.干冰、碳酸钙、空气 |
将36.5克稀盐酸和40克氢氧化钠溶液混合,充分反应,则所得溶液的pH值
| A.一定等于7 | B.可能等于7 | C.一定大于7 | D.一定小于7 |
除去下列各物质中的少量杂质所选用的试剂及操作方法均正确的是
| 项目 |
物质 |
杂质(少量) |
试剂 |
操作方法 |
| A |
KNO3 |
MnO2 |
足量的水 |
溶解、过滤、蒸发结晶 |
| B |
H2 |
水蒸气 |
适量的NaOH溶液 |
洗气 |
| C |
硝酸 |
盐酸 |
过量的硝酸银溶液 |
过滤 |
| D |
CO |
CO2 |
足量氧化铜 |
加热 |
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与 加入Zn的质量关系如图所示,下列说法正确的是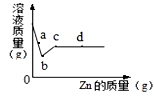
| A.a点溶液中的溶质有3种 |
| B.b点溶液是无色的 |
| C.若取b~c段溶液,滴加稀盐酸,有白色沉淀 |
| D.c点的固体中含有银、铜、锌 |
甲、乙、丙、丁四种物质之间转化关系如图所示,则物质甲可能是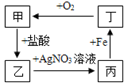
| A.Fe2O3 | B.CuO | C.Mg | D.Cu |
下列关于科学实验中“操作-现象-结论”的描述正确的是
| A.在某固体物质中加入稀盐酸,产生大量气泡,该物质一定是碳酸盐 |
| B.在某溶液中加入氯化钡溶液和稀硝酸,产生白色沉淀,该溶液中一定含有硫酸根离子 |
| C.某化肥与碱共热,若产生使湿润红色石蕊试纸变蓝的气体,证明为铵态氮肥 |
| D.在稀盐酸与氢氧化钠反应后的溶液中滴加无色酚酞试液不变色,可以断定两者恰好完全反应 |
下列实验设计能够成功的是
| |
实验目的 |
实验操作 |
| A |
实验室制备二氧化碳 |
将石灰石和稀硫酸混合后加热 |
| B |
证明铁、铜、银的活动性强弱 |
向盛有少量的氯化亚铁、氯化银的两支试管中,分别加入大小相同的铜片 |
| C |
除去氯化钠固体中的少量碳酸钠 |
加入过量的稀盐酸,充分反应后,蒸发结晶 |
| D |
除去硫酸钠溶液中少量氯化钠杂质 |
向含有氯化钠杂质的硫酸钠溶液中加入适量的硝酸银溶液,过滤 |
为研究某一镁铝合金的成分,进行甲、乙、丙三组实验。三组各取30 mL同浓度的盐酸溶液,加入该种镁铝合金粉末。每组实验加入合金质量和产生气体质量的有关数据如下:
| 实验序号 |
甲 |
乙 |
丙 |
| 合金质量(g) |
0.153 |
0.255 |
0.385 |
| 气体质量(g) |
0.015 |
0.025 |
0.03 |
根据表中的数据可判断
A.甲组盐酸不足量 B.乙组盐酸不足量
C.丙组盐酸不足量 D.甲、乙、丙三组均盐酸过量
长期暴露在空气中的氢氧化钠易吸收空气中的 而变质。为检验其是否变质,请选择三种不同物质类别(酸、碱、盐)的试剂进行实验,写出所选试剂的化学式:酸 ;碱 ;盐 。
铁粉和硫粉以适当的质量比混合,堆放在石棉网上,然后用烧红的玻璃棒一端接触混合物,这时部分混合物迅速变红热状态,撤离玻璃棒后,反应继续进行,直至全部混合物都呈红热的状态,冷却后得到一种黑色的固态物质。
(1)该黑色固态物质在物质分类上属于 (选填“酸”、“碱”、“盐”或“氧化物”)。
(2)铁与硫的反应是 反应(选填“吸热”、“放热”或“既不吸热也不放热的”)。
(3)可以证实反应中铁已从游离态变成化合态的方法是 。
(4)该反应的化学方程式为 。
(5)从理论上计算,为使铁粉和硫粉都能全部反应,两者最佳质量比应是 。
某同学对一瓶失去标签的溶液进行鉴定,并测定其溶质的质量分数,他进行了如下实验:
(1)取少量该溶液,倒入一洁净的试管中,加入少量稀硫酸和稀硝酸的混合溶液出现白色沉淀,他由此得出的结论是原溶液中含有 离子;
(2)从试剂瓶中取5克溶液,倒入一洁净的烧杯里,加入0.5毫升的稀硝酸,然后用滴管滴入AgNO3溶液,出现白色沉淀。他由此得出的结论是原溶液是 溶液,继续滴加AgNO3溶液至不再生成沉淀为止;
(3)将(2)中得到的液体进行过滤,在此玻璃棒的作用是 ;
(4)将(3)中得到的沉淀物取出充分干燥后称量其质量为0.1克,若沉淀的相对分子质量为n,原溶液中溶质的相对分子质量为m,则原溶液中的溶质质量分数为 ;
(5)在上述实验中,有一处错误操作是 。这一错误操作对所测溶液的溶质质量分数的影响是 。(填“偏大”或“偏小”)
实验室有一气体发生装置产生的无色气体可能含有H2、CO、CO2、HCl中的一种或几种,现将气体通过以下装置。
实验现象如下:B处由紫色变成红色;C处有白色沉淀生成;D处有白色沉淀生成;F处由黑色变成红色;G处由白色变成蓝色;H处无现象。
(1)无色气体肯定含 。
(2)由长颈漏斗加入的酸是 ,锥形瓶中装入的固体是少量 和 的混合物。
(3)E装置是为了排除对验证 的影响。
(4)E装置中浓硫酸(选填“能”或“不能”) 换成浓氢氧化钠。
(5)如果B装置中的试纸不变色,则可省去 、 装置(填装置代号)。
镁是一种银白色的金属,但实验室看到的镁条常常有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?甲同学认为可能是Mg0:乙同学认为可能是Mg2(OH)2CO3;丙同学认为可能是Mg(OH)2。
(1)丁同学认为甲的猜想是错误的,理由是 。
(2)丁同学按图所示的装置进行实验,发现被加热的试管内生成白色固体,且试管口有液滴出现,另一只试管内的澄清石灰水变浑浊。由此,丁同学认为丙的猜想也是错误的,其理由是 。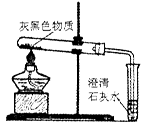
(3)大家查阅资料后又知道:Mg(OH)2和Mg2(OH)2CO3加热后均可分解,产物均为氧化物。据此请写出Mg2(OH)2C03受热分解的化学方程式 。
学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如Al2O3是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白。
【提出问题】Al2O3是否可以作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3可能可以作过氧化氢分解的催化剂。
【实验验证】
| |
实验步骤 |
实验现象 |
实验结论 |
| 实验一 |
|
有少量气泡 木条不复燃 |
常温下过氧化氢溶液分解速率很慢 |
| 实验二 |
在装有过氧化氢溶液的试管中加入少量 Al2O3,然后将带火星的木条伸入试管中 |
产生大量的气泡 木条复燃 |
|
【得出结论】Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂.
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验三:
实验三:【实验目的】探究
【实验步骤】①准确称量Al2O3(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤,洗涤,干燥,称量;④对比反应前后Al2O3的质量。
【交流讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂。
【提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究 。通过补充实验,证明Al2O3能作过氧化氢分解的催化剂,请你写出实验二中的化学反应方程式 。
已知氯化镁样品中含有杂质氯化钠,某化学兴趣小组的同学通过以下实验测定其中氯化镁的质量分数:称取该样品15g溶于水得到溶液,然后将一定溶质质量分数的氢氧化钠溶液100g平均分四次加入其中,充分振荡(实验数据见下表)。
| |
第1次 |
第2次 |
第3次 |
第4次 |
| 加入氢氧化钠溶液的质量/g |
25 |
25 |
25 |
25 |
| 生成沉淀的质量/g |
2.9 |
x |
8.7 |
8.7 |
(1)表中x = 。
(2)样品中氯化镁的质量分数是 。
(3)若实验室中只有80g质量分数为30%的氢氧化钠溶液,要想配成本实验所需溶质质量分数的氢氧化钠溶液,还需加入水的质量是多少?


 粤公网安备 44130202000953号
粤公网安备 44130202000953号