根据反应事实可以推出影响化学反应的因素,下列推理中不合理的是
| 选项 |
化学反应事实 |
影响因素 |
| A |
木炭在纯氧中燃烧的火焰比在空气中燃烧的火焰更明亮 |
反应物浓度 |
| B |
粉末状大理石与盐酸反应比块状大理石更加剧烈 |
反应物种类 |
| C |
红磷在常温下与氧气不发生反应,加热后能与氧气反应 |
反应温度 |
| D |
双氧水在通常情况下难分解,加入二氧化锰后迅速分解 |
催化剂 |
元素化合价发生改变的反应都是氧化还原反应。例如: ,反应前后, 和 元素的化合价发生了改变,该反应是氧化还原反应。下列反应不属于氧化还原反应的是
| A. | |
| B. | ↓ |
| C. | ↑ |
| D. | ↑ ↑ |
下列各组变化中,每个转化在一定条件下均能一步实现的是
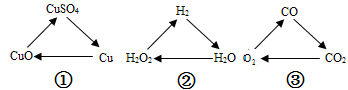
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
下列图像不能正确反映其对应关系的是()
| A. |
|
| B. |
|
| C. |
|
| D. |
|
将燃着的镁条伸入到盛有 的集气瓶中,镁条剧烈燃烧,发出强光,生成一种黑色固体和一种白色固体。你认为下列说法中不正确的是
的集气瓶中,镁条剧烈燃烧,发出强光,生成一种黑色固体和一种白色固体。你认为下列说法中不正确的是
A.某些金属(例如镁)着火时不能用 灭火器进行灭火 灭火器进行灭火 |
B.在反应 中,镁是还原剂 中,镁是还原剂 |
C.该反应的实质是镁条与 中的 中的 反应 反应 |
| D.该反应说明燃烧不一定要有氧气参与 |
右图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.下列能说明 密度大于空气且能与水反应的现象是( )
密度大于空气且能与水反应的现象是( )

| A.①变红,③不变红 | B.④变红,③不变红 |
| C.①、④变红,②、③不变红 | D.④比①先变红,②、③不变红 |
如下图所示:若关闭Ⅱ阀打开I阀,紫色小花(用石蕊溶液染成)变红;若关闭I阀打开Ⅱ阀,紫色小花不变红。则甲瓶中所盛的试剂可能是:①浓H2SO4(有强吸水性) ②浓NaOH溶液(能大量吸收CO2 ) ③饱和NaCl溶液

| A.只有① |
| B.只有② |
| C.①② |
| D.①②③ |
下列4个坐标图分别表示4个实验过程中某些质量的变化,其中不正确的是
| A.向一定量过氧化氢溶液中加入少量二氧化锰 |
| B.向相同质量与浓度的稀盐酸分别加入足量的铁粉和锌粉 |
| C.向相同质量的铁粉和锌粉中分别加入足量稀盐酸 |
| D.一氧化碳与一定量氧化铁在高温条件下完全反应 |
二氧化碳在高能真空紫外线照射下能直接产生氧气,该化学反应模型如图所示,下列说法错误的是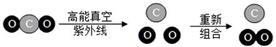
| A.反应中没有发生变化的微粒是碳原子和氧原子 |
| B.该反应属于分解反应 |
| C.反应前后元素化合价均没有发生改变 |
| D.为制取氧气提供了新方法 |
对右图实验的分析说明不正确是
| A.该实验说明一氧化碳具有还原性 |
| B.该实验说明生成物二氧化碳的密度比空气大 |
| C.该实验说明一氧化碳和氧化铜的反应需要加热 |
| D.该实验可以防止一氧化碳污染空气,同时充分利用能源 |
科学研究发现:金星大气层的成分之一是三氧化二碳(C2O3),实验证明三氧化二碳的化学性质与一氧化碳相似.下列关于三氧化二碳的说法中,不正确的是
| A.C2O3能使澄清石灰水变浑浊 |
| B.C2O3在O2中充分燃烧的产物为CO2 |
| C.C2O3在一定条件下能还原氧化铁 |
| D.C2O3中碳的化合价为+3价 |
将氮气、一氧化碳、二氧化碳的混合气体先通过足量澄清石灰水,再通过足量灼热的氧化铜,最后剩余的气体是( )
| A.氮气 | B.二氧化碳 | C.一氧化碳 | D.二氧化碳和氮气 |
实验表明:不能用块状大理石与稀硫酸制取二氧化碳气体,而能用大理石粉末与稀硫酸制取二氧化碳气体。由此得出的合理结论是
| A.能发生反应的物质之间是否发生反应,与反应的条件有关 |
| B.反应物之间接触面积越大,越有利于反应的进行 |
| C.块状大理石与大理石粉末的化学性质不同 |
| D.块状大理石与大理石粉末中各元素原子间电子的结合状况不同 |
下图是碳还原氧化铜的实验装置,相关说法错误的是
| A.反应前碳粉与氧化铜应充分混合 |
| B.Ⅱ中澄清石灰水变浑浊 |
| C.理论上Ⅰ中减少的质量可能等于Ⅱ中增加的质量 |
| D.反应结束时应先停止加热,待冷却后再将导管移出试管 |
在下列实验中,观察到的现象或得出的结论,完全正确的是

①浓氨水中出现红色,说明氨分子很小且不断运动
②既能说明甲烷有可燃性,又能说明甲烷是由碳和氢两种元素组成
③既能说明二氧化碳的密度比空气大,又能说明二氧化碳不能燃烧也不支持燃烧
④既能探究可燃物的燃烧条件,又说明白磷的着火点比红磷低
⑤铁钉表面无明显现象,能说明铁生锈的条件是要有氧气和水
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |