同学们在学习了木炭还原氧化铜的实验后,联想到单质碳的一些化学性质,对反应后的气体成分产生了疑问,某学习小组对该反应产物中的气体成分进行了探究。
〔猜 想〕
①气体产物全部是CO2 ②气体产物全部是CO ③气体产物 ①
〔查阅资料〕CO气体能使湿润的黄色氯化钯试纸变蓝色。
〔设计实验〕根据各自的猜想,他们共同设计了如下图的实验装置进行探究。

〔现象与分析〕
| 现象 |
结论 |
| 如果装置B ② ,装置C无现象 |
则猜想①成立 |
| 如果 ③ |
则猜想②成立 |
| 如果_________ ④ __ |
则猜想③成立 |
〔结论〕实验现象证明猜想③成立,同学们的疑问是合理的。
〔反思〕
(1)同学们对CO产生的原因进行了分析:
①原因一:木炭和氧化铜在高温条件下直接发生反出产生CO;
②原因二:反应 中的一种产物和反应物木炭又发生了化学反应,产生了CO;
中的一种产物和反应物木炭又发生了化学反应,产生了CO;
请你从原因一、原因二中选择其一,用化学方程式表示存在此原因的化学反应原理_________________⑤_________________。
(2)根据上述实验,请你归纳出单质碳在工业上的重要用途 ⑥
(3)从环保角度考虑,该套实验装置的明显缺陷是 ⑦
蚁酸(化学式为HCOOH)在一定条件下会分解生成两种氧化物。
【提出猜想】蚁酸分解的两种氧化物是什么
(1)甲同学根据蚁酸中含有 元素,推测出一种生成物是水;
(2)另一种生成物是气体,乙同学对该气体提出两种猜想:
猜想①:该气体是CO2; 猜想②:该气体是 。
【实验设计】乙同学将蚁酸分解产生的气体通过如下图所示装置(铁架台未画出):

【讨论交流】
Ⅰ.根据实验现象,A中溶液 浑浊(填“变”或“不变”),就能否认猜想①。
Ⅱ.装置B中的发生反应的化学方程式是 ,装置C的作用是 。
【讨论交流】从环保角度看,该装置的缺陷是 。
【拓展延伸】丙同学提出:蚁酸分解生成的两种氧化物中,如果一种是水,另一种氧化物就一定不是CO2。从理论上分析,其理由是 。
“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来了。”
小红看到这段话后非常感兴趣,她和同学们一起对该问题进行了探究。
[查阅资料]氢氧化钠、氢氧化钾、氢氧化钙等物质能使无色酚酞溶液变红。
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想]①可能有一种气体和另一种物质生成②反应过程中可能有能量变化
[设计装置]如右图所示

[实验探究]
实验一:探究反应后生成的气体是什么?
(1)打开右图装置中分液漏斗的活塞,控制滴加水的速度,
观察到试管内有气泡产生,用带火星的木条靠近P处,
木条复燃。说明生成的气体是______ _______;
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:_______________
实验二:探究反应后生成的另一种物质是什么?
(1)小军猜想另一种物质可能是Na2CO3,但小红通过设计实验:向溶液中滴加少量稀盐酸,无气泡产生,证实不存在 CO32-;
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,小军预测反应中应有
生成;
[表达]由实验探究的结果,写出过氧化钠和水反应的化学方程式:_ ____。
王丽对家中的家用制氧机产生了浓厚的兴趣。她通过阅读说明书了解到家用制氧机的工作原理如下:加压时,装填在制氧机内部的分子筛吸附空气中的氮气,制取高浓度氧气。减压时,分子筛将所吸附的氮气排放。整个过程中,分子筛并不消耗。王丽用这台家用制氧机制取并收集了一袋气体,带到实验室对其进行研究。
(1)这台家用制氧机制氧气的过程发生的变化属于 (填“物理”或“化学”)变化。
(2)实验I:小丽欲通过以下实验验证所收集的气体是否为纯净的氧气。
【实验记录】
| 实验步骤 |
实验现象 |
文字表达式 |
| 取一只250 mL的集气瓶,用排水法收集一瓶所带气体,然后把燃着的石蜡插入集气瓶中 |
石蜡燃烧得更旺 |
文字表达式I |
表中,文字表达式I是 。
【实验结论】收集的气体是纯净的氧气。
【实验反思】老师指出上述实验并不能证明小丽所带来的气体一定是纯净的氧气。该实验不能证明所收集气体为纯净氧气的原因是 。
(3)实验II:测定小丽所带气体中氧气的含量。同学们在老师的指导下设计了如下图所示装置,进行实验,并重复多次。
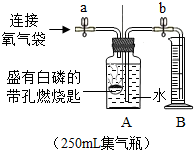
【实验记录 】
| 实验操作 |
主要实验现象 |
实验结论及解释 |
|
| ① |
检查装置的气密性 |
/ |
装置的气密性良好 |
| ② |
加入药品,将装置连接固定 |
/ |
/ |
| ③ |
打开止水夹a和b,向A中缓慢鼓入一定量气体后关闭止水夹a和b |
A中水进入到B中,B中水的体积为200 mL。 |
收集200 mL气体(由压强差引起的误差忽略不计) |
| ④ |
用凸透镜聚光引燃白磷 |
燃烧,产生大量白烟 |
/ |
| ⑤ |
待白磷熄灭并冷却到室温, 进行操作I |
现象I |
小丽收集的气体不是纯净的氧气 |
表中,操作I是 ;现象I是
出现上述现象的原因是 。
【数据记录】
| 实验次序 |
1 |
2 |
3 |
4 |
5 |
| B中剩余水体积/mL |
100 |
42 |
39 |
41 |
38 |
【数据处理】已知,在上表数据中,第1组数据偏差较大,存在明显误差,在数据处理时应删去。小丽所带气体中氧气的体积分数为 % 。
【实验反思】导致第1组数据产生较大误差的可能原因是
空气中氧气含量测定的再认识。
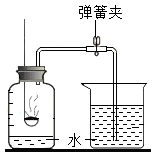
【实验回顾】如图是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。写出红磷燃烧的化学方程式_______________________。
步骤如下:
①用弹簧夹夹紧橡皮管。
②点燃燃烧匙内的红磷,立即伸入瓶中并塞紧塞子。
③_____________________________________。
④观察并记录水面的变化情况。
【实验反思】多次实验,发现集气瓶内上升的水的体积始终小于瓶内原空气体积的1/5。
【实验改进1】
I.根据铁在空气中生锈的原理(铁与氧气和水发生反应生成铁锈)设计右图实验装置,再次测定空气中氧气含量。装置中的食盐水和活性炭会加速铁生锈。
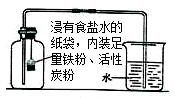
II.测得实验数据如表
| 测量项目 |
实验前 |
实验后 |
|
| 烧杯中水的体积 |
烧杯中剩余水的体积 |
集气瓶(扣除内容物)和导管的容积 |
|
| 体积/mL |
80.0 |
54.5 |
126.0 |
【交流表达】(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁,写出该反应的化学方程式____________________________________。
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是________。(消耗的水的体积忽略不计,计算结果保留一位小数)。
【猜想与假设】根据铁生锈的原理,某同学对最终生成的铁锈的主要成分作出猜想:
(Ⅰ)氧化铁(Ⅱ)碳酸铁,你认为猜想 (填序号)一定是错误的,理由是 。
【实验改进2】
使用右图装置进行实验。实验前应先进行的操作是______________________。

【实验过程】步骤1:在注射器中放入装有足量铁粉、活性炭粉的浸有食盐水的纸袋,封闭。
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹。
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化。
【数据处理】实验中需要记录的数据是___________________________________________。
计算得出氧气约占空气总体积的1/5。
【计算】铁的氧化物有多种,116g四氧化三铁与多少g氧化亚铁(FeO)中所含的氧元素质量相等。(写出计算过程)
【实验评价】与燃烧红磷法相比,用改进实验测定空气中氧气含量的优点是____________
____________________________________________。
(5分) 中央电视台举办的“3.15”晚会,曝出某品牌金饰品掺假的事件,引起同学们的好奇。某化学兴趣小组在老师的帮助下,对几种常见金属饰品所含的金属进行了相关的探究活动。
【提出问题】
(1)怎样鉴别真假黄金?(2)怎样确定钯的金属活动性?
【查阅资料】
(1)假黄金通常是黄铜(Cu-Zn合金);
(2)钯(Pd)呈银白色,有金属光泽,可用作饰品。
【实验药品】钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液
【实验探究】(1)鉴别黄金样品的真假
取黄金样品于试管中,滴加稀盐酸后,观察到黄金样品表面有气泡产生,该气体是 ,说明此样品为 (选填“真”或“假”)黄金。
(2)探究钯的金属活动性
依据生活经验,同学们猜想钯的活动性可能与银和铂相近,于是他们利用上述药品进行如下实验:
| 实验步骤 |
实验现象 |
实验结论 |
| 把钯浸入硝酸银溶液中 |
. |
钯的活动性比银弱 |
| 把铂浸入氯化钯溶液中 |
无明显现象 |
钯的活动性比铂 . |
初步得出结论:钯、银、铂的金属活动性由强到弱的顺序为 。
【废液处理】
(1)转化成沉淀。小组同学将所有液体倒入废液缸中,出现白色沉淀。
(2)通过科学合理的方法进一步回收金属钯。
利用如图所示的装置可进行一氧化碳还原氧化铁的实验,其中,氮气可用作本实验的保护气; 盛放氧化铁的是一支带有支管的试管,其支管可用于导出试管内的气体;酒精灯带网罩;整套装置的气密性良好.实验前,弹簧夹a、b均处于关闭状态,开始实验时,打开a,通入氮气一段时间后点燃酒精灯,再关闭a,打开b.请联系所学知识回答下列问题:
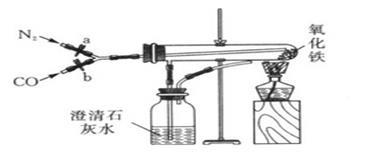
(1)该实验过程中可以观察到的现象有:_________________、_________________。
(2)试管内一氧化碳与氧化铁反应的化学方程式为____________________________。
(3)实验结束时,应先打开a,再___________,然后___________,继续通氮气直至装置冷却。(选填“A”或“B”)A.熄灭酒精灯 B.关闭b
(4)待试管冷却后,把生成的黑色粉末倒在白纸上后;用磁铁靠近黑色粉末,黑色粉末全部被吸引;再取少量黑色粉末放入足量硫酸铜溶液中,搅拌后发现黑色粉末部分变红。
【提出问题】炼出来的黑色粉末的成分是什么呢?
【查阅资料】在铁的氧化物中只有氧化铁是红棕色,其余都是黑色;只有氧化亚铁在空气中会很快被氧化成氧化铁;只有四氧化三铁有磁性。
【综合探讨】同学们得出此次炼铁得到的生成物是___________________。
(5)请从两个不同角度评价该实验的优点:_______________,_________________。
有人提出运用高科技可以使水变成汽油,小明认为可以用物质组成的观点揭开这个骗局。以下是小明的实验探究过程。
【提出问题】根据水的组成和汽油的组成判断,水是否可以变成汽油?
【猜想与验证】(1)探究水的组成。实验装置示意图如图:
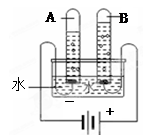
(1)通电一段时间后,经过检验可知,试管A中的气体是 。该反应的符号表达式为 。该实验说明:水是由 组成的(写名称)。
(2)探究汽油的组成。
实验操作如下:
| 实验步骤 |
实验现象 |
实验目的 |
| ①点燃使用汽油作燃料的油灯 |
  |
|
| ②将光洁干冷的小烧杯罩在油灯火焰的上方 |
现象:小烧杯内壁出现小水珠 |
证明汽油在空气中燃烧后的产物中有水 |
| ③将内壁蘸有 的小烧杯罩在油灯火焰的上方 |
现象: |
证明汽油在空气中燃烧后的产物中有二氧化碳 |
该实验说明:汽油的组成中肯定含有的元素有 (写元素符号)。
【得出结论】因为汽油和水的组成元素不同,所以水不能变成汽油。
下面是几位同学测量空气中氧气体积分数的四个实验,请你参与他们的探究:

[实验一]小强采用A图所示的装置进行实验:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推拉两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化。
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是 。
[实验二]:小红采用B图所示的装置进行实验:实验过程如下:
第一步:将集气瓶容积划分为五等份,并做好标记.
第二步:用放大镜点燃燃烧匙内的红磷.
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5.
请回答下列问题:
(1)集气瓶中剩余的气体主要是 ,根据实验推断它的化学性质有 。
(2)实验完毕,若进入集气瓶中水的体积小于总容积的1/5 ,其原因可能是 。
(3)红磷燃烧的现象是 ,其符号表达式为
[实验三]小华同学打算采用C图所示的装置进行实验:锥形瓶内空气体积为230mL,注射器中水的体积为50mL,该装置气密性良好。装入药品,按图所示连接好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
请回答下列问题:
(1)在整个实验过程中,可观察到气球的变化是___________________。
(2)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象是:①注射器中的水自动喷射出来,②当注射器中的水还剩 mL时停止下流。
[实验四]小明用图D装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
(1)冷却后打开止水夹,水能进入集气瓶的原因是 。
(2)若镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的 %,现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中还有 。
电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体。某化学兴趣小组对它的化学性质产生了浓厚的兴趣并进行下列探究。
【查阅资料】乙炔(C2H2)燃烧时伴有大量黑烟。氢气(H2)燃烧时发出淡蓝色火焰,用冷而干的烧杯罩在火焰上方烧杯内壁有水雾产生。CaO+H2O→Ca(OH)2。Ca(OH)2溶液能使酚酞变红。
【猜想与假设】
电石与水反应生成的可燃性气体是:O2、H2或乙炔(C2H2);电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙。
大家讨论后一致认为该气体不可能是O2,原因是 ,白色固体不可能是氧化钙,原因是 。
【实验探究】
| 实验步骤 |
实验现象 |
实验结论 |
| (1)取适量电石加水反应,收集生成的气体,验纯后点燃。 |
气体燃烧,产生黄色火焰并伴有浓烈黑烟。 |
电石与水反应产生的气体是 。 |
| (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸。 |
固体溶解, 。 |
电石与水反应产生的固体不是碳酸钙 |
| (3)取适量反应后生成的固体于试管中加水,向上层清液中滴加2~3滴 。 |
溶液变红 |
电石与水反应产生的固体是氢氧化钙 |
【反思交流】载有电石的货车可以在雨中整整燃烧一天而不熄灭,说明电石与水的反应是
(填“吸热”或“放热”)反应。
下列是初中化学的两个实验,按要求回答问题:
(1)某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:

①红磷在集气瓶中发生反应的文字表达式为
该实验可观察到的现象为
该实验中红磷稍过量,目的是
②由实验现象可得出的结论是
(2)某课外活动小组设计如图装置研究分子的性质:

① 向盛有约20ml蒸馏水的小烧杯①中加入5~6滴酚酞溶液,搅拌均匀观察到溶液
② 从上述烧杯①中取少量溶液置于试管中,向其中慢慢滴加浓氨水,观察到溶液
③ 另取一个烧杯②(如图),加入约5ml浓氨水。用一个大烧杯罩住①②两个小烧杯。过了几分钟,观察到
综合②③实验说明分子
反思:为什么两个烧杯不同时变色呢?
查阅资料:不同的分子在相同的条件下运动速率不同。
由此可根据现象推断 分子运动速率快(填氨或酚酞)。
【2015年福建省厦门市】用如图装置完成以下实验: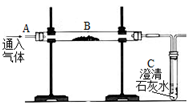
(1)探究燃烧条件:若B处盛放木炭。
Ⅰ.先在A处通入氮气一段时间后,在B处加热,B、C处没有明显变化;
Ⅱ.待B处冷却至室温,在A处通入氧气一段时间后,B、C处没有明显变化;
Ⅲ.在A处继续通入氧气,然后在B处加热,发现木炭燃烧,C处变浑浊。
Ⅰ与Ⅲ对比,说明燃烧的条件之一是____________;Ⅱ与Ⅲ对比,说明燃烧的条件之一是_____________。
(2)模拟工业炼铁:若B处盛放氧化铁粉末。在A处通入一氧化碳一段时间后,B处下方用喷灯加热,B处可观察到的现象为______________________________,尾气处理的方法为__________________________。《自然》杂志刊载“绿色炼铁”技术;电解熔融的氧化铁得到铁和氧气,该反应的化学方程式:_____________________,该炼铁技术另一种产物的用途为___________________________________。
(13)某校化学兴趣小组就空气中氧气的含量进行实验探究:

(1)小组同学设计了如右图所示的两套装置,你认为合理的是 (填字母)为了确保实验的成功,在装药品之前应该
(2)红磷在集气瓶中发生反应的文字表达式为 。该实验中红磷稍过量,目的是 。
(3)小组同学做完实验后发现水进入集气瓶的量远少于理论值.经讨论,同学们认为造成该现象的原因可能有_____________________或______________________
(4)若将红磷换成炭粉,该实验能否获得成功? ,理由是 。
(5)小淳同学对实验装置进行了大胆的改造,设计了如右图的装置。

请根据图示回答下列问题:
①闭合电源开关,可以观察到白磷
②装置冷却到室温时,可观察到U型管内左侧液面
③通过这个实验得出的结论是
④此实验还可推知反应后剩余气体的两点性质是:
在“空气中氧气含量测定”的实验探究中。甲同学设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内。塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温。打开铁夹,水注入集气瓶。回答下列问题。

(1)该实验中红磷需稍过量,目的是 。
(2)待燃烧停止、冷却后,打开止水夹,观察到烧杯中的水进入集气
瓶内水面最终接近刻度1/5处。由此可知氧气约占空气总体积的 。
(3)若将红磷换成炭粉,该实验能否获得成功? (填“能”或“不能”)。理由是 。
(4)实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果的可能原因(写2条)① ②
(5)由本实验还可以推测氮气的性质有(任写一种):
某小组的同学在课外进行科学探究,以验证铜片在空气中灼烧后,表面生成的黑色物质确实是铜与氧气化合生成的CuO,他们进行了以下实验:












(1)由上图两个实验步骤判断:铜片可能发生化学反应的是步骤 。(填“一”或“二”)
(2)为进一步证明步骤二铜片表面黑色物质的元素组成,他们选用了以下装置继续进行实验:

a.甲同学向A装置中通入纯净的H2,为检验反应产物,A的右边应连接上面的装置 _____
(填编号),所选装置的实验现象为 ,A装置中所发生的化学反应方程式为 _______ 。
b.乙同学向A装置中通入纯净的CO,A装置的实验现象为 ,为检验反应产物,A的右边应连接上面的装置 __ (填编号),所选装置中的实验现象为 ;此方法仅用上述装置有明显的缺陷,要弥补,应采取的措施是: 。
c.通入的气体如含有少量水蒸气,若在A装置左边增加一个B装置,则澄清石灰水应更换成______________。
d.对A装置加热前,应先通入纯净气体的目的是_________________________。
(3)结论:经过甲、乙两同学的实验现象证明 。