某固体可能由Na2SO4,NaCl,Na2CO3,KNO3中的一种或几种组成,现进行如下实验:
试回答:
⑴.白色沉淀A的化学式为________________;
⑵.原固体中一定含有_______________________,一定不含有_______________________,
可能含有____________________;
⑶.为检验上述可能含有的物质是否一定存在,某同学又设计了如下实验方案:(请补充完整)
取少量固体溶于水,____________________________________________________________。
A~H是初中化学常见的物质,它们之间的相互关系如下图所示,(“→”指向生成物。)其中B是红棕色粉末,A、C常温下均为气体,F是一种可溶性碱,反应③是复分解反应。请回答下面问题: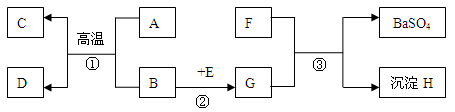
(1)物质E的化学式:
(2)反应① (填“是”或“不是”)置换反应。
(3)反应①的化学方程式是 。
(4)少量气体C通入F溶液中有白色沉淀产生,其化学方程式是 。
(5)一定量的物质D能与少量G在水溶液中能发生化合反应,且反应后溶液颜色呈浅绿色,则反应后溶液中的溶质是
天然气的主要成分是甲烷(CH4),某校化学兴趣小组的同学对甲烷燃烧的产物
产生了兴趣,请你参与:
【提出问题】:甲烷燃烧后生成哪些物质?
【查阅资料】:含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
【猜想与假设】:甲:CO2 、H2O ; 乙: CO、H2O;
丙: NH3 、CO2 、H2O; 丁: CO2 、CO、H2O 。
你认为 同学的猜想是错误的,理由是 。












 【实验探究】:为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列 装置:
【实验探究】:为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列 装置:
(1)A、B装置的顺序能否颠倒?(填“能”或“否”) ;
(2)实验中用纯净O2而不用空气的原因是 ;
(3)实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中黑色粉末变成红色,由此推断 同学猜想成立;
(4)请写出B中澄清石灰水变浑浊、C中黑色粉末变成红色的化学反应方程式:
、 。
(5分)实验室模拟炼铁原理进行实验,得到的尾气是CO、CO2的混合气体。现利用下图所示装置将混合气体进行分离,并得到干燥的气体。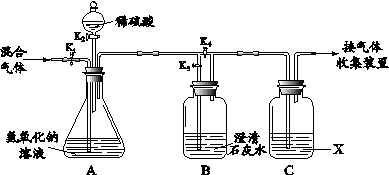
(1)检查装置的气密性。A、B、C装置内放入一定量水,使长导管浸没在水面以下,关闭k2、k4,打开k1、k3,并在最右端导管口接注射器。当向外缓慢拉动注射器活塞时,若观察到 ,则说明整套装置气密性良好。
(2)装入药品。C中所盛试剂X为 。
(3)分离两种气体。请完成下表(实验操作只需答出关闭和打开活塞即可)。
| 实验操作 |
分离出的气体 |
| |
|
| |
|
(4)在实验过程中,A中发生反应的化学方程式为 。
某实验小组根据下图所示装置探究燃烧的条件,请回答问题。 (1)检查装置气密性后,燃烧匙中放入少量的白磷,小烧杯内放入适量的碳酸钠粉末,组装好装置。打开弹簧夹,将溶液A缓慢加入到小烧杯内,溶液A是______,一段时间后,______(填写后续实验步骤和现象),关闭分液漏斗的活塞、弹簧夹,然后用凸透镜加热白磷,观察到白磷不燃烧,该实验过程的目的是______。
(1)检查装置气密性后,燃烧匙中放入少量的白磷,小烧杯内放入适量的碳酸钠粉末,组装好装置。打开弹簧夹,将溶液A缓慢加入到小烧杯内,溶液A是______,一段时间后,______(填写后续实验步骤和现象),关闭分液漏斗的活塞、弹簧夹,然后用凸透镜加热白磷,观察到白磷不燃烧,该实验过程的目的是______。
(2)停止加热,轻轻振荡装置,一段时间后打开弹簧夹,再用凸透镜加热白磷,观察到白磷燃烧,白磷燃烧的原因是______,该实验过程中发生反应的化学方程式为______。
人类的生存和发展离不开能源和资源。
(1)南京家用燃料的更新过程如下:
①下列有关家用燃料更新的理由,正确的是 (选填字母)。
A.天然气属于可再生能源
B.气体燃料比固体燃料利用率更高
C.天然气作为燃料可避免温室效应的发生
D.煤仅仅用作燃料烧掉浪费资源
②已知:同温、同压下,气体体积比等于分子个数比;管道煤气的主要成分是一氧化碳。原本以管道煤气为燃料的家庭若要改用天然气,灶具的改进方法可为 (选填字母)。
A.增大空气的进入量 B.增大天然气的进入量
C.减小空气的进入量 D.减小天然气的进入量
(2)水是生命之源,合理利用和保护水资源是我们义不容辞的责任。
①设法除去硬水中的 ,可以使硬水软化成软水。
②公共场所可利用“活性炭+超滤膜+紫外线”组合工艺获得直饮水,其中活性炭主要起 作用。
(3)海水中有大量可以利用的化学资源,其中所含的氯化镁是金属镁的重要来源之一。从海水中提取金属镁,可按下图流程进行: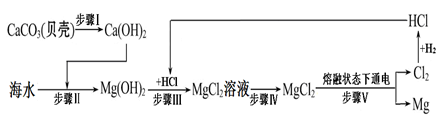
①下列有关说法正确的是 (选填字母)。
A.步骤Ⅰ通过一步反应即可实现
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁
C.步骤Ⅴ中化学能转化为电能
D.在此流程中涉及的基本反应类型有4种
②在此流程中可以循环利用的物质是 。
工业上以大理石和赤铁矿为主要原料制取B和G,其转化关系如右图所示,已知D、G为单质。
B的化学式为 ;反应①和③的化学方程式分别为 、

6分)实验小组对久置生石灰的成分进行分析,实验操作及部分现象如下图所示。
【资料:Na2CO3+CaCl2 =" 2NaCl" + CaCO3↓】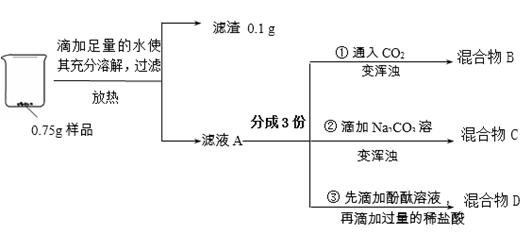
回答下列问题:
(1)样品加水放热的原因是 (用化学方程式表示)。
(2)②中反应的化学方程式是 。
(3)③中的实验现象是 。
(4)将混合物B、C、D倒入一个洁净的烧杯中,发现烧杯中有白色沉淀且上层清液呈红色,过滤,得滤液E和1 g滤渣。向滤液E中滴加CaCl2溶液,有白色沉淀生成,则滤液E中的溶质可能是 。
依据实验现象及数据判断,原样品的成分是 。
“海水晒盐”所获得的粗盐中,除含有泥沙等难溶性杂质外,还含有氯化镁、氯化钙等可溶性杂质,某化学小组为得到较纯净的食盐,进行了下列实验探究活动,请参与他们的探究活动。
[提出问题]如何获得较纯的食盐晶体?
[查阅资料]
20℃时,部分物质的溶解性
情况如下表所示:
| |
OH- |
CO32- |
| Na+ |
溶 |
溶 |
| Ca2+ |
微 |
不 |
| Mg2+ |
不 |
微 |
[实验方案]按如下方案进行提纯粗盐。
[解释与结论]
(1)实验操作X的名称是 ;沉淀D是 。
(2)为达到除去难溶性杂质的实验步骤是 。(填序号)
(3)实验步骤③的主要目的是 (用化学方程式回答);判断氢氧化钠溶液已过量的方法是 。
(4)在进行实验步骤⑤的蒸发时,为防止液体飞溅和获得相对更纯的食盐晶体需要进行的操作是 。
[反思与评价]
(5)有同学认为该实验方案并不完善,其理由及需补充的实验操作是 。
A-D分别是由一种或几种元素组成的初中常见的4种固体物质,按要求回答相应的问题:
(1)A投入某蓝色溶液中,会有一层红色的固体附在其表面,该红色固体是 。
(2)B是一种白色固体氧化物,能与水反应,向其溶液中通入二氧化碳后变浑浊,B与水反应的化学方程式是 。
(3)C溶液遇二氧化碳或碳酸钠溶液,均可以产生一种白色沉淀,C溶液中的溶质是 。(用名称表示)
(4)D与稀盐酸反应,生成一种无色气体,对于D的说法正确的是 。
①D一定是一种活泼金属 ②D可能是一种活泼金属
③D一定是一种碳酸盐 ④D可能是一种碳酸盐
⑤D可能含有三种元素,也可能含有四种元素。
一包白色粉末A由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的三种混合而成。为探究其组成,进行以下实验: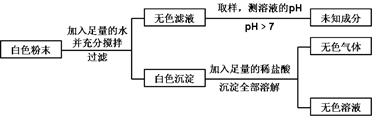
分析实验过程,回答:
①白色粉末A中一定有(8),一定没有(9);可能含有的物质是(10) 生成无色气体E的化学方程式是(11)。
② 对可能含有的物质,通过如下实验进一步确认:
| 实验操作 |
实验现象 |
实验结论 |
| 取未知成分溶液D少许,加入(12)溶液, |
(13) |
(14)。 |
(7 分)由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题。某化学研究小组的同学欲对某种塑料袋的组成进行分析研究,测定样品中元素的质量比,设计了如图所示的实验装置。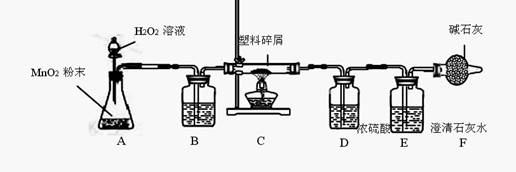
(小资料:该种塑料袋只含碳、氢两种元素,燃烧产物为二氧化碳和水。图中碱石灰可以吸收空气中的二氧化碳与水蒸气)
(1)按上面连接好装置,在装入药品之前,必须进行的操作是 。
(2)装置 A 中所发生的反应化学方程式为 。装置中 MnO2 粉末的作用是 。
(3)由于发生装置 A 制取的氧气中混有水蒸气,为不影响测定结果,装置B中盛放的试剂应该是_____________(写名称)。
(4)判断塑料袋试样中含有碳元素的依据是____________________________________。
(5)根据实验前后装置的质量变化测算出仪器D质量增重5.4g,仪器 E 质量增重 8.8g,则该塑料袋试样中碳元素与氢元素的质量比为______________。
(6)若实验过程中由于过氧化氢的量不足,塑料袋试样燃烧不充分,则该塑料试样中碳 元素与氢元素的质量比的测算结果 (填“一定偏大”、“一定偏小”、“基本一致”之一)。
有一包粉末,可能由NaCl、MgCl2、FeCl3、Na2CO3、Na2SO4中的一种或几种组成.为了探究该粉末的组成,进行了如下实验:
(1)取样加水溶解,得到无色透明溶液.
(2)取(1)所得溶液少许,加入NaOH溶液,观察,没有明显现象.
(3)另取少量粉末,滴加稀盐酸,观察,也没有明显现象.
根据上述实验可得到的结论是:原粉末一定不含 MgCl2、FeCl3、Na2CO3,可能含有的物质是 NaCl、Na2SO4.
初中化学中几种常见物质之间的相互转化关系如图所示。已知常温下B为气体,是植物进行光合作用的一种重要原料;D为无色液体;E为黑色固体(部分反应物和生成物及反应条件已略去)。下列有关判断正确的是
| A.A中一定含有碳酸根 |
| B.E可能是碳 |
| C.C转化为B一定是化合反应 |
| D.F由两种元素组成 |