下列指定反应的化学方程式正确的是( )
| A. |
镁条在氧气中燃烧:Mg+O 2 |
| B. |
古代湿法炼铜:2Fe+3CuSO 4═Fe 2(SO 4) 3+3Cu |
| C. |
用胃舒平[含Al(OH) 3]治疗胃酸过多:Al(OH) 3+3HCl═AlCl 3+3H 2O |
| D. |
用石灰石浆处理二氧化硫:SO 2+CaCO 3+O 2═CaSO 4+CO 2 |
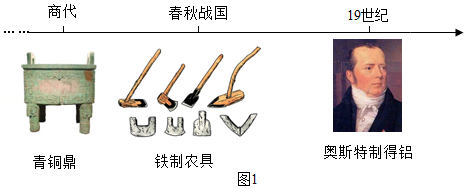
早在春秋战国时期,我国就开始生产和使用铁器,请根据所学知识回答下列问题:
(1)工业上常以赤铁矿为原料炼铁,请写出该反应的化学方程式 。
(2)据统计每年因腐蚀而报废的金属设备和材料相当于年产量的20%﹣﹣40%,铁制品锈蚀的过程实际上是铁与空气中的 等发生反应的过程。
CaCO 3在生产生活中有广泛的用途.
(1)煅烧石灰石可制得活性CaO,反应的化学方程式为 .为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等分,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如图1所示.可知:CaO与水反应会 热量(填"放出"或"吸收");上述温度中, ℃煅烧所得CaO活性最高.要得出正确结论,煅烧时还需控制的条件是 .
(2)以电石渣[主要成分为Ca(OH) 2,还含有少量MgO等杂质]为原料制备高纯CaCO 3的流程如下:

①如图为NH 4Cl浓度对钙、镁浸出率的影响(浸出率=  ×100%).可知:较适宜的NH 4Cl溶液的质量分数为 ;浸取时主要反应的化学方程式为 .
×100%).可知:较适宜的NH 4Cl溶液的质量分数为 ;浸取时主要反应的化学方程式为 .
②流程中虚线内部分若改用 溶液(填化学式),可一步得到与原流程完全相同的生成物.
③流程中虚线内部若改用Na 2CO 3溶液,也能得到高纯CaCO 3,试从生物的角度分析原流程的优点:
a.NH 3可循环利用;b. .

洪杰同学一家利用假日到郊外游玩,亲近自然,在游玩活动中,遇到一些有趣的化学问题,请认真阅读,解答下面的问题.
(1)化学与生活:
①野炊中,他取来一些清澈的泉水,进行了加热煮沸,从化学的视角看,给泉水加热煮沸既可以消毒杀菌,又可以 .
②他家的野炊食谱如下:主食;馒头;配菜;鸡蛋、牛肉干、花生米,从营养合理搭配的角度来看,你认为食谱中还应添加(填一种食品) 会更好.
(2)化学与能源:
①他找来一些木柴,准备做饭时,发现怎么也烧不着,并产生大量的黑烟,仔细观察发现木柴过于潮湿,后来它捡来一些干燥的木柴,解决了这个问题,请你利用燃烧的条件,解释潮湿木柴烧不着的原因 .
②新农村建设中,他发现许多村里安装了太阳能路灯,新建了沼气池,沼气的主要成分是甲烷,请你写出甲烷燃烧的化学方程式 .
(3)化学与工、农业生产:
①他在吃饭时,看到爸爸喝的是荆门市生产的"金龙泉"啤酒,盛装啤酒的铝制易拉罐的底部未经任何防腐处理,也没有腐蚀,原因是(用化学方程式表示) .
②他又看到一农民欲将碳酸氢铵与草木灰混用,他赶紧制止,其原因是 .
(4)化学与材料:
①他看到一位农民正用电烙铁对一破损的路灯塑料灯罩进行热修补,他告诉这位农民,塑料灯罩属于 (填"链状"或"网状")结构的高分子材料,一经加热成型,受热不会熔化,具有热固性,这种方法不能用于灯罩的修补.
②野炊结束后,剩下了大量的塑料食品包装袋,由此,他想到人类面临的"白色污染"的问题,请你为解决"白色污染"提出一条合理建议 .
烟台有漫长的海岸线,蕴藏着丰富的海洋资源。
(1)海水淡化。可以采用如图1所示的膜分离法淡化海水,水分子可以通过淡化膜(海水中体积较大的盐的离子和其他分子不能通过)进入左侧的淡水池,从而得到淡水。下列说法中正确的是 (填字母序号)。
A.膜分离法的原理与滤纸过滤原理类似
B.膜分离法还可以浓缩海水中的盐类物质
C.膜分离法也是一种分离混合物的方法
D.该膜分离法的目的是除去海水中的不溶物
(2)粗盐提纯。除去难溶性杂质后的食盐水中还含有Ca2+、Mg2+、SO42﹣等杂质离子,为得到较纯的氯化钠,进行如下的实验操怍①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液③加入过量的NaOH溶液; ④加入适量的盐酸调节溶液的pH等于7;⑤过滤;⑥蒸发。下列操作顺序正确的是 (填字母序号),其中操作④加入适量的盐酸调节溶液的pH等于7的目的是 。
A.①③②④⑤⑥
B.③②①④⑤⑥
C.③①②⑤④⑥
D.②③①⑤④⑥
(3)海水资源综合利用的部分途径如图2。
①氨碱工业生产过程中,在加压并不断向饱和的氨盐水中通入二氧化碳的条件下,使碳酸氢钠结晶析出,该反应的化学方程式是 。
②写出步骤Ⅰ电解饱和NaCl溶液的化学方程式是 。
③海水制镁。实际生产中,步骤Ⅲ常选用 作为沉淀剂,从海水中提取MgCl2历经步骤Ⅱ、Ⅲ、Ⅳ三步转换的主要目的是 。
含碳物质种类繁多。请回答下列问题:
(1)葡萄糖(C6H12O6)中C、H、O原子的数目之比是 。
(2)石墨烯和金刚石均为碳单质,但导电性差异很大,原因是 (填字母序号)。
a.原子的排列方式不同 b.原子在不断运动 c.原子的体积很小
(3)乙醇(C2H5OH)是 (填“可再生”或“不可再生”)能源,乙醇完成燃烧的化学方程式是 。该反应中,化学能转变为 能。
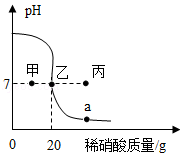
常温下,一锥形瓶中盛有20g溶质质量分数为4%的氢氧化钠溶液,先向其中滴加2滴酚酞试液,再逐滴滴加溶质质量分数为6.3%的稀硝酸,用pH传感器测得溶液的pH与加入稀硝酸的关系曲线如图。请回答问题:
(1)本实验反应的化学方程式是 。
(2)pH=7时,锥形瓶中的溶液呈 色,此时溶液的溶质质量分数是 (结果精确到0.01%)。
(3)图中a点对应的溶液中溶质的化学式是 。
(4)若改用溶质质量分数为12.6%的稀硝酸进行本实验,pH传感器测得的曲线可能经过
(填“甲”“乙”或“丙”)点。
2017年3月22日是世界水日,水是人类宝贵的自然资源,根据所学知识回答下列问题:
(1)火箭使用的燃料液氢在助燃剂液氧中燃烧的化学方程式为 .
(2)日常生活中通常向水中滴加 来检验硬水和软水.
(3)高铁酸钠(Na 2FeO 4)被广泛应用于自来水净化消毒,其原理为:
4Na 2FeO 4+10 =4Fe(OH) 3(胶体)+3 +8NaOH(请将化学方程式补充完整).
(4)水是常用的溶剂,某酒精(C 2H 5OH)的水溶液,溶质与溶剂中氢原子个数比为1:2,则该溶液中溶质的质量分数为 (精确到1%).
人类制得并利用金属有着悠久的历史:
(1)利用孔雀石冶炼铜的主要反应:①Cu 2(OH) 2CO 3 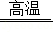 2CuO+H 2O+CO 2↑,该反应的类型是 反应(填"化合"、"分解"或"置换");
2CuO+H 2O+CO 2↑,该反应的类型是 反应(填"化合"、"分解"或"置换");
②2CuO+C  2Cu+CO 2↑,该反应前后铜元素化合价发生的变化是 。
2Cu+CO 2↑,该反应前后铜元素化合价发生的变化是 。
(2)高炉炼铁的主要反应过程如图2.请写出对应的化学方程式:
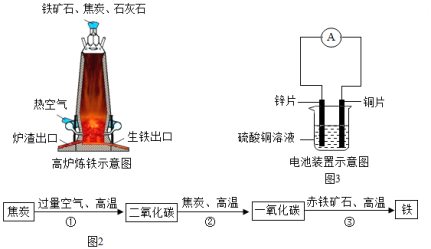
① ;② ;③ 。
(3)冶炼金属铝的主要反应:2Al 2O 3  4Al+3O 2↑,该反应的条件是 。图3装置中,两种金属的活动性:Zn Cu (填">"或"<")。当电流表指针发生偏转时,化学能转化为 。
4Al+3O 2↑,该反应的条件是 。图3装置中,两种金属的活动性:Zn Cu (填">"或"<")。当电流表指针发生偏转时,化学能转化为 。
我们已经学过实验室制取气体的一般思路和方法,请根据如图装置回答相关问题:
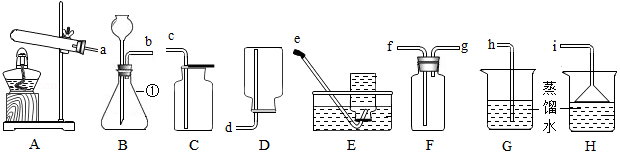
(1)写出图中仪器①的名称: 。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,该反应的化学方程式是 ;收集较纯净的氧气应选择的装置是 (填字母序号);B装置中长颈漏斗下端管口必须伸入液面以下的原因是 。
(3)氨气是一种无色气体,密度比空气小,极易溶于水,有刺激性气味,污染环境。加热氯化铵和熟石灰的固体混合物可制取氨气,实验室制取并收集氨气,所选装置的接口从左到右正确的连接顺序为 。
二氧化碳、氢氧化钠、氢氧化钙、氯化钠等都是重要的化工原料,在生产和生活中,有这重要的应用。
(1)二氧化碳用于制汽水,这是利用了二氧化碳 的性质。
(2)用石灰浆粉刷墙壁,干燥后又白又硬。这是因为(用化学方程式表示) 。
(3)厕所清洁剂和炉具清洁剂的作用是不同的。其中,炉具清洁剂中含有 ,利用其能与油脂反应的性质达到去除油污的目的。而厕所清洁剂因含有某些物质,呈强 (“酸”或“碱”)性,能达到消毒杀菌的效果。
(4)工业上,常用电解氯化钠溶液的方法制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为 。
CO 2的资源化利用日趋成为研究热点。
(1)某小组查阅资料发现:①CO 2与H 2能在催化剂表面反应生成CH 4与H 2O;②CH 4在高温下能与CuO反应。为探究上述反应,设计如下装置。

①仪器M的名称是 。装置B中反应的化学方程式为 。
②设计装置C的目的是 ,若要证明D中有CO 2生成,则需在E、F之间增加盛有 溶液的洗气瓶。
③一段时间后,装置D中黑色固体变红,E中白色固体变蓝,该小组由此得出结论:以上实验证明CH4在高温条件下能与CuO反应。你是否同意他们的结论? (填"同意"或"不同意"),理由是 。
(2)CH 4、乙炔(C 2H 2)和丙烷(CH 3H 8)都能在空气中燃烧,但是仅C 2H 2燃烧时有浓烟。试从物质组成的角度分析其燃烧现象不同的原因是: 。CH 4燃料电池具有洁净、高效的特点,其工作时主要是将 能转化为电能。
用化学式来表示化学反应的式子,叫做化学方程式。请写出下列反应的化学方程式:
(1)铁在氧气中燃烧 。
(2)硫酸铜溶液与氯化钡溶液反应 。
被誉为"中国天眼"的FAST,是目前世界上最大口径、最灵敏的射电望远镜,如图所示。请回答下列问题。
(1)选择角钢而不用纯铁作塔架的主要原因是 。
(2)角钢中含有锰(Mn)和硅,锰可以与稀盐酸发生置换反应,生成锰的化合物中锰元素显+2价。请写出锰与稀盐酸反应的化学方程式 。
(3)请你写出一条防止铁制材料生锈的具体措施 。
(4)向硝酸银和硝酸铜的混合溶液中加入一定量的铝粉,反应停止后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有 ;滤液中一定含有的溶质是 ,可能含有的溶质是 。(均填化学式)
