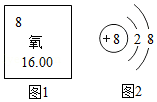
如图1是氧元素在元素周期表中的相关信息,图2是该元素形成的一种粒子的结构示意图.
(1)在元素周期表中,氧元素的原子序数为 .
(2)图2所示粒子为 (填“离子”或“原子”).
(3)由氧元素组成的一种气体单质可以支持燃烧,写出实验室制取该气体的一个化学方程式 .
铝、铜、铁是生活中常见的金属。
(1)铝在空气中具有良好的抗腐蚀性的原因是 ;
(2)用铜制品电线主要是利用铜具有良好的 性;
(3)焊接铁制品时,通常先用稀盐酸除去铁表面的锈,反应的化学方程式为 。
现有碳、一氧化碳、碳酸钠、碳酸钙、氧气、氧化铜、稀盐酸七种物质,请按要求选择适当的物质写出生成二氧化碳的化学方程式(每种物质不能重复使用)
(1)化合反应
(2)分解反应
(3)置换反应
(4)复分解反应
早在春秋战国时期,我国就开始生产和使用铁器,请根据所学知识回答下列问题:
(1)工业上常以赤铁矿为原料炼铁,请写出该反应的化学方程式 。
(2)据统计每年因腐蚀而报废的金属设备和材料相当于年产量的20%﹣﹣40%,铁制品锈蚀的过程实际上是铁与空气中的 等发生反应的过程。
CaCO 3在生产生活中有广泛的用途.
(1)煅烧石灰石可制得活性CaO,反应的化学方程式为 .为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等分,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如图1所示.可知:CaO与水反应会 热量(填"放出"或"吸收");上述温度中, ℃煅烧所得CaO活性最高.要得出正确结论,煅烧时还需控制的条件是 .
(2)以电石渣[主要成分为Ca(OH) 2,还含有少量MgO等杂质]为原料制备高纯CaCO 3的流程如下:

①如图为NH 4Cl浓度对钙、镁浸出率的影响(浸出率=  ×100%).可知:较适宜的NH 4Cl溶液的质量分数为 ;浸取时主要反应的化学方程式为 .
×100%).可知:较适宜的NH 4Cl溶液的质量分数为 ;浸取时主要反应的化学方程式为 .
②流程中虚线内部分若改用 溶液(填化学式),可一步得到与原流程完全相同的生成物.
③流程中虚线内部若改用Na 2CO 3溶液,也能得到高纯CaCO 3,试从生物的角度分析原流程的优点:
a.NH 3可循环利用;b. .

如图所示,铁钉最容易生锈的是 处(填“a”、“b”或“c”),常用稀硫酸除去铁锈,写出该反应的化学方程式: .

硫酸的浓度不同,化学性质会有很大差异。将65g锌加入到150g质量分数为98%的浓硫酸中,发现锌逐渐溶解,产生有刺激性气味的气体,该气体是形成酸雨的主要气体。随着反应不断进行,硫酸浓度变小,变成稀硫酸,此时产生的气体没有刺激性气味。最终锌与硫酸恰好完全反应,剩余的溶液只含有一种溶质。
(1)请写出锌与稀硫酸反应的化学方程式 ,
锌与浓硫酸反应的化学方程式 。
(2)生成的气体总质量是 g。
含碳物质种类繁多。请回答下列问题:
(1)葡萄糖(C6H12O6)中C、H、O原子的数目之比是 。
(2)石墨烯和金刚石均为碳单质,但导电性差异很大,原因是 (填字母序号)。
a.原子的排列方式不同 b.原子在不断运动 c.原子的体积很小
(3)乙醇(C2H5OH)是 (填“可再生”或“不可再生”)能源,乙醇完成燃烧的化学方程式是 。该反应中,化学能转变为 能。
金属在生产、生活中有广泛应用。
(1)我国深水钻井平台"981"用钢量达3万吨,露出平台的钢、铁很容易生锈,钢铁生锈的条件是 ,写出一种防止钢铁生锈的方法 。
(2)写出用盐酸除去铁制品表面铁锈的化学方程式 。
(3)硫酸铜、硫酸亚铁的混合溶液中加入一定量镁粉,充分反应后过滤,得到滤渣和滤液。若滤液呈无色,则滤渣中一定含有的金属是 。
化学就在我们身边,化学与生产生活息息相关。请回答下列问题:
(1)人类社会的生活和发展离不开常见金属和金属材料。用我们学到的化学知识和方法能分析和解释许多现象。
①下列生活用品,主要利用金属具有良好导热性的是

②下列事实不能用金属活动性顺序解释的
A.铝制品抗腐蚀能力比铁制品强 B.铜能将银从硝酸银溶液中置换出来
C.不能用金属铜与稀硫酸反应制取氢气 D.铁的硬度比铜大
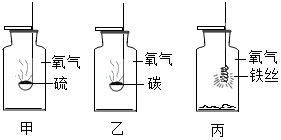
(2)氧气是一种化学性质比较活泼的气体,在点燃和加热的条件下能与许多物质发生化学反应。试回答下列与氧气有关的问题:
①空气中氧气的体积分数约占 。
②如图是一些物质与氧气反应的实验,甲中物质安静燃烧时火焰的颜色是 。任选一个实验,写出一个化学反应的方程式 。
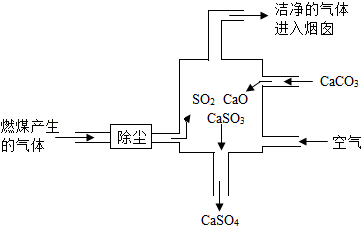
③如图是某燃煤发电厂处理废气的装置示意图,其工艺原理是:向废气处理塔中投入CaCO 3和鼓入空气在高温条件下,将SO 2全部吸收。
(Ⅰ)废气处理塔中发生的反应可用一个总化学方程式表示,写出这个反应的化学方程式: 。
(Ⅱ)若该发电厂每天有16kg二氧化硫产生,则投入的CaCO 3的质量至少是 kg。
2017年3月22日是世界水日,水是人类宝贵的自然资源,根据所学知识回答下列问题:
(1)火箭使用的燃料液氢在助燃剂液氧中燃烧的化学方程式为 .
(2)日常生活中通常向水中滴加 来检验硬水和软水.
(3)高铁酸钠(Na 2FeO 4)被广泛应用于自来水净化消毒,其原理为:
4Na 2FeO 4+10 =4Fe(OH) 3(胶体)+3 +8NaOH(请将化学方程式补充完整).
(4)水是常用的溶剂,某酒精(C 2H 5OH)的水溶液,溶质与溶剂中氢原子个数比为1:2,则该溶液中溶质的质量分数为 (精确到1%).
CO 2的资源化利用日趋成为研究热点。
(1)某小组查阅资料发现:①CO 2与H 2能在催化剂表面反应生成CH 4与H 2O;②CH 4在高温下能与CuO反应。为探究上述反应,设计如下装置。

①仪器M的名称是 。装置B中反应的化学方程式为 。
②设计装置C的目的是 ,若要证明D中有CO 2生成,则需在E、F之间增加盛有 溶液的洗气瓶。
③一段时间后,装置D中黑色固体变红,E中白色固体变蓝,该小组由此得出结论:以上实验证明CH4在高温条件下能与CuO反应。你是否同意他们的结论? (填"同意"或"不同意"),理由是 。
(2)CH 4、乙炔(C 2H 2)和丙烷(CH 3H 8)都能在空气中燃烧,但是仅C 2H 2燃烧时有浓烟。试从物质组成的角度分析其燃烧现象不同的原因是: 。CH 4燃料电池具有洁净、高效的特点,其工作时主要是将 能转化为电能。
用化学式来表示化学反应的式子,叫做化学方程式。请写出下列反应的化学方程式:
(1)铁在氧气中燃烧 。
(2)硫酸铜溶液与氯化钡溶液反应 。
被誉为"中国天眼"的FAST,是目前世界上最大口径、最灵敏的射电望远镜,如图所示。请回答下列问题。
(1)选择角钢而不用纯铁作塔架的主要原因是 。
(2)角钢中含有锰(Mn)和硅,锰可以与稀盐酸发生置换反应,生成锰的化合物中锰元素显+2价。请写出锰与稀盐酸反应的化学方程式 。
(3)请你写出一条防止铁制材料生锈的具体措施 。
(4)向硝酸银和硝酸铜的混合溶液中加入一定量的铝粉,反应停止后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有 ;滤液中一定含有的溶质是 ,可能含有的溶质是 。(均填化学式)
