某同学向盛有Ca(OH)2溶液的烧杯中加入K2CO3溶液到一定量时停止了实验,烧杯中产生了白色沉淀,发生的化学反应方程式为 。为了探究反应后液体的成分,用两支试管各取少量过滤后的滤液,继续做以下实验:
(1)向第一支试管的滤液中加入稀盐酸,有气泡产生,则滤液中的溶质是 (填化学式)。
(2)向第二支试管的滤液中通入足量的CO2气体后,再蒸干滤液,得到白色固体,该物质在农业生产中的用途: (写一点即可)。
化学实验是进行科学探究的重要手段。请填写下列空格:
(1)黄铜是铜锌合金,将外形完全相同的纯铜片和黄铜片相互刻划,该实验的目的是比较它们的 大小。
(2)用坩埚钳夹取一小块木炭,在酒精灯上加热至燃烧,然后将木炭插入盛有氧气的集气瓶内,观察现象。 据此可知,可燃物燃烧的剧烈程度与 有关。
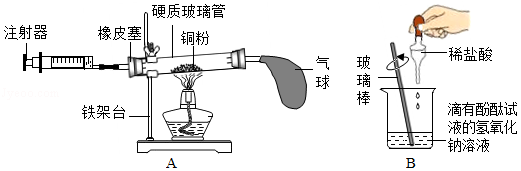
(3)用图 A 所示的装置可测定空气中氧气的含量。 该实验的原理是通过 (选填“化学”或“物理”)方法分离或除去混合物中的一种成分,从而测定混合物中某成分的含量。
(4)用图B 所示的装置探究酸碱中和反应。将稀盐酸滴入氢氧化钠溶液(滴有酚酞试液)中至过量,观察到的现象是 。从微观角度分析,中和反应的实质是 。 请另外写出一个符合上述反应实质的化学方程式 。
在实验室里可采用多种方法制取氧气。
(1)写出用如图装置制氧气的化学方程式 。(写出一个即可)
(2)收集氧气可以采用排水法,这是利用了氧气的什么性质? 。

下列是实验室制取气体常用的部分装置。

(1)同学们为了探究影响实验室制取二氧化碳气体的因素,进行了以下四组实验:
药品/实验编号 |
甲 |
乙 |
丙 |
丁 |
大理石 |
mg,块状 |
mg,块状 |
mg,粉末状 |
mg,粉末状 |
盐酸(过量) |
vmL,稀盐酸 |
vmL,浓盐酸 |
vmL,稀盐酸 |
vmL,浓盐酸 |
①写出上述反应的化学方程式 ,此反应属于的基本反应类型是 ,
原来收集二氧化碳气体的装置是 (填写字母)。
②若探究盐酸的浓度对上述反应的影响,可选择实验甲与 (选填实验编号)进行对照。
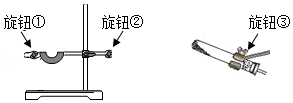
(2)小丽同学选用A装置加热高锰酸钾制取氧气时发现试管固定的太高,应调节图中的旋钮 (选填“①”、“②”、“③”)。
(3)通过比较,归纳实验室制取二氧化碳和氧气的实验,总结实验室制取气体选择装置时的一般思路。
选择气体发生装置的依据 |
|
选择气体收集装置的依据 |
阅读科普短文,回答相关问题。
钠元素在自然界中分布很广,储量极为丰富,常以氯化钠、碳酸钠、硫酸钠等物质存在。
19世纪初,英国化学家戴维在实验室中首次制得了金属钠。
钠是一种银白色金属,质软,密度为0.97g•cm﹣3,熔点为97.8℃。金属钠的性质很活泼,能与许多物质发生化学反应。钠暴露在空气中,与氧气反应生成氧化钠(Na2O),钠在空气中燃烧,生成淡黄色的过氧化钠(Na2O2);钠遇水立即发生剧烈反应,生成氢氧化钠和氢气。因此,实验室常将钠保存在煤油中。
金属钠的用途广泛。钠和钾形成的合金熔点低,常温下呈液态,可用作快中子反应堆的热交换剂。利用钠的强还原性,在一定条件下可以将钛(Ti)、锆(Zr)等稀有金属从其氯化物中置换出来。
工业上通常采用电解熔融氯化钠的方法制取单质钠。
(1)自然界中钠元素以 (填“单质”或“化合物”)形式存在。
(2)钠保存在煤油中,是为了防止钠与空气中的 反应而变质。
(3)过氧化钠中的阴离子为O22﹣,1个O22﹣离子含有的电子数为 。
(4)钠钾合金用作快中子反应堆的热交换剂,利用钠钾合金良好的 (填字母)。
a.导电性
b.导热性
c.延展性
(5)写出高温下钠与四氯化钛反应的化学方程式: 。
2016年11月,“冰箭”冲天,中国挺进大火箭时代。
(1)氢气的利用。火箭采用液氢、液氧作为推进剂,其内部温度极低,因此称为“冰箭”,氢气是 (填序号)。
a.常规能源 b.绿色能源 c.不可再生能源
(2)氢气的制取。利用太阳能分解水制H2与电解水制H2相比,其优点是
(3)氢气的储存。在常温和250kPa下,镧镍合金(LaNi5)吸收氢气生成LaNi5H7,写出该反应的化学方程式 。
(4)氢燃料电池是将化学能直接转化为 ,且能量转化效率高达约80%;与化石燃料相比,氢能源的优点是:①原料来源广,②产物无污染,③ 。

如图为CO还原Fe2O3的微型装置图,则A处V形管内的固体粉末由 色逐渐变黑; B处V形管内的溶液变浑浊,化学方程式为 ;将尾气点燃,化学方程式为 。

(1)如图1为实验室制取并收集气体的装置图,请回答下列问题。
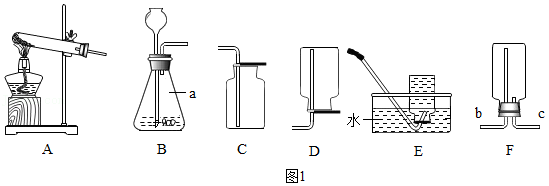
①仪器a的名称是 。
②若用A装置制取氧气,写出对应的化学方程式 。
③若需收集一瓶较纯净的氧气,应选用的装置是 (填装置序号)。
④若用C装置收集一瓶二氧化碳气体,其验满的方法是 。
⑤二氧化硫是一种有刺激性气味的有毒气体,比空气的密度大,易溶于水且与水反应。若用F装置收集二氧化硫气体,则气体应从 (填“b”或“c”)端导入。
(2)电解饱和食盐水可以制得氢氧化钠、氯气(Cl2)和氢气,并进而生产具有消毒、漂白作用的漂白液。
①粗盐中的难溶性杂质可通过溶解、 操作除去,以免破坏电解装置。
②写出电解饱和食盐水的化学方程式 。
③某同学想知道某一瓶放置一段时间的漂白液是否变质,设计了下列探究实验。
【查阅资料】
Ⅰ.制取漂白液(有效成分为NaClO)的原理:Cl2+2NaOH═NaCl+NaClO+H2O;
Ⅱ.在空气中NaClO易发生反应:2NaClO+H2O+CO2═Na2CO3+2HClO,HClO能使有色布条褪色,且HClO含量越高,漂白效果越好;HClO易分解,分解后丧失漂白作用;
Ⅲ.Ca(ClO)2易溶于水。
【提出问题】放置一段时间的漂白液是否变质?
【提出猜想】
猜想1:未变质,溶液中主要成分为NaCl、NaClO
猜想2:部分变质,溶液中主要成分为NaCl、NaClO、Na2CO3
猜想3:全部变质,溶液中主要成分为NaCl、Na2CO3
【实验探究】
实验操作 |
实验现象 |
实验结论 |
ⅰ取适量该溶液于烧杯中,放入有色布条 |
|
猜想3不成立 |
ⅱ另取适量该溶液于试管中,滴入适量氯化钙溶液 |
产生白色沉淀 |
猜想 成立 |
写出实验操作ii中产生白色沉淀的化学方程式 。
【拓展应用】由【查阅资料】和图2可知,需控制pH约为 时(填整数),漂白液具有最佳漂白能力。

金属材料与人类生活息息相关,请回答下列问题。
(1)钛元素在元素周期表中的信息如图所示,则钛的相对原子质量是 。
(2)家用台灯通常采用铜质插头,是利用金属铜的 性。
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是 。
(4)将一定质量的Zn片加入AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是 ;若滤液蓝色,则滤液中溶质一定有 。
我国“十四五”规划已经明确“2030年前实现碳达峰”的目标。碳达峰是指二氧化碳的排放达到峰值,不再增长。如图为自然界中CO2的循环图,图中箭头指向表示产生(排放)或消耗CO2的途径。回答下列问题:
(1)途径①需要消耗空气中的 。
(2)途径②中,枯枝败叶中的纤维素[化学式为(C6H10O5)n]在微生物作用下彻底转化为CO2和H2O,该转化中消耗O2与产生的CO2分子个数比为 。
(3)途径④通过光合作用吸收CO2的量白天 夜晚(填“大于”或“小于”)。

(4)途径⑤消耗的化石燃料是 (填“可”或“不可”)再生资源。
(5)降碳的一种途径是在合适的催化剂条件下,将二氧化碳与氢气反应使碳全部转化为乙烯(C2H4)、同时生成另一种化合物。请写出反应的化学方程式 。
(6)某年通过不同途径产生或消耗碳量的相对值如下表所示:
途径 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
相对值 |
0.6 |
60 |
60 |
121.8 |
5.5 |
92 |
90 |
据表可知,这一年大气中碳量增加了 (用表中相对值计算)。为达成“2030年前实现碳达峰”的目标,下列措施不可行的是 。
A.开发新能源
B.植树造林
C.禁止使用化石燃料
进一步分析上表回答:人口增多是否是大气中碳量增加的主要因素,并说明理由 。
2021年3月,四川“三星堆遗址”已出土黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物,其中青铜为合金。
(1)下列物质中属于金属材料的有 (填序号)。
A.象牙
B.黄金
C.丝织品
D.青铜
(2)青铜的硬度比纯铜 (填“大”或“小”)。
(3)铜制品长期暴露在空气中能与空气中的O2、H2O和 化合生成铜锈【主要成分是Cu(OH)2CO3】。
(4)黄铜是铜锌合金,区分黄铜和纯铜发生反应的化学方程式为 。
含有镁的合金广泛应用于航空航天领域,回答下列问题:
(1)取少量光亮的镁条于试管中,向其中加入稀盐酸,观察到 的现象可推断二者发生了化学反应。
(2)若验证镁与稀盐酸反应后的溶液中有盐酸剩余,下列实验设计可行的是 。
A.取生锈的铁钉于试管中,加入反应后的溶液
B.取少量反应后的溶液于试管中,滴加AgNO3溶液
C.取少量反应后的溶液于试管中,滴加稀氢氧化钠溶液
(3)向镁条中加入过量稀盐酸,完全反应后,再加入过量氢氧化钠溶液,生成5.8g氢氧化镁沉淀。
①写出加入氢氧化钠溶液时,生成氢氧化镁沉淀的化学方程式 ;
②计算镁条与稀盐酸完全反应后生成MgCl2的质量为 g。
新型冠状病毒肺炎疫情防控期间,要合理搭配饮食,以保证基本营养素的均衡摄取,增强身体免疫力;要合理使用消毒剂进行杀菌消毒。请回答下列问题:
(1)下列物质富含蛋白质的是 (填写字母标号)。
| A. |
水果、蔬菜 |
| B. |
花生油、奶油 |
| C. |
纯牛奶、蛋清 |
| D. |
米饭、馒头 |
(2)下列物质常用于制作消毒剂,其中属于氧化物的是 (填写字母标号)。
| A. |
过氧乙酸(CH 3COOOH) |
| B. |
二氧化氯(ClO 2) |
| C. |
苯酚(C 6H 6O) |
| D. |
次氯酸钙[Ca(ClO) 2] |
(3)体积分数为75%的酒精常用于手和皮肤消毒。因易燃,使用时要注意远离火源。乙醇燃烧的化学方程式是 。
(4)"84"消毒液的有效成分是次氯酸钠(NaClO),适用于物体表面以及室内环境等方面的消毒。NaClO中氯元素的化合价是 。
下列化学方程式及对应的基本反应类型都正确的是( )
A.CaHCO3═CaCO3↓+CO2↑+H2O 分解反应
B.Al(OH)3+3HCl═AlCl3+3H2O 复分解反应
C.P+O2 P2O5 化合反应
D.Fe2O3+3CO 3CO2+2Fe 置换反应
化学是一门以实验为基础的学科。请结合下列实验装置图回答问题:

(1)写出图中①、②两种仪器的名称:① ,② 。
(2)某同学用高锰酸钾加热制取氧气,反应的化学方程式为 ;应选择的发生装置为 (填字母) ,收集装置为 (填字母)。
(3)A装置与C装置比较,A装置的优点是可以控制反应的发生和停止。请写出一个利用A装置此优点的反应化学方程式 。
(4)实验室可用金属与浓硫酸反应制取SO2气体,金属锌和金属铜都能与浓硫酸反应制SO2气体。欲制取一瓶纯净的SO2气体,最好选择金属 (填“锌”或“铜”),选择理由是 。