甲、乙两种固体物质的溶解度曲线如图所示.

(1)
时甲物质的溶解度是
;乙物质的溶解度随着温度的升高而(填"增大"或"减小");
(2)
时甲物质的饱和溶液中溶质的质量分数为;将
时甲、乙两种物质的饱和溶液分别降温至
,溶液中溶质质量分数大小关系是:甲(填"<"、"="或">")乙.
如图1是a、b、c三种物质的溶解度曲线,回答下列问题:

(1)P点的含义是。
(2)
时,将50g a物质放入50g水中充分溶解得到溶液的质量为g。
(3)将
时,a、b、c三种物质的饱和溶液降温至
,所得溶液中溶质的质量分数由大到小的顺序是
(4)
时,将盛有c的饱和溶液的小试管放入盛水的烧杯中(如图2),向水中加入一定量的氢氧化钠固体后,试管中的溶液变浑浊,原因是 。
请你参与实验室配制一定溶质质量分数的硝酸钾溶液的实验,并进行实验过程的探究:
(1)计算:配制50g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为 g,所需蒸馏水的体积为 mL(水的密度约为1g/mL)。
(2)称量:分别在天平左右两盘放上纸片,调节平衡后,应 (填标号)。
A.先在托盘上放置所需的砝码,再添加硝酸钾直至天平平衡。
B.先添加所需的硝酸钾,再添加砝码到所在的托盘直至天平平衡。
【探究一】在称量过程中,某同学的称量操作如图所示,你认为该操作对本次实验的数据处理的正确性 (填“有”或“没有”)影响,理由是 .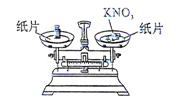
(3)量取:准确量取所需蒸馏水要用到的仪器是 (选填图中的标号)。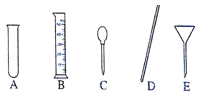
(4)溶解:将称量好的硝酸钾和蒸馏水混合溶解。
【探究二】:20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从表中找出计算所需的数据为: g/mL.
| 温度℃ 质量分数% |
20 |
40 |
60 |
| 4 |
1.023 |
1.016 |
1.007 |
| 10 |
1.063 |
1.054 |
1.044 |
20℃时,将等质量的甲、乙两种固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1所示,加热到50℃时现象如图2所示,甲、乙两种物质的溶解度曲线如图3所示。

请回答下列问题:
(1)图1中一定是饱和溶液的是溶液(填"甲"或"乙");图2中乙溶液一定是溶液(填"饱和"或"不饱和")。
(2)图3中表示乙的溶解度曲线的是(填"M"或"N");图2中乙溶液降温至30℃析出晶体(填"会"或"不会")。
(3)50℃时甲的饱和溶液中溶质质量分数为(计算结果精确到0.1%)。
、
、
三种固体物质在水中的溶解度曲线如图所示,请回答:

(1)℃时,
、
两种物质在100
水中达到饱和状态时溶解的质量相等;
(2)若
中混有少量的
,最好采用的方法提纯
;
(3)现有接近饱和的
物质溶液,使其变成饱和溶液的方法有:①加入
物质;②恒温蒸发溶剂;③;
(4)
℃时将20
物质放入50
水中,充分搅拌,所得溶液中溶质的质量分数是;
(5)将
℃时等质量的
、
、
三种物质的饱和溶液降温至
℃时,所得溶液的质量由大到小的顺序是。
如图所示,
、
、
为三种物质的溶解度曲线,请根据图示信息回答下列问题。

(1)
℃时,
、
、
三种物质中溶解度最小的是。
(2)
℃时,将20
物质投入100
水中,充分溶解,温度不变,所得溶液为溶液(填"饱和"或"不饱和")。
(3)下列说法正确的是。
| A. |
℃时,将 和 的混合溶液(两者均已达到饱和),降温到 ℃,析出的晶体含有 和 |
B. | 从混有少量 的 物质中提取较纯净的 ,可通过冷却它们的热饱和溶液实现 |
| C. |
℃时,将 、 、 的饱和溶液分别降温到 ℃,所得溶液中溶质质量分数的大小关系是 > > |
D. | ℃时,欲用 的饱和溶液配制10%的 溶液,只需要烧杯、量筒、胶头滴管三种玻璃仪器 |
(4)如图所示,向放有镁条的试管中滴加稀盐酸后,锥形瓶中
的饱和溶液变浑浊。请解释原因。

下图为甲、乙两种物质的溶解度曲线,请回答下列问题:
(1)20℃时,为使接近饱和的甲物质溶液变为饱和溶液的方法是: (任写一种方法即可);
(2)40℃时,乙物质的溶解度是____g。此温度下,该饱和溶液中乙物质的质量分数是 (精确到0.1%)。
下列图像不能正确反映其对应关系的是()
| A. |
|
| B. |
|
| C. |
|
| D. |
|
下图是甲、乙两种固体物质的溶解度曲线。下列说法错误的是

| A. | 时,甲、乙两物质的溶解度相等 |
| B. | 乙的饱和溶液降温时,溶质质量分数保持不变 |
| C. | 甲中混有少量乙,可采用降温结晶的方法提纯甲 |
| D. | 时,甲的饱和溶液溶质质量分数为20% |
硝酸钾溶解度随温度变化的曲线如图所示:

(1)图中
三点中属于不饱和溶液的是。
(2)由
点到
点可采取的措施。
(3)若
溶液中混有少量的
杂质,可以采取方法获得较纯净的
.
(4)若将
点溶液逐渐加水稀释使其质量分数降至10%,在此稀释过程中符合此溶液中溶质质量变化的规律的图像是。

为了测定某含杂质7%的黄铜样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:

(1)配制上述质量分数为14.6%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是;
(2)发生反应的化学方程式为;
(3)根据已知条件列出求解100g该黄铜样品中锌的质量(x)的比例式为;
(4)该黄铜样品中铜的质量分数是;
(5)向过滤后所得滤液中加入87.4g水,则最终所得溶液中溶质的质量分数是;
(6)欲将黄铜样品中的铜转化为铜盐,可将过滤后所得的不溶性物质洗涤、烘干,然后在空气中加热,充分反应,则可得到含杂质的氧化铜的质量是,再经过某些反应及操作就得到了所需铜盐。
在实验室小金分别用甲盐的晶体配置了溶质质量分数为5%的A溶液和30%的B溶液,但忘了贴标签,请你运用两种不同的科学原理,分别设计两个简单实验来判别这两瓶溶液。请写出简要的实验方案和明确的判别依据。有下列仪器、物品供选择:量筒、天平、
小烧杯、酒精灯、三脚架、石棉网、漏斗、玻璃棒、滤纸、温度计、新鲜罗卜、甲盐的晶体。
(实验室的室温为30℃,30℃甲盐的溶解度为50g)
方案1:
判别依据:
方案2:
判别依据:
、
两种固体物质的溶解度曲线如图所示,请根据曲线图回答下列问题。
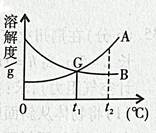
(1)现有常温下
的不饱和溶液,在只要求保持其中溶剂质量不变的条件下,将其变成饱和溶液,可行的方法有。
(2)现有一杯
时含
、
两种物质且均饱和的混合溶液,若要从中分离出少量A的纯净物,其操作方法是。
(3)下列说法正确的是。
①
时,
的溶液中溶质的质量分数一定比B的溶液中溶质的质量分数大;
② 将
,
、
的饱和溶液分别降温至
,此时两溶液中的质量分数相等;
③ 在
时,用两份等量的水分别配制成
、
的饱和溶液,这两种溶液的质量相等;
④ 在
时,用等量的
、
分别配制成两种饱和溶液,测得其质量依次为
和
,则
。
下列曲线能正确表达对应的反应或过程的是()

| A. | 向一定量的水中加入生石灰 | B. | 红磷在装有空气的密闭容器中燃烧 |
| C. | 向一定量的烧碱溶液中加入盐酸 | D. | 向饱和 溶液中加入 固体 |
、
、
在不同溶剂中的溶解度如下表所示。
表1
、
、
分别在水中的溶解度(
)
|
/℃ |
|||
| 0 |
42 |
7.1 |
35.7 |
| 10 |
51 |
12.2 |
35.8 |
| 20 |
109 |
21.8 |
36.0 |
| 30 |
119 |
39.7 |
36.3 |
表2 常温下,
、
、
分别在乙醇中的溶解度(
)
| 17.3 |
<0.01 |
0.1 |
根据表1和表2提供的数据回答下列问题:
(1)
在水中的溶解度随温度升高而(填"增大"或"减小")
(2)20℃时,饱和食盐水中溶质的质量分数为(计算结果精确到0.1﹪);
(3)为证明
能与
发生反应,小明同学将
通入饱和
的乙醇溶液中。请推测该实验可观察到的现象,推测依据是。