2015年初中毕业升学考试(黑龙江大庆卷)化学
下列说法正确的是()
| A. | 空气中氧气的体积分数最大 |
| B. | 用灯帽盖灭酒精灯是因为降低了可燃物温度 |
| C. | 海水资源丰富,所以淡水资源可以取之不尽,用之不竭 |
| D. | 使用新型可降解塑料可减少"白色污染" |
下列各选项中不属于化学反应的是
| A.用活性炭除去冰箱中的异味 | B.用胃舒平治疗胃酸过多 |
| C.在蔗糖中加入浓硫酸后变黑 | D.煤的干馏和石油的分馏 |
下列不能作为判断金属 三种金属活动性强弱的是()
| A. | 在纯氧中燃烧的现象 | B. | 与盐酸反应的快慢程度 |
| C. | 金属导电性强弱 | D. | 三种金属发现和利用的年代的先后顺序 |
下列说法正确的是
| A. | 水有三态变化,是由于水分子从静止状态变为运动状态 |
| B. | 煤或石油只要完全燃烧就不会造成空气污染 |
| C. | 氢氧燃料电池是把氢气和氧气反应的化学能直接转化为电能,供人们使用 |
| D. | 自来水净化中加入明矾的目的是杀菌消毒 |
下列关于反应的描述,反应方程式及反应类型完全正确的是
类比推理是化学学习中的一种重要思维方法,以下类推结果正确的是
下列说法正确的是
| A. | 酒精是最常用是消毒药,体积分数为95%的酒精杀菌能力最强 |
| B. | 亚硝酸钠( )外观极像食盐,且具有与食盐一样的咸味,但被误作食盐食用,会导致中毒事故发生 |
| C. | 为了防止大脖子病,食用的是加入碘化钾的食盐 |
| D. | 市售食醋中含乙酸约为30%-50% |
下列关于混合物、酸、碱、盐、氧化物分类完全正确的是( )
| 混合物 |
酸 |
碱 |
盐 |
氧化物 |
|
| A |
冰水混合物 |
硫酸 |
氢氧化钠 |
硫酸钡 |
干冰 |
| B |
焦炉煤气 |
硝酸 |
氢氧化钙 |
碳酸氢钙 |
四氧化三铁 |
| C |
合金 |
盐酸 |
碱式碳酸铜 |
氯化银 |
一氧化碳 |
| D |
空气 |
醋酸 |
氢氧化钡 |
碳酸钙 |
氯酸钾 |
(1)重铬酸钾
中Cr元素的化合价为。
(2)分子、原子、离子都是构成物质的粒子,下列物质由分子直接构成的是,由原子直接构成的是,离子直接构成的是。
①氧气 ②镁 ③氯化钠 ④二氧化碳
(3)硬水是指含较多的水,鉴别硬水和软水的最简便方法是加入。
已知
五种元素核电荷数依次增大,
原子核内无中子,
的一种单质是自然界中最硬的物质,
是地壳中含量最多的元素,
的最外层电子数与
的最外层电子数相同,且
形成的化合物之一是形成酸雨的罪魁祸首,
是地壳中含量居于第二位的金属元素,且其合金用量最多用途最广,请回答下列问题:
(1)写出
形成两种液态化合物的分子式
(2)画出
的原子结构示意图
(3)防止
锈蚀的方法
(4)
两种元素按质量比3:16形成化合物的分子式
(1)下列氮肥含氮量由高到低的排列顺序是:
| 常见氮肥 |
①
|
②
|
③
|
| 相对分子质量 |
80 |
79 |
60 |
(2)治理汽车尾气中的
和
的一种方法是:在汽车的排气管上装一个催化转化装置。使
和
反应生成
和
,写出该反应的化学方程式
(3)有机物中碳氢化合物可用
表示,其完全燃烧的化学方程式:
判断等质量的①
,②
,③
,三种碳氢化合物完全燃烧消耗氧气由大到小的顺序是
现有一包白色固体样品,可能含有
、
、
、
、
、
中的一种或几种,取样品进行如下实验:

(1)操作1所用到是玻璃仪器有
(2)原白色固体中一定不含有
(3)写出生成气体a的化学方程式
硝酸钾溶解度随温度变化的曲线如图所示:

(1)图中
三点中属于不饱和溶液的是
(2)由
点到
点可采取的措施
(3)若
溶液中混有少量的
杂质,可以采取
(4)若将
点溶液逐渐加水稀释使其质量分数降至10%,在此稀释过程中符合此溶液中溶质质量变化的规律的图像是

已知
通入澄清石灰水中,溶液变浑浊,继续通
气体由浑浊又变澄清,
,由此某化学兴趣小组欲探究
与
溶液反应后的溶质组成。
【提出问题】
与
溶液反应后的溶质组成
【查阅资料】1、
2、盐酸滴入碳酸钠溶液中,实际反应分两步进行
第一步反应:
第二步反应:
【提出猜想】猜想1:溶质为
猜想2:溶质为
猜想3:溶质为
猜想4:溶质为
【实验方案】I甲组同学为确定
与
溶液反应后所得溶液中溶质组成,设计如下实验方案。
(1)向所得溶液中加入足量的
溶液,若有白色沉淀生成,过滤后向溶液中加入足量的稀盐酸无气泡产生,则溶质为
(2)向所得溶液中加入足量的
溶液,若无白色沉淀生成,溶液中加入足量的稀盐酸有气泡产生,则溶质为
(3)向所得溶液中加入足量的
溶液,若有白色沉淀生成,过滤后向溶液中加入足量的稀盐酸有气泡产生,则溶质为
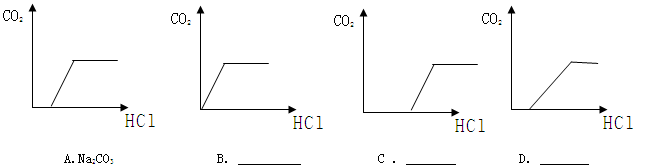
II乙组同学根据甲组同学的猜想,通过定量分析绘制出向所得溶液中逐滴加入稀盐酸的质量与生成二氧化碳的质量关系示意图,请根据图像确定溶质成分。
在各种金属材料中铜是人类应用比较广泛的金属之一,某学习小组欲测定铜的相对原子质量,设计如下实验方案:
实验步骤:①连接好装置,②-----③装入药品 ④打开分液漏斗活塞向锥形瓶中滴加入稀盐酸 ⑤一段时间后点燃酒精灯⑥D中黑色固体完全变成红色,停止加热,待D中玻璃管冷却至室温,关闭分液漏斗活塞 ⑦数据处理

请回答下列问题:
(1)补全实验步骤②。
(2)若使制取氢气是装置随开随用,随关随停,下列装置可选用的是。

(3)B装置中水的作用,长玻璃管的作用,C装置的作用.
(4)已知: 样品质量为m1克,E中增重为m2克,D中反应后固体质量为m3克,实际参加反应氢气的质量为m4克,试用m1,m2列出铜的相对原子质量的表达式。若无F装置,则对测定结果的影响(填"偏大"、"偏小"、"无影响"),以下数据还能测定铜的相对原子质量的是。
| A. | m 2 m 3 | B. | m 3 m 4 | C. | m 1 m 4 | D. | m 2 m 4 |
(5)请你评价实验有什么不妥之处,并说明原因。




 粤公网安备 44130202000953号
粤公网安备 44130202000953号