如图是
,
,
三种固体物质的溶解度曲线,请回答下列问题:

(1)
点的含义是;
(2)若
点混有少量
时,可采用的方法提纯
;
(3)
℃时,能不能配制溶质的质量分数为40%的
溶液?(填"能"或"不能");
(4)
℃时,将
,
,
三种固体物质各30
加入到100
水中,充分溶解,形成不饱和溶液的是;
(5)将
℃时
,
,
三种固体物质的饱和溶液升温到
℃,其溶质的质量分数由大到小的顺序是。
某化学小组初步探究"氢氧化钠溶液与盐酸发生中和反应时溶液温度的变化情况".
实验用品:37%的浓盐酸(密度为
)、10%的氢氧化钠溶液、蒸馏水、量筒、温度计
实验一:配制100
10%的盐酸(密度为
)
实验步骤
(1)计算:需要37%的浓盐酸的体积为
(精确到0.01
,下同);需要蒸馏水的体积为
(水的密度为
)
(2)量取浓盐酸和蒸馏水。
(3)混合配制。
实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:

(1)表中
的值为.
(2)试绘出溶液温度变化与加入盐酸体积之间的关系图.
(3)根据所绘曲线分析,加入盐酸的体积在0~10
时,溶液温度变化的趋势及其原因是。
(4)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素)。
横坐标及猜想理由:;
纵坐标及猜想理由:。

下图是两种物质的溶解度曲线,下列说法正确的是( )

| A. | 甲的溶解度大于乙的溶解度 |
| B. | ℃时等质量甲、乙两种物质的饱和溶液中溶质质量相等 |
| C. | ℃时等质量的甲、乙两物质的饱和溶液降温至 ℃时,两溶液中溶质质量分数相等 |
| D. | 氧气的溶解度随温度变化的规律与图中乙相似 |
如图是
、
、
三种固体物质的溶解度曲线图,请回答:

(1)
、
、
三种物质的溶解度受温度影响最大的是;
(2)t1℃时
的溶解度(填">"、"<"或"=")
的溶解度;
(3)在t2℃时,将15g
物质加入到50g水中,充分搅拌后,所得溶液中溶质的质量分数为。
如图是甲、乙、丙三种物质的溶解度曲线。下列说法错误的是

| A. | 时,三种物质的溶解度是丙>乙>甲 |
| B. | 时,甲和丙的饱和溶液溶质质量分数相等 |
| C. | 三种物质的溶解度均随温度的升高而增大 |
| D. | 当甲中混有少量的乙时可用冷却其热饱和溶液的方法提纯 |
如图是氯化钠和硫酸钠的溶解度曲线,看图后回答问题:

(1)的溶解度收温度影响变化不大。
(2)温度不变时,若将氯化钠的不饱和溶液变为饱和溶液可采取的方法是。(填一种即可)
(3)40℃时,将30
硫酸钠固体加入到50
水中充分溶解,所得溶液的质量是。
(4)用降温结晶的方法提纯含少量杂质氯化钠的硫酸钠,最佳的温度范围是℃以下,理由是。
甲、乙两种固体物质的溶解度曲线如图所示.

(1)
时甲物质的溶解度是
;乙物质的溶解度随着温度的升高而(填"增大"或"减小");
(2)
时甲物质的饱和溶液中溶质的质量分数为;将
时甲、乙两种物质的饱和溶液分别降温至
,溶液中溶质质量分数大小关系是:甲(填"<"、"="或">")乙.
如图1是a、b、c三种物质的溶解度曲线,回答下列问题:

(1)P点的含义是。
(2)
时,将50g a物质放入50g水中充分溶解得到溶液的质量为g。
(3)将
时,a、b、c三种物质的饱和溶液降温至
,所得溶液中溶质的质量分数由大到小的顺序是
(4)
时,将盛有c的饱和溶液的小试管放入盛水的烧杯中(如图2),向水中加入一定量的氢氧化钠固体后,试管中的溶液变浑浊,原因是 。
海水淡化可采用膜分离技术.如图一所示,对淡化膜右侧的海水加压,在其左侧得到淡水.其原理是海水中的水分子可以透过淡化膜,而其他各种离子不能透过。
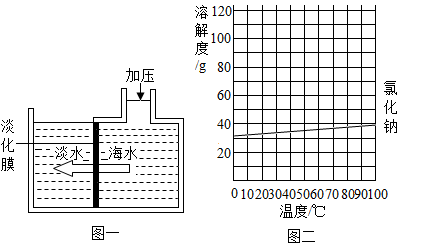
请回答:
(1)采用膜分离技术淡化海水的原理,与化学实验中常见的操作相似。
(2)对淡化膜右侧的海水加压后,海水中溶质的质量分数会(填"增大"、"减小"或"不变")。
(3)海水中含有大量的氯化钠,图二是氯化钠的溶解度曲线,据此可知盐场从海水中得到食盐晶体利用的方法是结晶(填"降温"或"蒸发")。
20℃时,将等质量的甲、乙两种固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1所示,加热到50℃时现象如图2所示,甲、乙两种物质的溶解度曲线如图3所示。

请回答下列问题:
(1)图1中一定是饱和溶液的是溶液(填"甲"或"乙");图2中乙溶液一定是溶液(填"饱和"或"不饱和")。
(2)图3中表示乙的溶解度曲线的是(填"M"或"N");图2中乙溶液降温至30℃析出晶体(填"会"或"不会")。
(3)50℃时甲的饱和溶液中溶质质量分数为(计算结果精确到0.1%)。
、
、
三种固体物质在水中的溶解度曲线如图所示,请回答:

(1)℃时,
、
两种物质在100
水中达到饱和状态时溶解的质量相等;
(2)若
中混有少量的
,最好采用的方法提纯
;
(3)现有接近饱和的
物质溶液,使其变成饱和溶液的方法有:①加入
物质;②恒温蒸发溶剂;③;
(4)
℃时将20
物质放入50
水中,充分搅拌,所得溶液中溶质的质量分数是;
(5)将
℃时等质量的
、
、
三种物质的饱和溶液降温至
℃时,所得溶液的质量由大到小的顺序是。
如图是甲、乙两固体物质的溶解度曲线,下列说法错误的是

| A. | 10 时,甲的溶解度小于乙的溶解度 |
| B. | 时,甲乙两物质的溶解度相等 |
| C. | 使甲物质从其饱和溶液中析出,可采取降温的方法 |
| D. | 甲、乙的饱和溶液从30 降温到10 时,析出的晶体质量甲一定大于乙 |
如图所示,
、
、
为三种物质的溶解度曲线,请根据图示信息回答下列问题。

(1)
℃时,
、
、
三种物质中溶解度最小的是。
(2)
℃时,将20
物质投入100
水中,充分溶解,温度不变,所得溶液为溶液(填"饱和"或"不饱和")。
(3)下列说法正确的是。
| A. |
℃时,将 和 的混合溶液(两者均已达到饱和),降温到 ℃,析出的晶体含有 和 |
B. | 从混有少量 的 物质中提取较纯净的 ,可通过冷却它们的热饱和溶液实现 |
| C. |
℃时,将 、 、 的饱和溶液分别降温到 ℃,所得溶液中溶质质量分数的大小关系是 > > |
D. | ℃时,欲用 的饱和溶液配制10%的 溶液,只需要烧杯、量筒、胶头滴管三种玻璃仪器 |
(4)如图所示,向放有镁条的试管中滴加稀盐酸后,锥形瓶中
的饱和溶液变浑浊。请解释原因。

甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述错误的是()
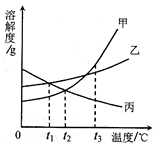
| A. | 时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量:甲>乙 |
| B. | 将 时甲、丙的饱和溶液升温到 ,两种溶液中溶质的质量分数相等 |
| C. | 将 时甲的饱和溶液变为 时甲的饱和溶液,可以采用蒸发水的方法 |
| D. | 将 时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:甲>乙>丙 |
溶解度是解决溶液相关问题的重要依据.
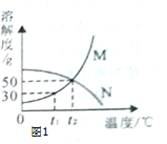
Ⅰ.根据图1解决下列问题:(
,
均不含结晶水)
(1)温度为
时,
,
两种物质的溶解度相等;
(2)
时,将20g
加入50g水中,充分溶解,形成溶液的质量为g.保持温度不变,向该溶液中再加入10g水充分搅拌,溶液的溶质质量分数将(填"变大"、"变小"或"不变");
(3)
时,将25g
加入50g水中,完全溶解后要提高该溶液的溶解质量分数,其操作方法是.
Ⅱ.根据表格解决实际问题:
| 温度/ | 20 |
30 |
50 |
80 |
90 |
|
| 溶解度/g |
|
31.6 |
45.8 |
85.5 |
100 |
169 |
|
|
110 |
114 |
121 |
126 |
139 |
某
样品中含有少量
,其提纯过程如图2: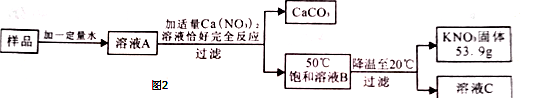
(1)图2中溶液
是(填"饱和"或"不饱和")溶液;
(2)样品中钾元素的质量为g(结果保留整数).