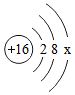某同学要在一块空地上种植作物,于是对这块空地的土壤酸碱度进行测定。
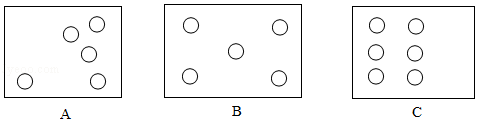
(1)在空地上确定5~6个位置进行取样测定土壤酸碱度。以下三种取样位置设定合理的是 。
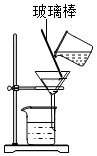
(2)将采集到的土样进行处理后,用玻璃棒蘸取土壤浸出液,滴在 上,将其呈现的颜色与标准比色卡比色,确定了空地土壤的pH约为7.查阅资料,常见作物最适宜生长的土壤pH范围如下表,则这块空地上适合种植的作物有 。
作物 |
大蒜 |
丝瓜 |
茄子 |
沙枣 |
最适pH范围 |
5.6~6.0 |
6.0~6.5 |
6.8~7.3 |
8.0~8.7 |
波尔多液含氢氧化钙、氢氧化铜和硫酸钙等物质,是农业上常用的杀菌剂。一种生产波尔多液的工艺流程如图。
(1)“煅烧”的化学方程式为CaCO3 CaO+CO2↑,该反应属于基本反应类型中的 反应。
(2)“混合”时不能用铁制容器,原因是 。
(3)“混合”时需不断搅拌,目的是 。
(4)“混合”过程中硫酸铜和氢氧化钙反应生成氢氧化铜的化学方程式为 。
(5)“混合”后得到的波尔多液温度明显高于室温,原因是 。
(6)用 可以测定波尔多液酸碱度。

“关爱生命,拥抱健康”是人类永恒的话题。
(1)烹饪过程中使用了加碘盐,其目的是为了防止缺碘引起 (选填“甲状腺”、“贫血”或“佝偻”)疾病;
(2)患胃酸过多症的病人可服用含 (选填“氢氧化铝”或“氢氧化钠”)的药物治疗;
(3)健康人的体液必须维持在一定的酸碱度范围内,用 可以测定人体内或排出的液体的酸碱度,帮助我们了解身体健康状况。
规范操作是实验成功的前提。请按要求回答下列问题:
(1)“粗盐中难溶性杂质的去除”实验中,玻璃棒的作用有:转移、 。
(2)“一定溶质质量分数溶液的配制”实验的基本步骤包括:计算、 、装瓶保存。
(3)利用pH试纸检验溶液的酸碱性,正确的操作应是 。
怀化靖州杨梅已有上千年的栽培历史,靖州杨梅以色泽呈乌,酸甜适中,果大核小,营养丰富而著称.
(1)写出杨梅中含有的一种基本营养物质 .
(2)杨梅树的施肥很讲究,已挂果的杨梅树只需施加有机物和硫酸钾,请写出硫酸钾的化学式 ,硫酸钾属于哪一类肥? .
(3)杨梅树皮可以提取杨梅苷,杨梅苷具有较高的药用价值,它的化学式为C21H20O12,它是由 种元素组成的,它的一个分子中含有 个氢原子,你认为杨梅苷是有机物还是无机物? .
(4)用pH计(测pH的一种仪器)测新鲜的杨梅汁,哪一项符合实际 (填序号).
A.10.0﹣12.0 B.7﹣7.7 C.2.5﹣6.5.
水是人类宝贵的自然资源,与人类的生产、生活密切相关.
(1)通过电解水实验,可以知道水是由 组成.
(2)饮用酸碱度过大或硬度过大的水都不利于人体健康.在实验室里可用 测定水的酸碱度;可通过 方法来降低水的硬度.
(3)净化水的常用方法有:①消毒杀菌 ②过滤 ③蒸馏 ④活性炭吸附 ⑤加明矾吸附沉降.天然水中往往含有许多杂质,要把天然水净化成生活中的自来水,所选用的净化方法按净化过程排序是 (填序号).
五一期间,小红和父母到张家界森林公园游览,感受自然的美.请你用学过的化学知识,帮助他们解决在游览中遇到的问题.
(1)五月的张家界山花烂漫,进入景区就感受到香气扑鼻,沁人心脾.用分子的观点解释闻到的原因 .
(2)景区内环保客运车的燃料是经过脱硫等处理的液化天然气.天然气最主要的成分是 ;液化天然气比汽油或柴油作汽车燃料的优点有 (写一条).
(3)他们在景区里的餐食谱如下:主食:米饭,配菜:土家腊肉、鸡汤、五香豆干.为了保证各种营养素的均衡摄入,你建议他们再添一道菜是 (选填字母,下同)
A.炒鸡蛋B.牛奶C.炒小白菜D.牛肉干
(4)在公园里游玩时,不小心被蚊虫叮咬(蚊虫能分米蚁酸),涂抹下列物质中的 ,可以减轻被蚊虫叮咬带来的疼痛.
A.肥皂水(pH>7)B.食盐水(pH=7)C.食醋(pH<7)
(5)公园内“严禁吸烟”,主要是为了防止丢下的燃着的烟头引燃干叶枯枝,造成森林火灾.这里,燃着的烟头作用是 .
(6)小红用空瓶盛装了一瓶金鞭溪的水带回实验室进行进行试验.用肥皂水检验溪水的实验现象如图所示.则金鞭溪的水属于 (选填“硬水”或“软水”):检验溪水的酸碱强弱程度,应选择用 进行检测.

某植物的花瓣汁液(以下简称:X汁液)呈紫色,X汁液分别滴加到盛有下列溶液的试管中有如下现象:
| 溶液名称 |
白醋 |
稀盐酸 |
氯化钠溶液 |
蒸馏水 |
石灰水 |
氢氧化钾溶液 |
| X汁液 |
红色 |
红色 |
紫色 |
紫色 |
绿色 |
绿色 |
(1)据上表推测,X汁液 (填"能"或"不能")做酸碱指示剂.
(2)将X汁液滴入肥皂水中溶液呈绿色,则肥皂水显 (填"酸"、"碱"或"中")性,pH (填">"、"<"或"=")7;
(3)粗略测定雨水的酸碱度可使用 .
水是人类最重要的资源,人类的日常生活离不开水。
(1)在生活中,当水的硬度过大或者病菌过多时,通常采取 的方法降低水的硬度和杀灭病菌。
(2)当空气受到硫氧化物污染时容易形成酸雨。若要测定雨水的酸碱度,可使用 。
(3)饭后洗碗时,用洗涤剂清洗油污是利用洗涤剂的 作用。
(4)写出一条生活中节约用水的方法 。
根据如图所示的实验回答问题

(1)甲实验中仪器a的名称是 ,进行粗盐提纯实验时过滤的目的是
(2)乙实验验证人体呼出气体中二氧化碳含量比空气中多时,除了要检验两种气体样品的体积相同外,还要控制 相同,实验现象是
(3)丙实验用pH试纸测定白醋的酸碱度时,先用蒸馏水润湿试纸则测得结果与实际值相比 (选择“偏大”、“偏小”或“相等”)
化学与生活密切相关,化学就在我们身边.
(1)下列食物中富含糖类的是 (填序号).
(2)某兴趣小组对清水江的水质状况进行调查研究.取回水样,在实验室静置后过滤,过滤需要用到的玻璃仪器有烧杯、漏斗和 .
(3)若要测定清水江江水的酸碱度,最适宜的是 (填序号)
A.紫色石蕊溶液 B.pH试纸 C.无色酚酞溶液
(4)当森林或草场发生火灾时,救火的措施之一是铲除火场周围一定宽度的树木和杂草,形成一道“防火墙”,其原理是 .
(5)烧碱露置在空气中不但会吸收空气中的水蒸气而潮解,还会发生变质,请你用化学方程式解释烧碱变质的原因 .
水是人类的宝贵自然资源,与人类的生产、生活密切相关。
(1)饮用酸、碱性过强或硬度过大的水都不利于人体健康,可用 来测定水的酸碱度。
(2)检验水是硬水还是软水,可用的物质是 ,日常生活中使硬水软化的方法是 。
(3)实验室用“电解水”或“氢气在氧气中燃烧”的实验探究水的组成元素,理论依据是 。
填写实验报告.
实验内容 |
实验现象 |
分析、结论及解释 |
(1)测定碱溶液的pH 取两片pH试纸,放在白瓷板上,分别用玻璃棒蘸取稀氢氧化钠溶液,将试纸显示的颜色与 比较,读出pH. |
/ |
若实验过程中,用沾有水的玻璃棒蘸取溶液,则所测得的pH (填“>”、“=”或“<”)实际值 |
(2)碱和指示剂作用取两只洁净的试管,分别加入约2mL的稀氢氧化钠溶液,澄清石灰水,再分别加入3滴无色酚酞溶液,观察溶液颜色变化. |
两只试管汇中的酚酞溶液均变为 色 |
稀氢氧化钠溶液、澄清石灰水都呈 性. |
(3)碱和非金属氧化物的反应用排水法收集一瓶呼出的气体,然后加入约2mL澄清石灰水,振荡,观察现象 |
澄清石灰水变浑浊 |
反应的化学方程式
|
以粗盐(含杂质Na2SO4、MgCl2、CaCl2、泥沙)为原料制备精盐。
(1)加水溶解后,用如图装置除去粗盐中的泥沙,玻璃棒的作用是 。
(2)为除去Na2SO4、MgCl2、CaCl2,并得到中性的食盐溶液,下列所加试剂和操作:①加过量的Na2CO3溶液,②过滤,③加过量的NaOH溶液,④加适量的稀HCl,⑤加过量的BaCl2溶液,能达到目的顺序是 。
A.⑤③②①④B.③⑤①④②C.③⑤①②④
(3)用pH试纸检验溶液是否呈中性的操作是 。
经过一年的化学学习,你掌握了很多的化学知识和方法,请回答下列问题:
(1)湿衣服晾干,从微观角度分析是因为水分子 的结果。
(2)病人在手术后,为了促进伤口的愈合,从营养角度分析,应增加 的摄入量。
(3)我国生态环境部的最新数据显示:2018 年首批实施新《环境空气质量标准》的74个城市,
PM2.5平均浓度下降42%,SO2平均浓度下降 68%.空气中SO2的含量显著降低可减少 造成的危害。如图是硫原子的结构示意图,其中 x= 。
(4)蓝莓中的花青素可以促进视网膜细胞中的视紫质再生,预防近视,增进视力。种植蓝莓要求土壤的pH值为4.0~5.5,最适pH值为4.0~4.8.为了解家乡的土壤是否适合种植蓝莓。小张同学提取了本村土壤样品的浸出液。他的下一步操作是用 测出土壤浸出液的pH值。