实验室配制氯化钠溶液的操作中,错误的是( )
| A. |
|
B. |
|
| C. |
|
D. |
|
在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数偏大的可能原因有( )
| A. |
用量筒量取水时俯视读数 |
| B. |
用来配制溶液的烧杯刚用少量蒸馏水润洗过 |
| C. |
用托盘天平称取蔗糖时,将蔗糖放在右盘,且称量时使用了游码 |
| D. |
用了含少量杂质的蔗糖配制溶液 |
以下实验室配制一定溶质质量分数的氯化钠溶液的流程示意图.
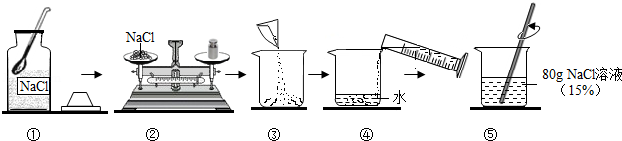
请根据示意图回答.
(1)托盘天平左盘中固体氯化钠的质量为 g,量筒中水的体积为 mL;
(2)上述溶液取10g加水40g进行稀释,所得氯化钠溶液的溶质质量分数是 .
黄铜(铜和锌的合金)因性能优良,被广泛用于制作钱币、饰品和生产中,铜的质量分数在59%﹣65%之间的黄铜性能优良。兴趣小组为了解某黄铜螺母的材料性能进行如下实验:取多个黄铜螺母放入烧杯中,另取80克19.6%的稀硫酸,分四次等质量加入,每次均充分反应,实验过程数据记录如表。
实验次数 |
1 |
2 |
3 |
4 |
稀硫酸的用量/克 |
20 |
20 |
20 |
20 |
剩余固体的质量/克 |
20.0 |
17.4 |
14.8 |
13.5 |
分析上述数据,请回答下列问题:
(1)第4次实验结束后溶液的pH 7(选填“>”“=”或“<”)。
(2)配制80克溶质质量分数为19.6%的稀硫酸,需98%的浓硫酸(密度为1.84克/厘米3)多少毫升?(精确到小数点后一位)
(3)通过计算说明该黄铜螺母的材料性能是否优良。
化学与生产、生活息息相关。
(1)水稻生长初期需要施氮肥,下列属于氮肥的是 。
A.K 2CO 3 B.(NH 4) 2SO 4 C.Ca 3(PO 4) 2 D.CO(NH 2) 2
(2)农业上常用溶质质量分数为16%的氯化钠溶液选种,现要配制100Kg这种溶液,需要 Kg氯化钠,配制该溶液的主要步骤有:①计算 ②称量 ③量取 ④ 。
(3)自行车是"绿色出行"的交通工具,为防止其链条生锈常采用的方法是 ;自行车支架使用的铝合金是 材料(填"金属"或"合成"),铝离子结构示意图如图 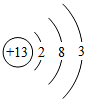 ,铝在化学反应中易 (填"得"或"失")电子,她的离子符号为 。
,铝在化学反应中易 (填"得"或"失")电子,她的离子符号为 。
某同学配制50g 6%的氯化钠溶液,整个操作过程中如图所示,回答下列问题:
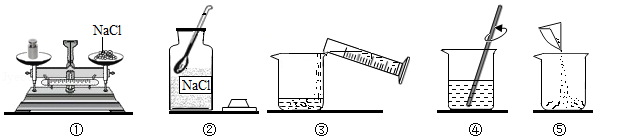
(1)配制溶液的正确操作顺序为 (填序号,下同),其中操作错误的是 。
(2)图②中盛放氯化钠固体的仪器名称是 ,需称取氯化钠 g。
(3)量水时选用的量筒的量程最合适的是 (填序号),读数时视线要与量筒内 保持水平。
A.10mLB.25mLC.50mLD.100mL
(4)取上述溶液10g加水 g,可稀释得到3%的NaCl溶液。
(5)若该同学配制的溶液溶质质量分数偏小,可能的原因是 (填序号)。
A.氯化钠固体不纯B.用生锈砝码称量
C.装瓶时有少量溶液洒出D.溶解前烧杯内有少量水
用所给实验器材(规格和数量不限),就能顺利完成相应实验的是( )
| 选项 |
相应实验 |
实验器材(省略夹持装置) |
| A |
硫酸铜晶体的制备和生长 |
烧杯、玻璃棒、蒸发皿、量筒 |
| B |
分离氯化钾和二氧化锰的混合物 |
烧杯、玻璃棒、胶头滴管、滤纸 |
| C |
用固体氯化钠配制5%的溶液 |
烧杯、玻璃棒、胶头滴管、量筒 |
| D |
用pH试纸测定溶液的酸碱性强弱 |
烧杯、玻璃棒、pH试纸、标准比色卡 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
正确的操作是实验成功的保证。
(1)如图甲所示,实验室稀释浓硫酸时,①处的试剂是 (填字母序号),用玻璃棒不断搅拌的作用是 (填字母序号)。
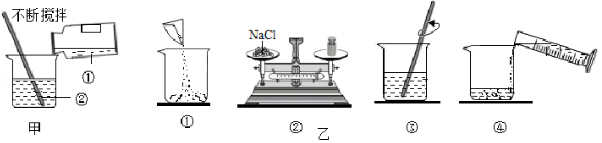
A.浓硫酸
B.水
C.引流
D.防止局部温度过高,造成酸液飞溅
(2)实验室配制一定溶质质量分数的氯化钠溶液的操作过程如图乙所示,正确的操作顺序是 (填字母序号)。
A.①②③④
B.②①④③
C.②①③④
2021年“世界水日”的主题为“珍惜水、爱护水”。
(1)2021年5月10日,“南水北调东线北延应急供水工程”启动向天津等地供水,以缓解我市可利用淡水资源 的现状。
(2)下列有关保护水资源的说法正确的是 (填序号)。
A.生活污水可直接排放
B.工业上对污染的水体作处理使之符合排放标准后再排放
C.农药、化肥的施用会造成水体污染,应该禁止施用
(3)如图是利用海水提取粗盐的过程。

根据海水晒盐的原理,下列说法正确的是 (填序号)。
A.进入贮水池中的海水,氯化钠的质量逐渐减少
B.在蒸发池中,海水中氯化钠的质量逐渐增加
C.析出晶体后,母液中的氯化钠溶液达到饱和
(4)某同学配制50g溶质质量分数为10%的氯化钠溶液。
①需要固体氯化钠的质量为 g。
②配制过程有以下步骤:a.称量及量取b.计算c.溶解d.装瓶贴标签,正确顺序是
(填序号)。
A.bcad
B.bacd
③将50g溶质质量分数为10%的氯化钠溶液,稀释成5%的氯化钠溶液,需要加水 g。
(5)为研究水的组成,某同学进行了电解水实验。
①电解水的化学方程式为 ;
②电解水的实验证明水是由 元素组成的。
氯化钠是生产、生活中的一种重要化合物,应用很广泛。
Ⅰ.图甲和图乙分别是钠原子和氯原子的原子结构示意图。

(1)图甲中的x= 。
(2)金属钠与氯气反应时,由图乙的结构可知,氯原子容易得到钠失去的1个电子,从而形成最外层有 个电子的相对稳定的氯离子,氯离子用化学符号表示为 。
Ⅱ.如表是氯化钠在不同温度下的溶解度数据。
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
37.8 |
(1)30℃时,将10g氯化钠加入到50g水中,充分搅拌后,所得到的氯化钠溶液属于
(填“饱和”或“不饱和”)溶液。
(2)医用盐水(溶质为NaCl)的溶质质量分数为0.9%,现有200mL该盐水(假定该溶液的密度为1g/mL),其中含NaCl的质量为 g。
(3)学生化学实验活动之一:配制50g质量分数为6%的氯化钠溶液,该实验需要的仪器有药匙、托盘天平、玻璃棒、胶头滴管、 (从下列图中选择写出名称)。

Ⅲ.工业上常用电解饱和食盐水的方法来制取氢氧化钠、氯气和氢气,其化学反应方程式可表示为:xNaCl+yH2O zNaOH+wH2+vCl2↑,若w=v=1,那么x=y=z=
zNaOH+wH2+vCl2↑,若w=v=1,那么x=y=z=
(填数字)。
某同学配制100g质量分数为11%的葡萄糖溶液,下列操作会导致所配溶液浓度偏高的是( )
A.用托盘天平称葡萄糖时,砝码放在左盘
B.转移葡萄糖时,纸上有少量残留
C.用量筒量取水时,俯视液面
D.配好溶液装入试剂瓶时,有少量洒出
配制100g质量分数为16%的Na2CO3溶液,用于演示灭火器原理。回答下列问题。
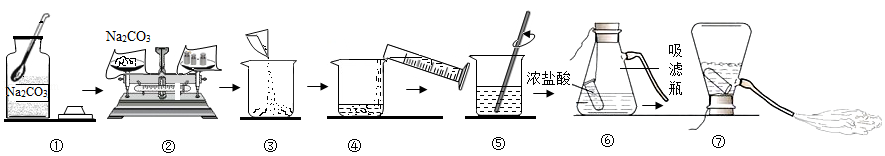
(1)计算Na2CO3的质量为 g,称量Na2CO3的仪器名称是 。
(2)20℃时,Na2CO3的溶解度为21.5g,⑤中的溶液 (填“是”或“不是”)该物质的饱和溶液。
(3)将烧杯中溶液倒入吸滤瓶的操作是 ,从橡胶管喷出大量液体的原因是 。
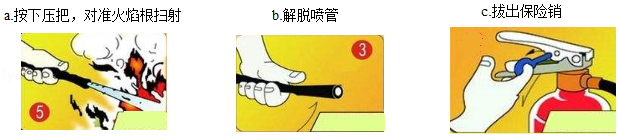
(4)酒精(C2H5OH)可作燃料,在空气中完全燃烧的化学方程式是 。酒精燃烧失火,可用干粉灭火器灭火。NaHCO3是干粉的主要成分,俗称是 。用干粉灭火器灭火的正确操作顺序是 → → (填序号)。
从如图选择仪器,配制60g溶质质量分数为10%的NaCl溶液。

(1)需要称量NaCl的质量为 g。
(2)量取水用到的仪器有 (写名称)。
(3)从配好的溶液中倒出10g,其中溶质和溶剂的质量比为 。
水和溶液对于人类的生产和生命活动有重大的意义。
(1)生活中可以用 区分硬水和软水,通过 的方法将硬水软化。
(2)电解水的实验中,正负两极产生气体的体积比为 ,通过实验可以得出水是由 ___ 组成的。
(3)用氯化钠固体和水配制6%的氯化钠溶液。如图正确的操作顺序是 (填字母序号),若量取水时仰视读数,其它操作均正确,则配制的氯化钠溶液中溶质质量分数 6% (填">""<"或"=")。
