化学是一门以实验为基础的学科,规范的实验操作是实验成功的保障。下列实验操作正确的是( )
| A. |
闻药品气味 |
B. |
加热固体 |
| C. |
过滤泥水 |
D. |
熄灭酒精灯 |
我国是一个历史悠久、文化灿烂的国家,古代诗词歌赋百花齐放、绚丽多彩。下列诗词中涉及化学变化的是( )
| A. |
白玉为党金作马 |
B. |
暗香浮动月黄昏 |
| C. |
蜡炬成灰泪始干 |
D. |
日照香炉生紫烟 |
安全重于泰山,危险化学品必须贴警示标识。浓硫酸应该贴的警示标识是( )
| A. |
|
B. |
|
C. |
|
D. |
|
某学习小组用不同浓度的溶液浇灌植物,研究重金属对植物生长的影响。
(1)该小组首先研究了 的影响。每次施用的浇灌液均为 ,配液方案如下:
(本研究所用溶液很稀,密度均近似看作 )
|
编号 |
浇灌液中CuSO4的 浓度 |
总体积/mL |
5%CuSO4溶液的 用量/mL |
水的用量/mL |
|
盆1 |
5% |
100 |
100 |
0 |
|
盆2 |
3% |
100 |
60 |
40 |
|
盆3 |
1% |
100 |
a |
b |
|
盆4 |
w |
100 |
c |
d |
①补充盆3的配液数据:a=______,b=______。
②为了获得严谨的结论,合理设计盆4的配液方案:w=______,d=______。
(2)该小组还研究了 的影响。研究结束后该小组将未用完的 溶液和 溶液直接混合,准备作无害化处理。
①混合后产生大量白色沉淀,反应的化学方程式为______。
②过滤,所得蓝色滤液中含有的溶质可能是:
假设一:只有 假设二: 和 假设三:______。
③设计实验确定蓝色滤液的成分,完成下表:
|
实验操作 |
现象与结论 |
|
取少量滤液于试管中,______。 |
______说明假设二不成立。 |
|
______。 |
______,说明假设三成立。 |
通过观察和实验等方法获取证据是科学探究的重要环节。
(1)向少量 沉淀中加入稀盐酸,观察到______,可判断发生了反应。
(2)向 溶液中通入 ,观察到______,可判断发生了反应。
(3)向氢氧化钙溶液中滴加稀盐酸,无明显现象。两位同学欲获取反应发生的证据。
①甲同学向滴有酚酞溶液的氢氧化钙溶液中,逐滴滴加稀盐酸至足量,溶液由红色变成无色,证明溶液中______,可判断 与 发生了反应。
②乙同学将氢氧化钙溶液与稀盐酸混合,然后检验了混合液中含有 和 ,他据此认为 与 发生了反应,且生成了 。你认为乙同学是否找到了反应发生的证据?请说出你的观点并阐述理由:______。
(4)如图a所示,向 稀溶液中缓缓通入 气体,测定该过程中溶液导电能力的变化,实验结果如图b.(溶液体积、温度的变化可忽略)

①分析A→B段变化,其他条件相同,导电能力: ______ 。(填“>”“<”或“=”)
②分析B→C段变化,溶液的导电能力除了与离子种类有关,还与______有关。
制盐在我国有着悠久的历史。某盐湖水样品含有 及少量 和 ,某小组从中获取 和 的主要过程如下:
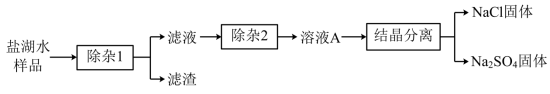
(1)“除杂1”应依次加入的两种试剂是______、______,“除杂2”应加入的试剂是______。(除杂限选试剂: )
(2)将“溶液A”在 蒸发浓缩,至有少量固体析出。

①该小组分析溶解度曲线,推测析出的少量固体是 ,但检验后却发现是 。请作出合理解释:______。
②该小组停止蒸发浓缩,经______、过滤得到大量 固体及母液;将母液中的 分离出来,操作是______。
(3)设计由硫磺(单质硫)生产 的转化路径,依次写出反应的化学方程式:______。(提示:常见 价硫的化合物可与 化合为 价硫的化合物)
我国古代科技璀璨夺目,金属的冶炼与使用在当时已处于世界先进水平。
(1)日常生活中,适合制作电缆的金属是______(填标号)。
| A. |
金 |
B. |
铜 |
C. |
汞 |
D. |
钨 |
(2)明代《天工开物》描述了锡的冶炼方法,如图a。
①原料锡砂中的 和木炭反应得到锡和二氧化碳,化学方程式为______。
②炼锡时混入少许铅形成合金,产物更易熔化流出,原因是______。
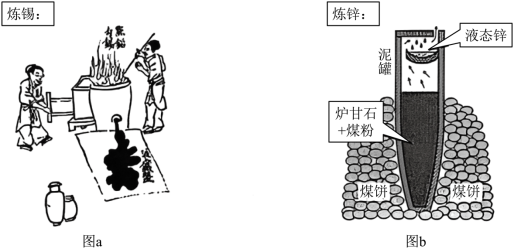
(3)图b为古代炼锌工艺原理示意图。炉甘石成分是 ,高温易分解生成 。
①泥罐外煤饼的主要作用是燃烧提供热量,泥罐内煤粉的主要作用是______。
②已知锌的沸点为 。泥罐下部温度可达 ,上部约为 ,该工艺从反应混合物中收集液态锌的方法属于______(填标号)。
| A. |
结晶 |
B. |
蒸发 |
C. |
蒸馏 |
D. |
升华 |
③必须冷却后才能取锌,是为了防止发生反应:______(写化学方程式)。
(4)湿法冶金利用置换反应。向 混合液中加入 粉,充分反应后过滤。若滤渣中有两种金属,则滤液中一定不含的金属阳离子是______。
磷及其化合物广泛应用于新能源汽车电池的制造,如 等。
(1)白磷保存在水中可以防止自燃,主要原因是______。
(2)测定空气中氧气含量时,消耗 氧气至少有______ 红磷参加反应。
(3)磷有多种化合价, 读作______;已知 (磷酸),磷酸根离子的化学符号是______;根据化合物的分类, 属于______。
关于下列实验的说法,正确的是( )

| A. |
实验①:滴有浓硫酸的部位变黑,说明浓硫酸有腐蚀性 |
| B. |
实验②:试管壁发烫,说明物质溶解过程伴随热量变化 |
| C. |
实验③:反应后总质量减小,说明该反应不符合质量守恒定律 |
| D. |
实验④:氨气用向下排空气法收集,说明氨气的密度比空气大 |
钴( )的金属活动性与铁相似,钴的化合物相关性质如下、下列预测合理的是( )
|
物质 |
|
|
|
|
|
在水中的溶解性 |
难溶,灰绿色 固体 |
难溶,粉红色 固体 |
易溶,溶液呈 粉红色 |
难溶,粉红色 固体 |
| A. |
能从 溶液中置换出 |
| B. |
能与盐酸反应得到粉红色溶液 |
| C. |
能与盐酸反应生成 |
| D. |
可由 与 溶液反应制得 |
下列果汁或饮料中,呈弱碱性的是( )
| A. |
苹果汁( ) |
B. |
番茄汁( ) |
| C. |
西瓜汁( ) |
D. |
苏打水( ) |
是重要的化工原料, 和 反应的微观示意图如下,下列说法正确的是( )
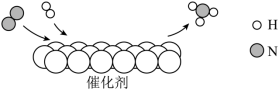
| A. |
常温下 的化学性质很活泼 |
| B. |
|
| C. |
|
| D. |
反应前后分子种类和数目发生变化 |
用电解水实验探究水的元素组成,下列说法不正确的是( )
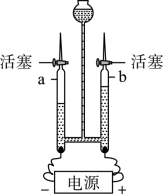
| A. |
管和 管中气体体积比约为 |
| B. |
管中的气体能使燃着的木条烧得更旺 |
| C. |
该探究说明水中含有氢分子和氧分子 |
| D. |
该探究的依据是化学变化前后元素种类不变 |
液氢、煤油(含 元素)、液氧可用作神州飞船运载火箭的推进剂,下列说法不正确的是( )
| A. |
火箭发射时仅靠空气不足以使燃料充分燃烧 |
| B. |
液氢和煤油完全燃烧的反应都是化合反应 |
| C. |
液氢是高能燃料且燃烧后的产物无污染 |
| D. |
飞船进入轨道后主要利用太阳能维持工作 |