我校高一化学兴趣小组的同学们为探究铁与浓硫酸的反应,设计了如图所示装置进行实验。
(1)实验过程中,观察到B中的实验现象是 ;写出C中发生反应的离子方程式 。
(2)浓硫酸与足量的铁丝反应一段时间后,若观察到从C中有少量的气泡冒出,此气泡的成分是 。试分析产生该气体的原因 。
(3)用“可抽动的铁丝”代替“直接投入铁片”的优点是 ;
(4)反应一段时间后,他们对A中溶液的金属阳离子进行了探究
①提出假设:
假设1: ;
假设2: ;
假设3:溶液中存在Fe2+和Fe3+。
②已知假设3是正确的,选择合适的试剂,设计实验验证上述假设3,写出实验操作步骤、实验现象及结论。限选试剂:稀HNO3、氯水、酸性KMnO4溶液、NaOH溶液、KSCN溶液。
| 实验操作步骤 |
实验现象 |
结论 |
| Ⅰ ; |
; |
溶液中存在Fe3+; |
| Ⅱ 。 |
。 |
。 |
(1)滑石一种硅酸盐矿物,其化学式为Mg3Si4O10(OH)2,用氧化物的形式表示为 。
(2)除去下列物质中所含杂质(括号内为杂质),写出除去杂质的试剂。
①Fe2O3(Al2O3) ②NO(NO2)
③Cl2 (HCl) ④FeCl3 (FeCl2)
(3)用铝箔包裹0.1mol金属钠,用针扎若干小孔,放入水中,完全反应后,用排水取气法收集到标准状况下气体的体积是_________(填字母序号)
a.1.12Lb.>1.12Lc.<1.12L
物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图所示,回答下列问题:
(1)Y是 (化学式)。
(2)将X与Y混合,可生成淡黄色固体,书写相关化学方程式 。
(3)将X的水溶液久置于空气中会变浑浊,说明X具有 性质。
(4)烧杯中加一些蔗糖,滴几滴水,并倒入一些W的浓溶液,用玻璃棒搅拌,观察到的所有现象为 ,说明W的浓溶液具有 、 和 性质。
(5)欲制备Na2S2O3,从氧化还原角度分析,合理的是 (填序号)。
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4 d.SO2 + Na2SO4
将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如下图所示。则下列说法不正确的是
| A.生成的氢气在标准状况下的体积为11.2 L |
| B.最初20 mLNaOH溶液用于中和过量的硫酸 |
| C.硫酸的物质的量浓度为2.5 mol/L |
| D.镁和铝的总质量为9 g |
用以下三种途径来制取等质量的硝酸铜:①铜与稀硝酸反应;②铜与浓硝酸反应;③铜先与氧气反应生成氧化铜,氧化铜再跟稀硝酸反应。以下叙述不正确的是
| A.三种途径所消耗的铜的质量相等 |
| B.所消耗的硝酸的物质的量是①>②>③ |
| C.途径③的制备方法是最符合“绿色化学”理念的 |
| D.途径①中被氧化的铜与被还原的硝酸的物质的量比是3:2 |
某无色混合气体中可能含有Cl2、O2、HCl、SO2、NO2、NO、NH3中的两种或多种。将此无色混合气体通过品红溶液后,品红溶液褪色;把剩余气体排入空气中,气体很快变为红棕色,该无色混合气体遇浓盐酸未看到明显现象。下列关于原混合气体成分的判断正确的是
| A.一定有SO2、NH3和NO | B.一定有NO和HCl |
| C.可能有Cl2和O2 | D.一定没有Cl2、NO2、NH3和O2 |
下列说法正确的是
| A.某溶液中滴加硝酸酸化的Ba(NO3)2溶液有白色沉淀,该溶液一定有SO42- |
| B.某溶液中滴加盐酸,产生无色无味的气体,将该气体通入澄清的石灰水中产生白色沉淀,则该溶液一定有CO32- |
| C.某溶液中滴加NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,则该溶液中一定有NH4+ |
| D.某溶液中滴加AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,则该溶液中一定有Cl- |
关于SO2的说法有:
①SO2是一种大气污染物;
②SO2和Cl2都有漂白作用,且这两种物质的漂白原理相同;
③工业上可用潮湿的石灰石粉末吸收SO2;
④SO2溶于水得硫酸,SO2是一种酸性氧化物;
⑤SO2是硫及某些含硫化合物在空气中燃烧的产物;
⑥SO2可以使酸性高锰酸钾溶液褪色,因为SO2具有漂白作用。其中正确的是
| A.①②⑤ | B.①③④⑤ | C.①③⑤ | D.①③⑤⑥ |
只用一种试剂就可将AgNO3、KSCN和H2SO4、NaOH四种无色溶液区分,这种试剂
是
| A.Fe(NO3)3溶液 | B.FeCl2溶液 | C.BaCl2溶液 | D.FeCl3溶液 |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.71g氯气中氯原子数为 NA |
| B.标准状况下,22.4 LNH3所含的电子数为10NA |
| C.5.6g Fe在足量氯气中燃烧转移的电子数为2NA |
| D.标准状况下,11.2 L H2O中含有分子的数目为0.5NA |
下列离子方程式正确的是
| A.铜和稀硝酸的反应:Cu2++4H++2NO3-=Cu2++2NO2↑+2H2O |
| B.氯化铁腐蚀印刷电路板:Fe3++Cu = Fe2++Cu2+ |
| C.氯化铝溶液加入氨水:Al3++3OH-= Al(OH)3↓ |
D.实验室制氯气:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
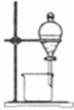
完成下列实验所选择的装置或仪器不正确的是
| A |
B |
C |
D |
|
| 实验 |
分离水和酒精 |
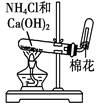
用铵盐和碱制取NH3 |
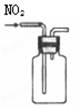
用排空气法收集NO2 |
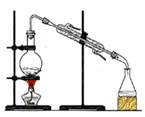
用自来水制取蒸馏水 |
| 装置 或 仪器 |
 |
 |
 |
 |
在无色透明强酸性溶液中,能大量共存的离子组是
| A.K+、MnO4-、Mg2+、SO42- | B.K+、Na+、Cl-、CO32- |
| C.Zn2+、Al3+、NO3-、Cl- | D.Na+、Fe2+、NO3-、SO42- |