通常情况下,多个羟基连在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双键的结构: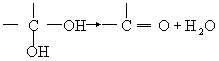
下面是9个化合物的转变关系
(1)化合物①是______,它跟氯气发生反应的条件A是______。
(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨,⑨的结构简式是_______,名称是______。
(3)化合物⑨是重要的定香剂,香料工业上常用化合物②和⑧直接合成它。此反应的化学方程式是____________。
图中的每一方格表示有关的一种反应物或生成物,其中粗框表示初始反应物(反应时加入或生成的水,以及生成沉淀J时的其他产物均已略去)。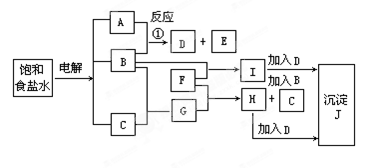
请填写下列空白:
(1)物质B是______,F是_______,J是______。
(2)反应①的离子方程式是 。
A,B,C和D分别是NaNO3,NaOH,HNO3和Ba(NO3)2四种溶液中的一种。现利用另一种溶液X,用如下图所示的方法,即可将它们一一确定。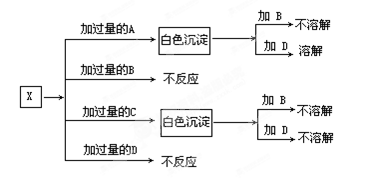
试确定A,B,C,D,X各代表何种溶液。
A:______B:______C:______D:______X:______
现有一包白色粉末,其中可能含有CaCO3、Na2CO3、Na2SO4、NaCl、CuSO4,进行如下实验①溶于水得无色溶液;②向溶液中加入BaCl2溶液生成白色沉淀,再加盐酸时沉淀消失,据上述实验现象推断:一定不存在___________,一定存在_____________,可能存在_________,对于可能存在的物质应如何近一步检验?写出简要的步骤和有关的离子方程式。
有A、B、C、D、E、F六种化合物,它们之间的反应关系如下:
①A +B → C + E
②C +NaOH→蓝色沉淀D + F
③D → A +E
④F +Ba(NO3)2→白色沉淀+NaNO3
(1)试写出它们的化学式:
A___________;B___________;C__________;D__________;E_________;F_________.
(2)写出反应①、④的离子方程式。
①___________________________________;
④___________________________________。
有五瓶溶液分别为a、b、c、d、e,它们可能是AgNO3、BaCl2、HCl、K2CO3、K2SO3.现做如下实验:a与b混合;a与c混合;a与d混合;c与d混合;e与d混和;e与a混合,都有白色沉淀生成,b与c混合有无色无味气体生成,则五种溶液是a________;b_________;c________;d_________;e_________。
A、B、C、D四种可溶性盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是NO3-、SO42-、Cl-、CO32-中的某一种。
(1)若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色。
(2)若向(1)的四支试管中分别加盐酸,B盐溶液有沉淀产生,D盐溶液有无色无味气体逸出。
根据(1)(2)实验事实可推断它们的化学式为:
A. _________;B. _________;C. _________;D. ___________。
将HCl、H2SO4、Ba(NO3)2三种溶液,按一定顺序滴入到Na2CO3溶液中至恰好完全反应有以下现象:
(1)加入A时有白色沉淀;
(2)往(1)中沉淀里加入B时沉淀溶解,并有气体逸出;
(3)往(2)中溶液里加入C时,又有白色沉淀生成。
根据以上现象判断A、B、C分别是HCl溶液、H2SO4溶液、Ba(NO3)2溶液中的哪种?
A_________________,B_______________,C__________________.
写出B使沉淀溶解的离子方程式____________________________________________.
(9分)下列物质之间能够发生如图所示的化学反应,合金由两种金属组成,取C溶液进行焰色反应则火焰呈黄色。在反应中产生的水均未在图中标出。其中G→H的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3

(1)写出下列物质的化学式:A: D: F:
(2)标出下列反应的电子转移情况:4Fe(OH)2 + O2 + 2H2O === 4Fe(OH)3
(3)写出下列反应的离子方程式:
A→B: 、
K→D: 。
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的最高价氧化物对应水化物与其氢化物能生成盐M;D与A同主族,且与E同周期;E元素原子的最外层电子数比次外层电子数少2;A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若干种化合物。请回答:
(1) C和E两种元素相比较,原子得电子能力较强的元素在周期表中的位置为 ,以下三种说法中,可以验证C和E得电子能力强弱的是(填写编号) ;
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,C元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
(2)盐M中含有的化学键类型有 ;
(3)A、B、C、E可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中相互反应的离子方程式为 。
(4)B2A4是一种可燃性液体,B2A4—空气燃料电池是一种碱性燃料电池,B2A4的氧化产物为B2。则负极上的电极反应式为 。
(5)已知1molD与水反应放出283.5kJ的热量,试写出D与水反应的热化学反应方程式 ;
(7分)A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
ABCD
请回答下列问题:
(1)若常温下A为淡黄色固体单质,D为强酸,则A、D分别为(填写化学式)A:________,D:________。
写出D→B的化学方程式:____________________________。
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红。则A为______________,写出A→B转化的化学方程式:________________________________________________。
信息时代产生的大量电子垃圾对环境构成了极大的威胁。某"变废为宝"学生探究小组将一批废弃的线路板简单处理后,得到含70%、25%
、4%
及少量
、
等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
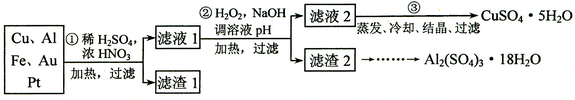
请回答下列问题:
⑴ 第①步与酸反应的离子方程为;
得到滤渣1的主要成分为。
⑵ 第②步加的作用是,使用H2O2的优点是;调溶液pH的目的是使生成沉淀。
⑶ 用第③步所得·
制备无水
的方法是。
⑷ 由滤渣2制取·18
,探究小组设计了三种方案:

上述三种方案中,方案不可行,原因是;
从原子利用率角度考虑,方案更合理。
⑸ 探究小组用滴定法测定·5
(
=250)含量。取
试样配成100
溶液,每次取20.00
,消除干扰离子后,用
标准溶液滴定至终点,平均消耗
溶液
。滴定反应如下:
+
=
+
写出计算·5
质量分数的表达式
=;
下列操作会导致·5
含量的测定结果偏高的是。
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除净可与EDTA反应的干扰离子
已知:,
代表原子或原子团。
是一种有机合成中间体,结构简式为:
,其合成发生如下:

其中,、
、
、
分别代表一种有机物,合成过程中的其他产物和反应条件已略去。
与
在一定条件下反应可以生成酯
,
的相对分子质量为168。
请回答下列问题:
(1)能发生反应的类型有(填写字母编号)
| A. | 取代反应 | B. | 水解反应 | C. | 氧化反应 | D. | 加成反应 |
(2)已知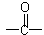 为平面结构,则
为平面结构,则分子中最多有个原子在同一平面。
(3)写出与
在一定条件下反应生成
的化学方程式。
(4)写出含有3个碳原子且不含甲基的的同系物的结构简式:。
(5)写出第②步反应的化学方程式。
香豆浆是一种天然香料,存在于黑香豆、兰花等植物中。工业上常用水杨醛与乙酸酐在催化剂存在下加热反应制得:
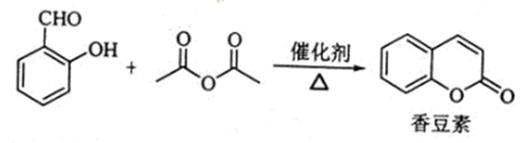
以下是由甲苯为原料生产香豆素的一种合成路线(部分反应条件及副产物已略去)
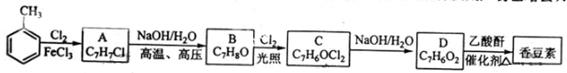
已知以下信息:
① A中有五种不同化学环境的氢
② B可与溶液发生显色反应
③ 同一个碳原子上连有连个羧基通常不稳定,易脱水形成羧基。
请回答下列问题:
(1) 香豆素的分子式为;
(2) 由甲苯生成A的反应类型为;A的化学名称为
(3) 由B生成C的化学反应方程式为;
(4) B的同分异构体中含有苯环的还有种,其中在核磁共振氢谱中只出现四组峰的有种;
(5) D的同分异构体中含有苯环的还有中,其中:
① 既能发生银境反应,又能发生水解反应的是(写解构简式)
② 能够与饱和碳酸氢钠溶液反应放出的是(写解构简式)
菠萝酯是一种具有菠萝香气的食用香料,是化合物甲与苯氧乙酸 发生酯化反应的产物。
发生酯化反应的产物。
(1)甲一定含有的官能团的名称是。
(2)5.8 g甲完全燃烧可产生0.3 mol 和0.3 mol
,甲蒸气对氢气的相对密度是29,甲分子中不含甲基,且为链状结构,其结构简式是。
(3)苯氧乙酸有多种酯类的同分异构体。其中能与溶液发生显色反应,且有2种一硝基取代物的同分异构体是(写出任意2种的结构简式)。
(4)已知:



菠萝酯的合成路线如下:

①试剂X不可选用的是(选填字母)。
a.溶液 b.
溶液
c.溶液 d.
②丙的结构简式是,反应Ⅱ的反应类型是。
③反应Ⅳ的化学方程式是。